一定质量的乙醇在氧气不足的情况下,燃烧生成2.7g水、2.2g二氧化碳和一定质量的一氧化碳,则参加反应的乙醇的质量为___________ ;此反应的化学方程式为___________ 。
2024·河南驻马店·一模 查看更多[2]
更新时间:2024-04-26 08:46:14
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】钴(Co)是一种银白色金属,其化学性质与铁相似,钴及其化合物广泛应用于磁性材料、电池材料等领域。经查阅资料,Co(NO3)2和CoSO4溶液均呈粉红色,Co(OH)2难溶于水。
(1)①向Co(NO3)2溶液中滴入少量氢氧化钠溶液,反应的化学方程式为______ 。
②向CoSO4溶液中加入足量锌粉,观察到的现象是______ 。
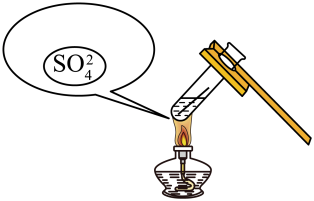
(2)将一段金属钴条(表面覆盖有CoCO3、Fe2O3等物质)放入过量的稀硫酸中,如图:______ (填化学式),并请在图中补充完善反应后溶液中含有的粒子种类(粒子数目不作要求,不考虑水)_____ 。
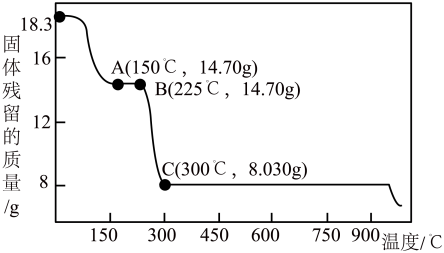
(3)四氧化三钴(Co3O4)是制备新能源汽车电池的原料之一,工业上可以将草酸钴晶体(CoC2O4·2H2O,相对分子质量为183)在空气中煅烧制得。实验室模拟其制备方法,测得煅烧过程中质量变化与温度的关系如图所示:______ g。
(1)①向Co(NO3)2溶液中滴入少量氢氧化钠溶液,反应的化学方程式为
②向CoSO4溶液中加入足量锌粉,观察到的现象是
(2)将一段金属钴条(表面覆盖有CoCO3、Fe2O3等物质)放入过量的稀硫酸中,如图:
(3)四氧化三钴(Co3O4)是制备新能源汽车电池的原料之一,工业上可以将草酸钴晶体(CoC2O4·2H2O,相对分子质量为183)在空气中煅烧制得。实验室模拟其制备方法,测得煅烧过程中质量变化与温度的关系如图所示:
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】在点燃条件下,4.4gC3H8与12.8g氧气恰好完全反应,生成7.2g水、4.4g二氧化碳和agX。则a=_____ ;该反应的化学方程式为______ 。
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】氯化铜晶体(CuCl2·xH2O)是重要的化工原料,可用作催化剂、消毒剂等。用含少量铁的氧化铜制取氯化铜晶体(CuCl2·2H2O),操作流程如图,回答相关问题。

已知:有关金属阳高子形成氢氧化物时溶液的pH:
(1)“酸浸”步骤:稀盐酸能否换成“稀硫酸”______ (填“能”或“不能”):实际操作中常将铁和氧化铜碾成粉末,这样做的目的是______ ;“酸浸”后所得溶液中大量含有的离子共有______ 种。
(2)“氧化”步骤:在工业生产中常用双氧水作为试剂A,将FeCl2转化为FeCl3,该反应的化学方程式为______ 。
(3)“过滤”步骤:常用氧化铜作为试剂B调节浴液的pH,为提高产品纯度、降低原料损耗,应将溶液pH控制在______ 范围。
(4)“结晶”步骤:从滤液中得到CuCl2晶体的方法是:加热浓缩→______ →过滤→洗涤→低温烘干。
(5)已知CuC12加热到一定的温度就会分解为CuCl,取40.5gCuCl2加热到一定的温度时得到33.4gCuCl2和CuCl的混合物,则该混合物中CuCl2的质量为______ 。

已知:有关金属阳高子形成氢氧化物时溶液的pH:
| pH | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀的pH | 1.9 | 5.4 |
| 沉淀完全的pH | 3.2 | 6.9 |
(2)“氧化”步骤:在工业生产中常用双氧水作为试剂A,将FeCl2转化为FeCl3,该反应的化学方程式为
(3)“过滤”步骤:常用氧化铜作为试剂B调节浴液的pH,为提高产品纯度、降低原料损耗,应将溶液pH控制在
(4)“结晶”步骤:从滤液中得到CuCl2晶体的方法是:加热浓缩→
(5)已知CuC12加热到一定的温度就会分解为CuCl,取40.5gCuCl2加热到一定的温度时得到33.4gCuCl2和CuCl的混合物,则该混合物中CuCl2的质量为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】中国的高铁建设被誉为中国经济发展的奇迹,频频刷新世界纪录。请结合所学的化学知识,回答下列有关问题:
(1)高铁列车上提供的下列食品中,含蛋白质最高的物质是____ (填序号);
①矿泉水;②橙汁;③牛奶;④饼干
(2)铁轨属于_____ (填“有机合成材料”或“金属材料”),雨后的铁轨表面易产生少量的锈迹,这是因为铁与空气中的___ 同时接触发生了反应;
(3)铝热剂是修建铁路时常用的焊接材料,其反应原理是铝在高温条件下与氧化铁反应得到熔融的铁与另一种氧化物,写出其化学反应方程式____ ;
(4)某品牌的空气净化剂含有过氧化钠(Na2O2),它可以使车厢里的二氧化碳转化为碳酸钠和氧气,7.8g过氧化钠完全反应后可产生氧气的质量为____ g;
(1)高铁列车上提供的下列食品中,含蛋白质最高的物质是
①矿泉水;②橙汁;③牛奶;④饼干
(2)铁轨属于
(3)铝热剂是修建铁路时常用的焊接材料,其反应原理是铝在高温条件下与氧化铁反应得到熔融的铁与另一种氧化物,写出其化学反应方程式
(4)某品牌的空气净化剂含有过氧化钠(Na2O2),它可以使车厢里的二氧化碳转化为碳酸钠和氧气,7.8g过氧化钠完全反应后可产生氧气的质量为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A~G是初中化学常见的物质,其转化关系如下图所示。其中,A是一种紫黑色固体;B和G均是黑色固体,B和F的溶液混合后也能产生D;J能用于光合作用。

(1)F的名称为______ ,M的化学式为______ 。
(2)由D转化为J的化学方程式为______ ,该反应的类型为______ 反应(填基本反应类型)
(3)反应①化学方程式为______ 。

(1)F的名称为
(2)由D转化为J的化学方程式为
(3)反应①化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】天然气中常含有少量H2S。脱硫是资源利用和环境保护的重要研究课题。
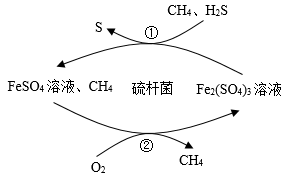
(1)生物脱H2S。反应的原理如图所示:
①该脱硫过程在_______ 条件下进行(填“酸性”或“碱性”)。
②硫杆菌存在时,FeSO4与氧气反应的速度是无菌时的5×105的倍,该菌的作用是_______ 。依据图1和图2判断,使用硫杆菌的最适宜条件为_______ 。若温度过高,反应速度下降,其可能原因是_______ 。


(2)H2O2脱H2S。随着参加反应的分子数之比【N(H2O2):N(H2S)】变化,反应产物发生变化。当N(H2O2):N(H2S)=4:1时,除生成H2O外,另一种产物的分子式为_______ 。
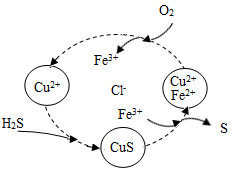
(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如下图所示。其中化合价不变的元素是_______ (填元素符号)。
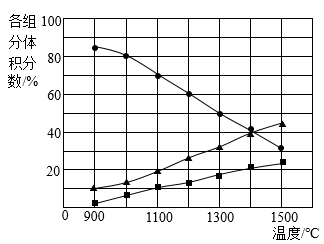
(4)高温分解H2S生成硫蒸气和H2.若在不同温度下反应足够长的时间,混合气体中各组分的体积分数(即各组分所占气体分子个数百分比)如图所示,则H2S在高温下分解反应的化学方程式为_______ 。

(1)生物脱H2S。反应的原理如图所示:
①该脱硫过程在
②硫杆菌存在时,FeSO4与氧气反应的速度是无菌时的5×105的倍,该菌的作用是


(2)H2O2脱H2S。随着参加反应的分子数之比【N(H2O2):N(H2S)】变化,反应产物发生变化。当N(H2O2):N(H2S)=4:1时,除生成H2O外,另一种产物的分子式为
(3)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如下图所示。其中化合价不变的元素是

(4)高温分解H2S生成硫蒸气和H2.若在不同温度下反应足够长的时间,混合气体中各组分的体积分数(即各组分所占气体分子个数百分比)如图所示,则H2S在高温下分解反应的化学方程式为

您最近一年使用:0次
填空与简答-科普阅读题
|
较难
(0.4)
解题方法
【推荐1】我国航空航天事业取得令人瞩目的成就,阅读以下相关主题科普材料,回答问题。材料一;神舟十三号载3名宇航员在太空执行任务,时长180天,空间站中常用水气整合系统实现 的清除和
的清除和 的再生(简易流程如下图),科学家通过填密计算,为了提供3名字航员在太空生活所需的
的再生(简易流程如下图),科学家通过填密计算,为了提供3名字航员在太空生活所需的 ,至少需从地球带486kg的水进行电解。
,至少需从地球带486kg的水进行电解。

材料二:我国探月工程实现“六战六捷”。未来还将探索在月球建设基地的可能,其中一个前提就是在月球上大规模制造 ,在月球上可以电解熔融月壤(含
,在月球上可以电解熔融月壤(含 、
、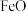 、CaO、
、CaO、 等)制造氧气。
等)制造氧气。
(1)分析材料一流程可知,可循环利用的化合物有______ (填物质的化学式),航天员呼吸属于缓慢______ 过程,并______ 热量。
(2)请计算电解486kg水能产生氧气的质量(填写具体计算过程)。
(3)月壤成分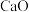 中含氧的质量分数为
中含氧的质量分数为______ %(结果保留小数点后一位)。理论上,电解等质量的下列氧化物,产生氧气最多的是______ 。
A. B.
B.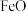 C.CaO
C.CaO
 的清除和
的清除和 的再生(简易流程如下图),科学家通过填密计算,为了提供3名字航员在太空生活所需的
的再生(简易流程如下图),科学家通过填密计算,为了提供3名字航员在太空生活所需的 ,至少需从地球带486kg的水进行电解。
,至少需从地球带486kg的水进行电解。
材料二:我国探月工程实现“六战六捷”。未来还将探索在月球建设基地的可能,其中一个前提就是在月球上大规模制造
 ,在月球上可以电解熔融月壤(含
,在月球上可以电解熔融月壤(含 、
、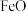 、CaO、
、CaO、 等)制造氧气。
等)制造氧气。(1)分析材料一流程可知,可循环利用的化合物有
(2)请计算电解486kg水能产生氧气的质量(填写具体计算过程)。
(3)月壤成分
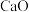 中含氧的质量分数为
中含氧的质量分数为A.
 B.
B.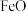 C.CaO
C.CaO
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】某纯净物1.6g在氧气中完全燃烧,生成4.4g二氧化碳和3.6g水,则消耗氧气的质量为___________ ;写出该物质燃烧的化学方程式:___________ 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】回答下列问题:
(1)某元素Q的氧化物相对分子质量为x,其硫酸盐的相对分子质量为y,则该元素的化合价可能是___________ (用x, y表示)。
(2)有氧气和二氧化硫的某混合气体,其氧元素质量分数为60%,则该混合气体中氧气与二氧化硫的质量比为___________ 。
(3)M元素的一个原子的质量是a克,N元素的相对原子质量为A,化合物MN2的相对分子质量为B,则W克MN2中M的原子数是___________ 。
(4)配制5%的盐酸1 L (ρ=1.025g/cm3),需取用36.5%(ρ=l.181g/cm3)的盐酸___________ mL(保留一位小数)。
(1)某元素Q的氧化物相对分子质量为x,其硫酸盐的相对分子质量为y,则该元素的化合价可能是
(2)有氧气和二氧化硫的某混合气体,其氧元素质量分数为60%,则该混合气体中氧气与二氧化硫的质量比为
(3)M元素的一个原子的质量是a克,N元素的相对原子质量为A,化合物MN2的相对分子质量为B,则W克MN2中M的原子数是
(4)配制5%的盐酸1 L (ρ=1.025g/cm3),需取用36.5%(ρ=l.181g/cm3)的盐酸
您最近一年使用:0次



