有一包固体粉末,可能由NaCl、Na2SO4、CuSO4、Na2CO3、BaCO3中的一种或几种组成。为确定其成分,某化学兴趣小组进行如下实验探究,请你参与探究并回答相关问题.
【提出问题】该固体粉末的成分是什么?
(1)【实验探究】
【交流与解释】
(2)白色沉淀C中加入过量的稀盐酸,产生气泡的反应方程式为_______ 。
(3)在老师的指导下,通过讨论,同学们认识到由上述实验探究尚不能得出固体粉末中含有NaCl,理由是________ (用方程式表示)。
为了进一步确定白色粉末中是否含有NaCl,继续进行如下探究。
(4)【继续探究】
通过上述实验探究,确定了该固体粉末的成分。
【拓展与反思】在混合溶液中,检验某种离子时,需排除离子间的相互干扰。
【提出问题】该固体粉末的成分是什么?
(1)【实验探究】
| 实验步骤 | 实验现象及结果 | 实验结论 |
| 取该白色粉末样品于烧杯,加足量水溶解 | 样品全部溶解,得到无色溶液A | 固体粉末中不含 |
| 取少量无色溶液A于试管,加入过量BaCl2溶液,充分反应后过滤 | 得到无色溶液B和白色沉淀C | 固体粉末中含有 |
| 向白色沉淀C中加入过量稀盐酸 | 沉淀部分溶解,并有气泡冒出 | |
| 在无色溶液B中滴加几滴AgNO3溶液 | 产生白色沉淀 | 固体粉末中含有NaCl |
【交流与解释】
(2)白色沉淀C中加入过量的稀盐酸,产生气泡的反应方程式为
(3)在老师的指导下,通过讨论,同学们认识到由上述实验探究尚不能得出固体粉末中含有NaCl,理由是
为了进一步确定白色粉末中是否含有NaCl,继续进行如下探究。
(4)【继续探究】
| 实验步骤 | 实验现象 | 实验结论 |
| 另取少量无色溶液A于试管中,加入过量的 | 产生白色沉淀 | 固体粉末中含有NaCl |
| 取实验⑤所得上层清液于试管,加入AgNO3溶液 | 产生白色沉淀 |
【拓展与反思】在混合溶液中,检验某种离子时,需排除离子间的相互干扰。
更新时间:2024-04-13 16:05:24
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】课堂上,老师取20g蔗糖放入烧杯中,加少量水使它润湿,注入10mL浓硫酸,搅拌,同学们看到蔗糖先变黑后“发酵”形成“黑面包”,同时还闻到刺激性气味,同学们判断黑色固体是碳,原因浓硫酸有强脱水性,形成“黑面包”的主要原因是什么?在老师指导下,同学们开展了探究活动。
【猜想与假设】浓硫酸与碳反应,生成大量气体使黑色固体膨胀。
【查阅资料】Ⅰ.浓硫酸与碳在加热条件下反应,生成物中有SO2、CO2两种气体;
Ⅱ.SO2是一种具有刺激性气味的气体,能与Ca(OH)2溶液反应生成白色沉淀;
Ⅲ.SO2能使品红溶液褪色,而CO2不能。
【实验探究】为验证碳与浓硫酸在加热条件下生成的气体产物,同学们在老师指导下设计并进行如图实验:

【事实与结论】(1)请将能得出对应结论的实验现象填入表中。
(2)碳与浓硫酸反应的化学方程式是_______________ ;
(3)浓硫酸与碳在加热条件下产生大量的SO2和CO2,使黑色固体膨胀,形成“黑面包”,猜想成立。
【反思与交流】(1)小明同学提出,因老师的演示实验没有进行加热,所以同学们的探究实验无意义,其他同学一致否定了他的说法,理由是____________ ;
(2)若B、E中试剂交换,______ (填“能”或“不能”)得出有CO2产生的结论,理由是______ ;
(3)C中酸性高锰酸钾溶液的作用是_________ 。
【猜想与假设】浓硫酸与碳反应,生成大量气体使黑色固体膨胀。
【查阅资料】Ⅰ.浓硫酸与碳在加热条件下反应,生成物中有SO2、CO2两种气体;
Ⅱ.SO2是一种具有刺激性气味的气体,能与Ca(OH)2溶液反应生成白色沉淀;
Ⅲ.SO2能使品红溶液褪色,而CO2不能。
【实验探究】为验证碳与浓硫酸在加热条件下生成的气体产物,同学们在老师指导下设计并进行如图实验:

【事实与结论】(1)请将能得出对应结论的实验现象填入表中。
| 验证气体 | 实验现象 | 实验结论 |
| SO2 | 有SO2产生 | |
| CO2 | 有CO2产生 |
(3)浓硫酸与碳在加热条件下产生大量的SO2和CO2,使黑色固体膨胀,形成“黑面包”,猜想成立。
【反思与交流】(1)小明同学提出,因老师的演示实验没有进行加热,所以同学们的探究实验无意义,其他同学一致否定了他的说法,理由是
(2)若B、E中试剂交换,
(3)C中酸性高锰酸钾溶液的作用是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某校化学兴趣小组的同学利用稀盐酸、碳酸钠、Ba(OH)2溶液三种物质探究“复分解反应发生的条件”,做了以下实验。

(1)大家一致认为在试管①中还需要加入______ 溶液才能证明发生了复分解反应。
(2)试管②中观察到的现象是______ ,试管③中反应的化学方程式为______ 。
(3)通过三组实验,同学们得出复分解反应发生的条件是______ 。
(4)兴趣小组的同学将试管③反应后的物质过滤,对滤液中溶质的成分进一步探究。
【提出问题】滤液中溶质的成分是什么?
【猜想假设】猜想一:NaOH;
猜想二:Ba(OH)2、NaOH
猜想三:______ 。
【设计实验】验证你的猜想正确
【反思拓展】
(5)同学们发现Ba(OH)2和NaOH化学性质相似,你认为Ba(OH)2的保存方法是______ 。
(6)步骤一中,加入足量CaCl2溶液的目的是______ 。

(1)大家一致认为在试管①中还需要加入
(2)试管②中观察到的现象是
(3)通过三组实验,同学们得出复分解反应发生的条件是
(4)兴趣小组的同学将试管③反应后的物质过滤,对滤液中溶质的成分进一步探究。
【提出问题】滤液中溶质的成分是什么?
【猜想假设】猜想一:NaOH;
猜想二:Ba(OH)2、NaOH
猜想三:
【设计实验】验证你的猜想正确
| 实验操作 | 现象 | 结论 |
| 步骤一:取试管③中滤液少量于试管中, 加入足量CaCl2溶液 | 有 | 猜想三正确 |
| 步骤二:静置一段时间,向上层清液中 滴加适量 | 有蓝色沉淀产生 |
【反思拓展】
(5)同学们发现Ba(OH)2和NaOH化学性质相似,你认为Ba(OH)2的保存方法是
(6)步骤一中,加入足量CaCl2溶液的目的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】黄河被宁夏人称为母亲河,对宁夏的发展有深远影响。某化学小组对黄河的用途,排入黄河废水的酸碱性、成分,黄河的防护治理等产生了浓厚兴趣,在老师的指导下他们展开了项目式学习探究。
项目一:调查黄河的用途
【资料检索】黄河是宁夏境内第一大河,具有灌溉、发电、工业和城市居民供水等用途。
【交流讨论】
(1)黄河水在进入千家万户之前,需要经过自来水厂的净化。自来水厂在净化水时会加入活性炭,其目的是___________ 。
项目二:探究某工厂排入黄河废水的酸碱性
(2)同学们获得了一瓶该工厂排入黄河的废水样品。他们用pH试纸测得废水的pH>7,说明该废水显___________ 性,该水对黄河水生生物的危害有___________ (写一条)。
项目三:探究该工厂排入黄河废水的成分
【信息检索】该废水中一定含有Na+,可能含有Ca2+、OH-、 中的一种或几种离子。
中的一种或几种离子。
【进行实验】
(3)为探究废水成分,同学们设计了如下实验方案:
【反思评价】
(4)步骤①中发生反应的化学方程式为___________ 。
项目四:黄河的防护治理
【小组讨论】
(5)为保护黄河水,全流域守护水质,让一泓清水入黄河,可采取的措施有________ (写一条)。
【成果分享】通过学习探究,同学们了解了黄河的用途,掌握了化学知识,提升了保护环境的意识。
项目一:调查黄河的用途
【资料检索】黄河是宁夏境内第一大河,具有灌溉、发电、工业和城市居民供水等用途。
【交流讨论】
(1)黄河水在进入千家万户之前,需要经过自来水厂的净化。自来水厂在净化水时会加入活性炭,其目的是
项目二:探究某工厂排入黄河废水的酸碱性
(2)同学们获得了一瓶该工厂排入黄河的废水样品。他们用pH试纸测得废水的pH>7,说明该废水显
项目三:探究该工厂排入黄河废水的成分
【信息检索】该废水中一定含有Na+,可能含有Ca2+、OH-、
 中的一种或几种离子。
中的一种或几种离子。【进行实验】
(3)为探究废水成分,同学们设计了如下实验方案:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量废水于试管中,加入 | 产生白色沉淀 | 废水中含有 |
| ②取步骤①反应后的上层清液于另一支试管中,滴加少量 | 无明显现象 | 废水中不含OH- |
【反思评价】
(4)步骤①中发生反应的化学方程式为
项目四:黄河的防护治理
【小组讨论】
(5)为保护黄河水,全流域守护水质,让一泓清水入黄河,可采取的措施有
【成果分享】通过学习探究,同学们了解了黄河的用途,掌握了化学知识,提升了保护环境的意识。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某学习小组根据碱的化学性质网络图进行了相关实验的探究。

(1)1号试管:向稀的氢氧化钠溶液中滴加无色酚酞,观察到的现象是_______ 。
(2)2号试管:向澄清石灰水中通入二氧化碳,发生反应的化学方程式为_______ 。
(3)3号试管:向氢氧化铜中滴加稀硫酸,当出现_______ 现象时,说明中和反应已完全反应。
(4)4号试管:向氢氧化钙溶液中滴加碳酸钠溶液,产生白色沉淀,过滤,滤液中的溶质可能是什么?
【提出猜想】猜想一:溶质只有NaOH;
猜想二:溶质为NaOH、Ca(OH)2;
猜想三:溶质为_______ 。
【实验探究】
【反思与评价】1 对所学的知识要及时归纳和总结。
2 实验时的废液应倒入_______ (选填“水池”或“废液缸”)中集中处理。

(1)1号试管:向稀的氢氧化钠溶液中滴加无色酚酞,观察到的现象是
(2)2号试管:向澄清石灰水中通入二氧化碳,发生反应的化学方程式为
(3)3号试管:向氢氧化铜中滴加稀硫酸,当出现
(4)4号试管:向氢氧化钙溶液中滴加碳酸钠溶液,产生白色沉淀,过滤,滤液中的溶质可能是什么?
【提出猜想】猜想一:溶质只有NaOH;
猜想二:溶质为NaOH、Ca(OH)2;
猜想三:溶质为
【实验探究】
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| (5) | 取少量滤液于5号试管中,加一定量的稀盐酸 | 猜想三错误 | |
| (6) | 另取少量滤液于试管中,加入一定量的 | 产生白色沉淀 | 猜想二正确 |
2 实验时的废液应倒入
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】将4cm光亮镁条放入一定量的稀HCl中,产生大量气泡后出现白色固体。
小组同学为探究白色不溶物的成分进行如下实验。
【资料】
在MgCl2溶液中,常温下发生反应:Mg+2H2O═Mg(OH)2↓+H2↑。
【猜想】
Ⅰ.生成的MgCl2过多而析出
Ⅱ.反应后有镁粉剩余Ⅲ.生成了Mg(OH)2沉淀
【实验】相同3次实验,过滤并用蒸馏水洗涤固体,直至最后一次洗涤所得滤液中滴加硝酸银溶液无___ (填现象),分别得到干燥洁净固体mg。
(1)对比实验:将mg固体与mg___ ,分别加入5mL蒸馏水中,充分振荡,观察固体有无明显减少。
结论:假设Ⅰ不成立。
(2)取m g固体,加入稀盐酸。若观察到___ 现象。
结论:假设Ⅱ也不成立。
(3)取m g固体,全部溶于稀硝酸,将所得溶液分成两等份。
①向一份溶液中滴加过量的NaOH溶液,生成了1.16gMg(OH)2沉淀;
②向另一份溶液中滴加过量的AgNO3溶液,生成了2.87g沉淀。
结论:假设Ⅲ也不成立,若已知白色固体化学式为[Mgx(OH)y___ z],则缺少的元素符号为___ 。
【结论】经计算分析x:z=___ ,x:y=___ 。
请写出得到白色固体和H2的化学方程式(已知两者计量数比为1:2):___ 。
小组同学为探究白色不溶物的成分进行如下实验。
【资料】
在MgCl2溶液中,常温下发生反应:Mg+2H2O═Mg(OH)2↓+H2↑。
【猜想】
Ⅰ.生成的MgCl2过多而析出
Ⅱ.反应后有镁粉剩余Ⅲ.生成了Mg(OH)2沉淀
【实验】相同3次实验,过滤并用蒸馏水洗涤固体,直至最后一次洗涤所得滤液中滴加硝酸银溶液无
(1)对比实验:将mg固体与mg
结论:假设Ⅰ不成立。
(2)取m g固体,加入稀盐酸。若观察到
结论:假设Ⅱ也不成立。
(3)取m g固体,全部溶于稀硝酸,将所得溶液分成两等份。
①向一份溶液中滴加过量的NaOH溶液,生成了1.16gMg(OH)2沉淀;
②向另一份溶液中滴加过量的AgNO3溶液,生成了2.87g沉淀。
结论:假设Ⅲ也不成立,若已知白色固体化学式为[Mgx(OH)y
【结论】经计算分析x:z=
请写出得到白色固体和H2的化学方程式(已知两者计量数比为1:2):
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐3】兴趣小组同学在做镁与盐反应的实验时,不小心将镁条加到饱和的碳酸氢钠溶液中,意外发现溶液中有白色不溶物生成。同学们对白色不溶物的成分产生了浓厚兴趣,于是在老师的帮助下进行了如下的探究。
【猜想与假设】
猜想①是Mg(OH)2
猜想②是MgCO3
猜想③是Mg(OH)2和MgCO3的混合物
【查阅资料】
①MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
②白色无水硫酸铜遇水变蓝。
③碱石灰是固体氢氧化钠和氧化钙的混合物。
【实验验证】取适量干燥的白色不溶物,充分加热,并使分解产生的气体依次通过如图1所示装置。
【实验现象】装置A中______ ,装置B中______ 。
【实验结论】猜想③正确。请写出Mg(OH)2受热分解的化学方程式______ 。
【拓展探究】直接向白色不溶物中滴加足量______ ,也能检验MgCO3的存在。
同学们为了进一步测定白色不溶物中各组分的质量关系,继续进行了下列探究;
称取干燥的白色不溶物36.8g,充分加热至不再产生气体,并使分解产生的气体全部被如图2所示装置C和D吸收。
【实验数据】实验后装置C增重3.6g,装置D增重13.2g。
【实验结论】若上述白色不溶物的组成用xMg(OH)2•yMgCO3表示,则x:y=______ 。
【反思评价】实验后,同学们经过讨论交流,发现实验方案可进一步优化,下列优化方案错误的是______ (填序号)。
①只称量装置C、D增重的质量,不称量白色不溶物的质量
②去掉装置D,只称量白色不溶物和装置C增重的质量
③去掉装置C,只称量白色不溶物和装置D增重的质量

【猜想与假设】
猜想①是Mg(OH)2
猜想②是MgCO3
猜想③是Mg(OH)2和MgCO3的混合物
【查阅资料】
①MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
②白色无水硫酸铜遇水变蓝。
③碱石灰是固体氢氧化钠和氧化钙的混合物。
【实验验证】取适量干燥的白色不溶物,充分加热,并使分解产生的气体依次通过如图1所示装置。
【实验现象】装置A中
【实验结论】猜想③正确。请写出Mg(OH)2受热分解的化学方程式
【拓展探究】直接向白色不溶物中滴加足量
同学们为了进一步测定白色不溶物中各组分的质量关系,继续进行了下列探究;
称取干燥的白色不溶物36.8g,充分加热至不再产生气体,并使分解产生的气体全部被如图2所示装置C和D吸收。
【实验数据】实验后装置C增重3.6g,装置D增重13.2g。
【实验结论】若上述白色不溶物的组成用xMg(OH)2•yMgCO3表示,则x:y=
【反思评价】实验后,同学们经过讨论交流,发现实验方案可进一步优化,下列优化方案错误的是
①只称量装置C、D增重的质量,不称量白色不溶物的质量
②去掉装置D,只称量白色不溶物和装置C增重的质量
③去掉装置C,只称量白色不溶物和装置D增重的质量
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】实验室里有一些同学们实验后剩余的白色固体,可能是碳酸钠、硫酸钠、碳酸钙、氢氧化钙、氢氧化钠中的一种或几种,化学兴趣小组想探究其成分。
【实验探究】化学兴趣小组同学取一定量白色粉末于烧杆中,加入足量水至固体完全溶解。小组同学认为白色固体中一定没有___ :此时有人提议,从离子的角度探究也可以得出正确的结论。
【提出问题】无色溶液中含有哪几种离子?
【展开探究】同学们分组后,各组分别进行了如图过程的实验;
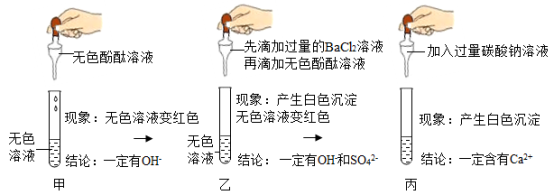
【评价交流】
甲组同学实验___ (填“能”或“不能”)得出正确结论;
丙组同学实验___ (填“能”或“不能”)得出正确结论;
丙组同学实验中一定发生反应的化学方程式___ ;
请评价乙组同学由实验现象得出的结论___ 。
【归纳与总结】通过上述实验探究过程,你认为在探究溶液中的溶质或离子成分时首先要注意排除___ 并且还要注意在探究过程中___ 。
【实验探究】化学兴趣小组同学取一定量白色粉末于烧杆中,加入足量水至固体完全溶解。小组同学认为白色固体中一定没有
【提出问题】无色溶液中含有哪几种离子?
【展开探究】同学们分组后,各组分别进行了如图过程的实验;

【评价交流】
甲组同学实验
丙组同学实验
丙组同学实验中一定发生反应的化学方程式
请评价乙组同学由实验现象得出的结论
【归纳与总结】通过上述实验探究过程,你认为在探究溶液中的溶质或离子成分时首先要注意排除
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某班同学用氢氧化钠溶液和稀硫酸进行中和反应实验。
(1)甲同学在烧杯中加入约5L氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈红色,接着用滴管滴入一定量的稀硫酸,再用玻璃棒搅拌,发现溶液变为无色,该反应的化学方程式为______ 。
(2)甲、乙、丙同学对反应后溶液中的溶质成分进行探究。
【提出问题】反应后溶液中的溶质是什么?
【猜想与假设】猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
以上猜想中,可以直接排除的是______ ,理由是______ 。
【实验探究】
为了验证另外两种猜想,甲,乙、丙同学分别设计如下实验方案:
老师认为甲同学方案不合理,你认为理由是______ 。
【反思交流】实验结束后,废液处理方法正确的是______ (填字母)。
A.倒入下水道 B.倒入废液缸 C.带出实验室
(1)甲同学在烧杯中加入约5L氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈红色,接着用滴管滴入一定量的稀硫酸,再用玻璃棒搅拌,发现溶液变为无色,该反应的化学方程式为
(2)甲、乙、丙同学对反应后溶液中的溶质成分进行探究。
【提出问题】反应后溶液中的溶质是什么?
【猜想与假设】猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
以上猜想中,可以直接排除的是
【实验探究】
为了验证另外两种猜想,甲,乙、丙同学分别设计如下实验方案:
实验操作 | 实验现象 | 实验结论 | |
甲同学方案 | 取少量反应后的溶液于试管中, 向试管中滴加BaCl2溶液 | 有白色沉淀产生 | 猜想二成立 |
乙同学方案 | 取少量反应后的溶液于试管中, 向试管中加入Na2CO3溶液 | 有气泡产生 | 猜想二成立 |
丙同学方案 | 取少量反应后的溶液于试管 中,向试管中加入铁锈 | 猜想二成立 |
老师认为甲同学方案不合理,你认为理由是
【反思交流】实验结束后,废液处理方法正确的是
A.倒入下水道 B.倒入废液缸 C.带出实验室
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】为了使同学们掌握酸根离子的检验方法,老师提供了一包白色固体,可能是碳酸钠、硫酸钠、氯化钠中的一种或几种。请你和同学们一起通过实验的方法探究白色固体的成分。
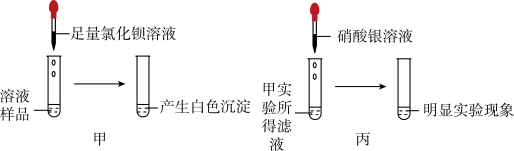
【提出问题】如何确定白色固体的成分?
【实验探究】甲同学取少量白色固体配成溶液,取溶液样品,实验如图所示,由此他得出实验结论:白色固体中一定含有硫酸钠。
【收集证据】他得出此结论的理由是_______________ (用化学方程式解释)。
【继续探究】乙同学取甲同学实验所得白色沉淀于试管中,向其中加入_________________ ,观察到白色固体表面冒气泡固体逐渐减少至消失,于是得出实验结论:原白色固体中一定含有__________ (填化学式,下同),一定不含___________ ,据此可知甲同学的实验结论不正确。白色固体中是否含有氯化钠呢?丙同学取甲同学实验所得滤液,向其中滴加的酸银溶察到明显的实验现象,于是得出实验结论:白色固体中含有氯化钠。请你评价丙同学的及结论_______________ 。
【反思与实践】经研究,同学们对实验进行了适当的调经和改进,最终确定了白色固体的成分是碳酸钠和氯化钠。
【归纳与总结】由上述探究可知:如果我们取一次样品先后鉴别几种物质,在鉴别第一种物质时,要注意所加试剂不能____________ (填一点)。

【提出问题】如何确定白色固体的成分?
【实验探究】甲同学取少量白色固体配成溶液,取溶液样品,实验如图所示,由此他得出实验结论:白色固体中一定含有硫酸钠。
【收集证据】他得出此结论的理由是
【继续探究】乙同学取甲同学实验所得白色沉淀于试管中,向其中加入
【反思与实践】经研究,同学们对实验进行了适当的调经和改进,最终确定了白色固体的成分是碳酸钠和氯化钠。
【归纳与总结】由上述探究可知:如果我们取一次样品先后鉴别几种物质,在鉴别第一种物质时,要注意所加试剂不能
您最近一年使用:0次



