为强化对水资源的保护,我省各地对主要河流建立了市级河长制。某研究实践小组在一次环保调查中,对一硫酸厂生产车间排放的废水进行了检测。取澄清废水样品100g,逐滴加入氯化钡溶液,生成沉淀与加入氯化钡溶液的质量关系如下图所示。(杂质不参与反应)___________ 。
(2)实验过程中生成硫酸钡的质量是___________ g。
(3)该车间产生的废水需经过处理才能向外排放,从经济和处理效果分析,下列物质中,最适合用于废水处理的是___________(填序号)。
(4)该车间排放的废水中所含硫酸的质量分数是多少?(写出计算过程)
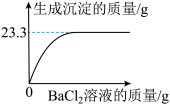
(2)实验过程中生成硫酸钡的质量是
(3)该车间产生的废水需经过处理才能向外排放,从经济和处理效果分析,下列物质中,最适合用于废水处理的是___________(填序号)。
| A.氢氧化钠 | B.氧化铜 | C.熟石灰 | D.食盐 |
(4)该车间排放的废水中所含硫酸的质量分数是多少?(写出计算过程)
2024·江西新余·一模 查看更多[1]
更新时间:2024-05-08 17:29:36
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸100g于烧杯中,逐滴滴加1.71%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如下图所示。___________ g。
(2)求该硫酸溶液的溶质质量分数

(2)求该硫酸溶液的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】钠元素在人体内可起到调节体液平衡、维持肌肉正常兴奋和细胞的通透性等作用。若缺乏,将导致肌肉痉挛、头痛等;若过量,将导致水肿、高血压、贫血等。假设钠元素全部来源于食盐(NaCl)。
(1)每位成人每天正常摄入食盐的质量约为5 g,试计算每人每天摄入的钠元素的质量。
(2)某病人因为食盐的摄入量不够,需静脉输入一定量的生理盐水(NaCl的质量分数为0.9%,密度约为1 g·mL-1)来补充食盐。医生给他确定每天应补充NaCl约2.7 g,问每天需输入生理盐水多少毫升?
(3)某卫生部门对市面上一批生理盐水进行质量分析,取这种生理盐水250 mL,加入足量的AgNO3溶液,充分反应最终得到14.35 g沉淀,试通过计算判断这批生理盐水是否符合医用标准。(提示:化学反应方程式为NaCl+AgNO3=NaNO3+AgCl↓)
(1)每位成人每天正常摄入食盐的质量约为5 g,试计算每人每天摄入的钠元素的质量。
(2)某病人因为食盐的摄入量不够,需静脉输入一定量的生理盐水(NaCl的质量分数为0.9%,密度约为1 g·mL-1)来补充食盐。医生给他确定每天应补充NaCl约2.7 g,问每天需输入生理盐水多少毫升?
(3)某卫生部门对市面上一批生理盐水进行质量分析,取这种生理盐水250 mL,加入足量的AgNO3溶液,充分反应最终得到14.35 g沉淀,试通过计算判断这批生理盐水是否符合医用标准。(提示:化学反应方程式为NaCl+AgNO3=NaNO3+AgCl↓)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】为测定某硫酸溶液的溶质质量分数,实验小组设计了以下方案:在烧杯中加入该硫酸溶液100 g,然后向烧杯中逐滴加入氢氧化钡溶液,滴加的氢氧化钡溶液质量与生成沉淀的质量关系如图所示。请你帮其解决下列问题:_____ g。
(2)求该硫酸溶液的溶质质量分数(写出计算过程)。

(2)求该硫酸溶液的溶质质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】向20g某赤铁矿石(主要成分是Fe2O3,假设杂质不溶于水,也不与酸反应)样品中,逐渐加入稀硫酸,充分反应。实验相关数据如图所示。

(1)20g赤铁矿石样品中氧化铁的质量为______g
(2)计算试验中所用稀硫酸溶质的质量分数(写出计算过程)

(1)20g赤铁矿石样品中氧化铁的质量为______g
(2)计算试验中所用稀硫酸溶质的质量分数(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某化验室用80g质量分数为20%的氢氧化钠溶液洗涤一定量工业废水中残余的 (工业废水中的其他杂质都不与氢氧化钠溶液反应),当恰好完全反应时,所得溶液总质量为276g,求此工业废水中硫酸的溶质质量分数。
(工业废水中的其他杂质都不与氢氧化钠溶液反应),当恰好完全反应时,所得溶液总质量为276g,求此工业废水中硫酸的溶质质量分数。
 (工业废水中的其他杂质都不与氢氧化钠溶液反应),当恰好完全反应时,所得溶液总质量为276g,求此工业废水中硫酸的溶质质量分数。
(工业废水中的其他杂质都不与氢氧化钠溶液反应),当恰好完全反应时,所得溶液总质量为276g,求此工业废水中硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某地新建一家硫酸厂,为检测其排出的中和处理前的废水中硫酸的质量分数,工厂技术科做了如下实验:取废水1000g,向其中不断投入熟石灰,用pH计测得溶液pH与所加入的熟石灰的质量关系如下图,计算:
(2)若该厂每天排出废水1000t,若完全中和,则每天应采购熟石灰_________ t。

(2)若该厂每天排出废水1000t,若完全中和,则每天应采购熟石灰
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】学习完“酸的性质”后,某化学兴趣小组的同学们到实验室中发现废液桶内有较多的废液,经询问后,确定是上节课同学们完成实验后,产生的酸性废液,这些废液需处理至中性后,才能排放。于是该小组的同学取100g含硫酸的废液样品,逐滴加入4%的氢氧化钠溶液,至废液呈中性,废液中硫酸的质量分数变化如右图所示。(假设废液中不含硫酸钠,且其他成分不与氢氧化钠反应)

(1)P点对应溶液能使紫色石蕊试液变成___________ 色。
(2)当废液处理至中性时,反应的氢氧化钠溶液中溶质的质量为___________ g。
(3)计算该废液中硫酸的质量分数。(写出计算过程)

(1)P点对应溶液能使紫色石蕊试液变成
(2)当废液处理至中性时,反应的氢氧化钠溶液中溶质的质量为
(3)计算该废液中硫酸的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某厂生产的食品级碳酸钾中混入了少量氯化钾,为测定该产品中碳酸钾的质量分数,进行以下实验:取15.0g碳酸钾样品放入烧杯中,称得烧杯及所盛样品的总质量为158.0g;再把120g稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下:
(1)实验______ (填编号)中稀盐酸是过量的。
(2)计算该产品中碳酸钾的质量分数。(写出计算过程)
(3)分析实验数据,在图中画出加入120g稀盐酸的过程中,溶液中氯化钾的质量变化图,并标注必要的数据。(数值精确到0.1)

| 实验编号 | ① | ② | ③ | ④ |
| 所加稀盐酸的质量/g | 30 | 60 | 90 | 120 |
| 烧杯及所盛物质总质量/g | 186.2 | 214.4 | 243.6 | 273.6 |
(2)计算该产品中碳酸钾的质量分数。(写出计算过程)
(3)分析实验数据,在图中画出加入120g稀盐酸的过程中,溶液中氯化钾的质量变化图,并标注必要的数据。(数值精确到0.1)

您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在农业生产中,常用15%~20%的氯化钠溶液选种,为了测定某氯化钠溶液是否符合要求,取该溶液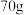 于烧杯中,再向其中逐滴的加入一定溶质质量分数的硝酸银溶液,充分搅拌,过滤、洗涤、干燥,得到白色沉淀,测得加入硝酸银溶液的质量与产生沉淀的质量关系如图所示,请回答:
于烧杯中,再向其中逐滴的加入一定溶质质量分数的硝酸银溶液,充分搅拌,过滤、洗涤、干燥,得到白色沉淀,测得加入硝酸银溶液的质量与产生沉淀的质量关系如图所示,请回答:_______ (填“有”或“无”)氯离子。
(2)通过计算确定该氯化钠溶液是否符合选种要求?(结果精确到0.1%)
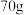 于烧杯中,再向其中逐滴的加入一定溶质质量分数的硝酸银溶液,充分搅拌,过滤、洗涤、干燥,得到白色沉淀,测得加入硝酸银溶液的质量与产生沉淀的质量关系如图所示,请回答:
于烧杯中,再向其中逐滴的加入一定溶质质量分数的硝酸银溶液,充分搅拌,过滤、洗涤、干燥,得到白色沉淀,测得加入硝酸银溶液的质量与产生沉淀的质量关系如图所示,请回答:
(2)通过计算确定该氯化钠溶液是否符合选种要求?(结果精确到0.1%)
您最近一年使用:0次





