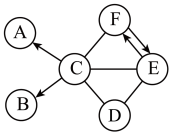
如图是初中化学几种常见物质之间的关系图。已知A、B、C、D、E是五种不同类别的物质,D、E、F的水溶液均呈碱性,C是胃酸的主要成分。________ 。
(2)请写出E→F的化学方程式________________ 。
(3)请写出物质D的一种用途________ 。
(2)请写出E→F的化学方程式
(3)请写出物质D的一种用途
更新时间:2024-04-29 07:10:12
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
真题
【推荐1】A~G表示初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去),其中A为金属氧化物,E、F为金属单质,且F为紫红色,化学反应②和③的基本反应类型相同。
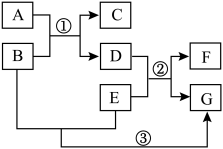
请按要求填空:
(1)物质C的化学式为___________________ 。
(2)写出反应②的一个化学方程式_______________________________________ 。
(3)反应③的基本反应类型是__________________________ 。
(4)E、F和氢由强到弱的金属活动性顺序为________________________________ 。

请按要求填空:
(1)物质C的化学式为
(2)写出反应②的一个化学方程式
(3)反应③的基本反应类型是
(4)E、F和氢由强到弱的金属活动性顺序为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】芯片的制造代表一个国家的科技水平,我国华为公司在5G及芯片的开发上正在努力开拓,其中5G技术领先全球2~3年。芯片的主要成分是高纯硅。如图是工业上以某种石英砂(主要成分:SiO2、Li2O、Fe2O3、Al2O3,其中SiO2质量分数为75%)为主要原料制取纯硅和金属锂的一种方法。请回答以下问题。
查阅资料知:
Ⅰ.LiCl的熔点是605℃、沸点是1350℃;
Ⅱ.NH4Cl在100℃开始分解,337.8℃分解完全,NH3和HCl在常温下又能反应生成NH4Cl固体;
Ⅲ.当溶液pH=5时,Fe3+和Al3+已沉淀完全。

(1)“酸浸”的稀盐酸要过量,其目的是_______ 。
(2)操作a的名称是_______ ,反应①属于_______ (填基本反应类型)反应。
(3)反应②除了生成Si外,还生成一种常见的化合物,该物质溶于水呈酸性,请写出反应②的化学方程式_______ ,该反应需要在无氧气环境中进行,原因是_______ (答出一种即可)。
(4)要得到较纯净的LiCl和NH4Cl固体,应加入试剂X调节溶液pH=5,使Fe3+和Al3+沉淀完全,则试剂X可以选择下面的(填字母)。
(5)已知石英砂的质量为10t,理论上可生成纯Si的质量为_______ t。
查阅资料知:
Ⅰ.LiCl的熔点是605℃、沸点是1350℃;
Ⅱ.NH4Cl在100℃开始分解,337.8℃分解完全,NH3和HCl在常温下又能反应生成NH4Cl固体;
Ⅲ.当溶液pH=5时,Fe3+和Al3+已沉淀完全。

(1)“酸浸”的稀盐酸要过量,其目的是
(2)操作a的名称是
(3)反应②除了生成Si外,还生成一种常见的化合物,该物质溶于水呈酸性,请写出反应②的化学方程式
(4)要得到较纯净的LiCl和NH4Cl固体,应加入试剂X调节溶液pH=5,使Fe3+和Al3+沉淀完全,则试剂X可以选择下面的(填字母)。
| A.NaOH | B.(NH4)2SO4 | C.NH3•H2O | D.K2CO3 |
(5)已知石英砂的质量为10t,理论上可生成纯Si的质量为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】垃圾分类回收,不仅可以避免污染环境,还可以充分利用资源。以普通锌锰电池的锌皮(主要成分是Zn和少量FeO)为原料制备纳米氧化锌,可用于催化材料、光化学半导体材料等。具体流程如图所示:___________ ,滤渣A的成分是___________ 。
(2)请写出浸出液与锌反应的化学方程式:___________ ,该反应属于___________ (填基本反应类型)反应。
(3)请写出Zn2(OH)2CO3分解的反应化学方程式:___________ 。
(4)酸浸过程中,要注意通风、严禁明火的原因是___________ 。
(5)写出滤液B的一种用途:___________ 。

(2)请写出浸出液与锌反应的化学方程式:
(3)请写出Zn2(OH)2CO3分解的反应化学方程式:
(4)酸浸过程中,要注意通风、严禁明火的原因是
(5)写出滤液B的一种用途:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐1】A~K为中学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,它们之间的转换关系如图所示。

(1)D的化学式_____ 。
(2)①的基本反应类型是_____ 。
(3)反应②的化学方程式是_____ 。
(4)气体E在该实验中体现的主要性质是_____ 性。

(1)D的化学式
(2)①的基本反应类型是
(3)反应②的化学方程式是
(4)气体E在该实验中体现的主要性质是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】氯化钡是一种可溶性重金属盐,广泛应用于化工领域。工业上以重晶石(主要成分BaSO4,杂质为Fe2O3)为原料,通过下列流程生成氯化钡晶体(BaCl2·xH2O)。
已知:①
②CaO、BaO都能与水反应生成碱
③钡离子是重金属离子,有毒
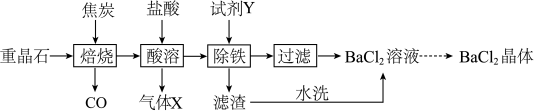
(1)焙烧时,焦炭与杂质Fe2O3发生反应的化学方程式为____________ ;
(2)气体X的成分除H2S和少量挥发出的HCl、水蒸气外,还含有____________ 。
(3)除铁反应中,试剂Y可以是___________ (填字母)
a NaOH溶液 b 氨水 c 生石灰 d BaO固体
证明铁已除尽的方法是:取上层清液于试管中,____________ 。
(4)对滤渣进行水洗的目的是提高晶体产率和____________ 。
已知:①

②CaO、BaO都能与水反应生成碱
③钡离子是重金属离子,有毒

(1)焙烧时,焦炭与杂质Fe2O3发生反应的化学方程式为
(2)气体X的成分除H2S和少量挥发出的HCl、水蒸气外,还含有
(3)除铁反应中,试剂Y可以是
a NaOH溶液 b 氨水 c 生石灰 d BaO固体
证明铁已除尽的方法是:取上层清液于试管中,
(4)对滤渣进行水洗的目的是提高晶体产率和
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐3】A-G均是初中化学常见的物质,如图所示是它们之间的转化关系(反应条件及部分反应物、生成物已略去)。其中B是石灰石的主要成分,E是人体胃液中帮助消化的成分,D、F、G均为气体。请回答下列问题:

(1)B的化学式是______ 。
(2)F→G在实际中的应用是______ 。
(3)E→D的基本反应类型是______ 。
(4)写出A→C反应的化学方程式______ 。

(1)B的化学式是
(2)F→G在实际中的应用是
(3)E→D的基本反应类型是
(4)写出A→C反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐1】某学习小组运用传感器探究钠与水的反应得到如下图像,其中图1是反应过程中溶液温度与时间的图像,图2是反应过程中溶液pH与时间的图像。

回答下列问题:
(1)钠与水的反应属于_________ 反应(填“吸热”或者“放热”)。
(2)结合图1分析,钠充分反应时对应的点是_________ 。
(3)钠与水反应能生成一种可燃性气体,请结合图2写出反应的化学方程式_________ 。
(4)将少量金属钠投入稀的硫酸镁溶液中,生成一种白色沉淀,写出该沉淀的化学式_________ 。

回答下列问题:
(1)钠与水的反应属于
(2)结合图1分析,钠充分反应时对应的点是
(3)钠与水反应能生成一种可燃性气体,请结合图2写出反应的化学方程式
(4)将少量金属钠投入稀的硫酸镁溶液中,生成一种白色沉淀,写出该沉淀的化学式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】某工厂生产硼砂产生的固体废料,主要含有MgCO3、CaCO3、SiO2、Al2O3和Fe2O3等,其中MgCO3质量分数为63%。回收镁的工艺流程如图:

(1)使用固体废料时首先要进行充分粉碎,目的是______ 。
(2)“酸浸”时MgCO3发生反应的化学方程式为______ 。
(3)“调pH”前滤液Ⅰ的pH______ 7(填“>”或“<”)。
(4)滤液Ⅲ中可回收的主要物质是______ (填化学式)。
(5)已知固体废料质量为m,理论上可生产Mg(OH)2的质量为______ 。

(1)使用固体废料时首先要进行充分粉碎,目的是
(2)“酸浸”时MgCO3发生反应的化学方程式为
(3)“调pH”前滤液Ⅰ的pH
(4)滤液Ⅲ中可回收的主要物质是
(5)已知固体废料质量为m,理论上可生产Mg(OH)2的质量为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐3】硝酸钙可用于无土栽培等。一种利用石灰石制备硝酸钙晶体的流程如下:

已知:硝酸会挥发、受热会分解。
(1)气体X为_______ (填化学式)。
(2)“制浆”所得的混合物属于_______ (填字母)。
a 溶液
b 悬浊液
c 乳浊液
(3)写出“中和”步骤主要反应的化学方程式:________ 。
(4)工业生产根据以下两项指标判断“中和”反应完全发生:容器内混合物基本变澄清和_____ 。
(5)“制浆”时须控制好加入水的量。加入水量太少会导致制浆困难;加入水量太多会导致_ 。
(6)若省去“制浆”步骤也可制得硝酸钙。但硝酸利用率会降低、同时会产生污染气体NOx。产生NOx的原因是______ 。

已知:硝酸会挥发、受热会分解。
(1)气体X为
(2)“制浆”所得的混合物属于
a 溶液
b 悬浊液
c 乳浊液
(3)写出“中和”步骤主要反应的化学方程式:
(4)工业生产根据以下两项指标判断“中和”反应完全发生:容器内混合物基本变澄清和
(5)“制浆”时须控制好加入水的量。加入水量太少会导致制浆困难;加入水量太多会导致
(6)若省去“制浆”步骤也可制得硝酸钙。但硝酸利用率会降低、同时会产生污染气体NOx。产生NOx的原因是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】已知某固体混合物A中可能含有BaCl2、Na2CO3、NH4Cl、CuO、NH4NO3五种物质中的两种或多种。按图所示进行实验,出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全进行)。

试根据实验过程和发生的现象做出判断,填写以下空白:
(1)在常温下,气体B水溶液pH_______ 7 (填“大于”“小于”“等于”之一)。
(2)滤液C中大量存在的阳离子为(写离子符号)_________________ 。
(3)溶液E中,最多有___________________ 种溶质。
(4)写出实验过程④中发生反应的化学方程式:_________________ 。
(5)混合物A中,肯定不存在的物质是(写化学式)_________________ ,理由是_____________________ 。

试根据实验过程和发生的现象做出判断,填写以下空白:
(1)在常温下,气体B水溶液pH
(2)滤液C中大量存在的阳离子为(写离子符号)
(3)溶液E中,最多有
(4)写出实验过程④中发生反应的化学方程式:
(5)混合物A中,肯定不存在的物质是(写化学式)
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3和不与酸反应的不溶性杂质)为原料制备高纯氧化镁的实验流程图如图1。
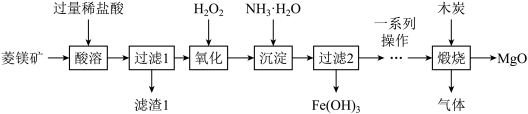
(1)酸溶时,需将菱镁矿磨成粉末状,目的是______ 。MgCO3与稀硫酸反应的化学方程式为______ 。
(2)氧化时,反应的方程式为2FeSO4+H2O2+______ ═Fe2(SO4)3+2H2O,KMnO4溶液也能将Fe2+氧化成Fe3+,并生成可溶性的锰盐,选择H2O2的优点是______ 。
(3)沉淀时,需严格控制NH3•H2O的用量,其目的是使Fe3+完全沉淀,______ (填离子符号)不沉淀。
(4)流程中“一系列操作”主要过程为:蒸发浓缩,______ ,过滤、洗涤、干燥等。

(1)酸溶时,需将菱镁矿磨成粉末状,目的是
(2)氧化时,反应的方程式为2FeSO4+H2O2+
(3)沉淀时,需严格控制NH3•H2O的用量,其目的是使Fe3+完全沉淀,
(4)流程中“一系列操作”主要过程为:蒸发浓缩,
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐3】已知A~E为初中化学常见的5种不同类别的物质,A俗称苛性钠,C是最轻的气体,它们的部分反应和转化关系如图所示(“—”表示两种物质能发生反应,“→”表示一种物质能直接转化成另一种物质,部分反应物、生成物及反应条件已省路)。

请回答下列问题:
(1)D的化学式是__________ ,A的用途是__________ (写一种)。
(2)A—B反应的微观实质是__________ 。
(3)B—E反应的化学方程式是__________ ,该反应的现象是__________ 。
(4)E—C反应所属的基本反应类型是__________ 。

请回答下列问题:
(1)D的化学式是
(2)A—B反应的微观实质是
(3)B—E反应的化学方程式是
(4)E—C反应所属的基本反应类型是
您最近一年使用:0次



