高纯氧化镁可用于制药。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的流程如下: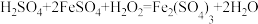
(1)FeCO3中铁元素的化合价为______ ,MgCO3与稀硫酸反应的化学方程式为______ 。
(2)“酸溶”步骤中加入过量的硫酸的目的是______ 。
(3)滤渣2的成分是______ 。
(4)补充完整“…”部分的实验操作:向滤液中______ ,洗涤、干燥,将得到的碳酸镁煅烧得到氧化镁。
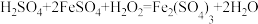
(1)FeCO3中铁元素的化合价为
(2)“酸溶”步骤中加入过量的硫酸的目的是
(3)滤渣2的成分是
(4)补充完整“…”部分的实验操作:向滤液中
2024·江苏无锡·一模 查看更多[3]
江苏省无锡市锡山区2024年中考一模考试理科综合题-初中化学(已下线)专题12 工业流程-【好题汇编】2024年中考化学一模试题分类汇编(江苏专用)(已下线)押无锡卷第26题 非选择题-备战2024年中考化学临考题号押题(无锡专用)
更新时间:2024-05-08 13:40:03
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】小明在学完初中化学知识后,把常见八种化合物(酸、碱、盐、氧化物)的相互关系连接成如图所示。已知A是最常见的一种溶剂、也是人体中含量最多的物质,E是胃酸的主要成分;F、G、H三种物质的类别相同。(“→”表示一种物质可以通过一步反应转化为另一种物质,“一”表示相连的两种物质之间可以发生反应。反应条件、部分反应物和生成物已略去。)

(1)写出物质的化学式:A___________ ,D___________ 。
(2)请写出E和H反应的化学方程式___________ 。
(3)B→C属于___________ 反应。

(1)写出物质的化学式:A
(2)请写出E和H反应的化学方程式
(3)B→C属于
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】已知A~E是初中化学常见的物质,且都含有一种相同的元素,A、C、D所属物质类别相同:“A-B”的反应可用于工业除铁锈;它们相互间的关系如下图所示。
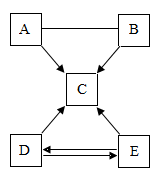
(“一”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系)
(1)若E为单质,通过动植物呼吸作用可实现E→D的转化,则E的化学式是________ ;通过绿色植物的________ 作用,可实现D→E的转化。
(2)写出A与B反应的化学方程式________ 。
(3)者B和E属于同一类物质,则C的化学式是:________ 。在转化为C的四个反应中,不涉及到的基本反应类型是________ 。

(“一”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系)
(1)若E为单质,通过动植物呼吸作用可实现E→D的转化,则E的化学式是
(2)写出A与B反应的化学方程式
(3)者B和E属于同一类物质,则C的化学式是:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】绿矾(FeSO4·7H2O)是一种重要的食品添加剂。某工厂产生的炉渣主要含有FeO和Fe2O3,还有一定量的SiO2(SiO2不溶于水、不与稀硫酸反应)。实验室以此炉渣制备绿矾的流程如下:

(1)步骤①实验时需用到的玻璃仪器是___________ 、玻璃棒和烧杯。该过程发生反应的化学方程式为:①FeO+H2SO4=FeSO4+H2O,②__________________ 。
(2)滤液A中含有的溶质有FeSO4、_______________ 。
(3)加入试剂X的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2(SO4)3+2H2O=2FeSO4+2Y,则Y的化学式是__________ 。
②若试剂X是Fe,转化原理为Fe+ Fe2(SO4)3=3FeSO4。测得反应后溶液的pH明显增大,其原因是__________________ 。
(4)步骤③的操作是蒸发浓缩、___________ 、过滤,即得到绿矾晶体。

(1)步骤①实验时需用到的玻璃仪器是
(2)滤液A中含有的溶质有FeSO4、
(3)加入试剂X的目的是将Fe3+转化为Fe2+,试剂X可用SO2或Fe。
①若试剂X是SO2,转化原理为SO2+Fe2(SO4)3+2H2O=2FeSO4+2Y,则Y的化学式是
②若试剂X是Fe,转化原理为Fe+ Fe2(SO4)3=3FeSO4。测得反应后溶液的pH明显增大,其原因是
(4)步骤③的操作是蒸发浓缩、
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】电缆生产过程中产生了一定量的含铜废料。化学兴趣小组利用稀硫酸和铁粉分离回收铜,并获得硫酸亚铁晶体。先将含铜废料粉碎,再按如下设计方案处理:

查阅资料得知:
①在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜。反应的化学方程式:2Cu +2H2SO4 +O2 2CuSO4 +2H2O。
2CuSO4 +2H2O。
②硫酸亚铁晶体的溶解度随着温度升高而增大(在一定温度范围内)。
(1)写出铁与硫酸铜溶液反应的化学方程式_____________ ;
(2)蓝色溶液A中溶质的成分是____________ (填化学式);
(3)该方案中应该加入略过量的铁粉,过量的目的是_________ ;从固体C中获得纯净的铜,操作(Ⅱ)的具体处理方法是__________ ;
(4)浅绿色溶液B经一系列操作[操作(Ⅰ)]可得硫酸亚铁晶体(FeSO4·7H2O),该系列操作的顺序为___________ (用编号a、b、c表示)→洗涤→干燥。
a.冷却结晶 b.过滤 c.加热浓缩

查阅资料得知:
①在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜。反应的化学方程式:2Cu +2H2SO4 +O2
 2CuSO4 +2H2O。
2CuSO4 +2H2O。②硫酸亚铁晶体的溶解度随着温度升高而增大(在一定温度范围内)。
(1)写出铁与硫酸铜溶液反应的化学方程式
(2)蓝色溶液A中溶质的成分是
(3)该方案中应该加入略过量的铁粉,过量的目的是
(4)浅绿色溶液B经一系列操作[操作(Ⅰ)]可得硫酸亚铁晶体(FeSO4·7H2O),该系列操作的顺序为
a.冷却结晶 b.过滤 c.加热浓缩
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】硫酸铁铵NH4Fe(SO4)2·xH2O是一种重要的化合物,常用于物质检测的指示剂。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下,回答下列问题:

(1)硫酸铁铵属于______ (填“酸”、“碱”、“盐”),其中铁元素的化合价是_______ 。
(2)步骤①的目的是除去废铁屑表面的油污,可选择的试剂有______。
(3)步骤②中发生的反应化学方程式为_______ 。该反应加热的目的是_______ 。温度欲保持在80~90℃,采用的合适加热方式是_______ 。
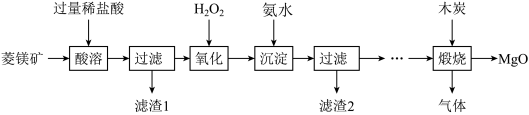
(4)步骤③中的反应为2FeSO4+X+H2O2=Fe2(SO4)3+2H2O(放热),X的化学式为______ 。反应过程中要分批加入H2O2溶液,原因是_______ 。
(5)步骤⑤的具体实验操作有:_____ 、降温结晶、过滤、洗涤、干燥得到硫酸铁铵晶体样品。

(1)硫酸铁铵属于
(2)步骤①的目的是除去废铁屑表面的油污,可选择的试剂有______。
| A.稀盐酸 | B.纯碱溶液 | C.氢氧化钠溶液 |
(4)步骤③中的反应为2FeSO4+X+H2O2=Fe2(SO4)3+2H2O(放热),X的化学式为
(5)步骤⑤的具体实验操作有:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】氯化钾样品中含有少量氯化钙、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作(注意事项:①所加试剂必须过量;②过量试剂必须除去;③不能引入新的杂质)。
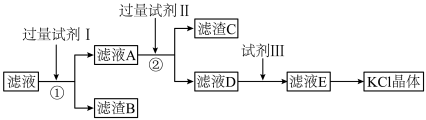
(1)写出滤渣B的化学式______ 。
(2)②中所加试剂II是______ (填化学式),滤渣C中有_______ 种固体;
(3)滤液E中除K+和Cl-外,还含有的离子是______ (填离子符号);
(4)由所得KC1溶液制成氯化钾晶体的操作_____ 。
(5)如果称得加入的样品质量为3g,实验得到的氯化钾晶体质量为3.1g,则下列分析不正确的是______(填字母)。

(1)写出滤渣B的化学式
(2)②中所加试剂II是
(3)滤液E中除K+和Cl-外,还含有的离子是
(4)由所得KC1溶液制成氯化钾晶体的操作
(5)如果称得加入的样品质量为3g,实验得到的氯化钾晶体质量为3.1g,则下列分析不正确的是______(填字母)。
| A.蒸发过程中可能有水分没有蒸干 |
| B.溶解操作中氯化钾没有完全溶解 |
| C.除杂过程中有氯化钾生成 |
您最近一年使用:0次



