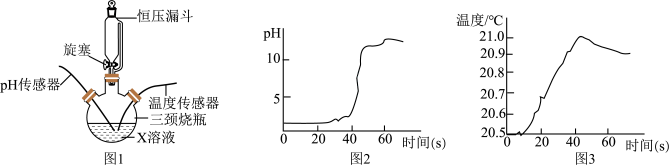
实验小组对稀NaOH溶液与稀盐酸的反应进行研究。实验装置见图1。用恒压漏斗匀速滴加某溶液,过程中,溶液pH和温度随时间的变化分别见图2和图3。______ ,恒压漏斗能匀速滴加溶液的原因是______ 。
(2)溶液X是______ ,40s时溶液中质量分数最高的溶质是______ 。
(3)盐酸和氢氧化钠反应的化学反应方程式为______ ,反应过程中溶液温度先升高后下降的原因是______ 。
(2)溶液X是
(3)盐酸和氢氧化钠反应的化学反应方程式为
更新时间:2024-05-09 10:48:16
|
相似题推荐
实验题
|
适中
(0.65)
【推荐1】如图所示,在6支试管中分别滴加2滴紫色石蕊溶液。
(资料:KCl溶液、CaCl2溶液均显中性)

(1)作为对照试验的是试管_____ (选填①~⑥编号)。
(2)试管②、⑤溶液变为红色,其原因是溶液中溶质都含有_____ 元素。
(3)试管⑥中溶液变为蓝色,说明碳酸钾溶液显_____ (选填“酸性”、“中性”或“碱性”)。碳酸钾属于 _____ (填物质类别),可做 _____ 肥使用,取该溶液灼烧,透过蓝色钴玻璃火焰呈 _____ 色。
(4)将试管⑤倒入试管④中,写出该反应的化学方程式_____ 。充分反应后溶液呈现 _____ 。
A 红色 B 紫色 C 蓝色
(5)实验后将试管①②⑥中的废液倒入大烧杯中,最终得到红色溶液,则大烧杯的废液中除了石蕊外,一定还含有_____ 。
(资料:KCl溶液、CaCl2溶液均显中性)

(1)作为对照试验的是试管
(2)试管②、⑤溶液变为红色,其原因是溶液中溶质都含有
(3)试管⑥中溶液变为蓝色,说明碳酸钾溶液显
(4)将试管⑤倒入试管④中,写出该反应的化学方程式
A 红色 B 紫色 C 蓝色
(5)实验后将试管①②⑥中的废液倒入大烧杯中,最终得到红色溶液,则大烧杯的废液中除了石蕊外,一定还含有
您最近一年使用:0次
【推荐2】酸碱中和反应是初中阶段重要的一类反应,请你参与一起探究。
【实验1】从能量变化角度探究酸和碱的反应
某小组同学测量盐酸与氢氧化钠溶液反应过程中温度的变化,观察到溶液温度升高,因此,得出两者能反应的结论。有同学认为此结论不够严谨,在密闭隔热容器中设计了以下实验:
①10mL一定浓度的盐酸与10mL蒸馏水混合,测量溶液温度的变化。
②10mL一定浓度的氢氧化钠溶液与10mL蒸馏水混合,测量溶液温度的变化。
③10mL一定浓度的盐酸与10mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
用数字化实验技术测得3个实验中溶液温度随时间变化的关系如图1所示。
(1)由图1可知,盐酸、氢氧化钠溶液稀释时均______ (填“放热”或“吸热”),但它们稀释时温度的变化量远______ (填“大于”或“小于”)两溶液混合时温度的变化量,由此说明氢氧化钠和盐酸发生了反应。
(2)从微观角度分析,此中和反应的温度变化主要是由于______ (填离子符号),两种离子反应放出热量的缘故,由此说明氢氧化钠和盐酸发生了中和反应。
(3)在10mL溶质质量分数为10%的NaOH溶液(密度为1.1g/mL)中加入溶质质量分数为5%的盐酸(密度为1.0g/mL)溶液的体积为______ mL,就能使反应后溶液的pH等于7。(结果保留整数)
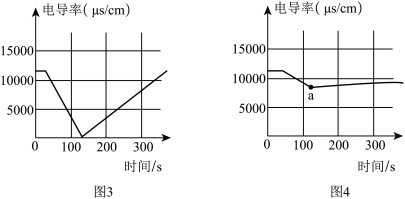
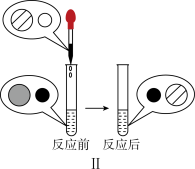
小组同学根据图2进行相应实验操作,利用电导率传感器分别测定A试管和B试管反应过程中溶液的电导率变化,结果如图3和图4,电导率的大小能反映离子浓度的大小。
(4)根据图3所示电导率变化,请写出对应试管中发生反应的化学方程式为______ 。基本反应类型为______ 。
(5)图4中电导率的变化______ (填“能”或“不能”)说明酸和碱发生了反应,a点所示溶液中含有的溶质是______ (填化学符号)。
【实验1】从能量变化角度探究酸和碱的反应
某小组同学测量盐酸与氢氧化钠溶液反应过程中温度的变化,观察到溶液温度升高,因此,得出两者能反应的结论。有同学认为此结论不够严谨,在密闭隔热容器中设计了以下实验:
①10mL一定浓度的盐酸与10mL蒸馏水混合,测量溶液温度的变化。
②10mL一定浓度的氢氧化钠溶液与10mL蒸馏水混合,测量溶液温度的变化。
③10mL一定浓度的盐酸与10mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
用数字化实验技术测得3个实验中溶液温度随时间变化的关系如图1所示。
(1)由图1可知,盐酸、氢氧化钠溶液稀释时均
(2)从微观角度分析,此中和反应的温度变化主要是由于
(3)在10mL溶质质量分数为10%的NaOH溶液(密度为1.1g/mL)中加入溶质质量分数为5%的盐酸(密度为1.0g/mL)溶液的体积为


小组同学根据图2进行相应实验操作,利用电导率传感器分别测定A试管和B试管反应过程中溶液的电导率变化,结果如图3和图4,电导率的大小能反映离子浓度的大小。
(4)根据图3所示电导率变化,请写出对应试管中发生反应的化学方程式为
(5)图4中电导率的变化
您最近一年使用:0次
【推荐1】具备基本的化学实验技能是学习化学的基础和保证。在化学实验操作考试中,小明和小英分别抽取了Ⅰ、Ⅱ两组试题。可供选择的实验药品:大理石、KClO3、MnO2、稀盐酸、NaOH溶液、H2O2溶液、酚酞溶液、石蕊溶液等。
相关实验装置如图所示。
(1)仪器a的名称是______ 。
(2)小明想用同一套装置分别制取O2和CO2,应选用制取装置为______ ,其中,制取CO2的化学方程式为______ 。
Ⅱ组:溶液酸碱性的检验和酸碱的化学性质
(3)为了鉴别稀盐酸和NaOH溶液,小英使用pH试纸测得pH=1的溶液是______ 。
(4)稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加______ 溶液,再逐滴加入稀盐酸至过量,观察到溶液由红色变为无色。
相关实验装置如图所示。

(1)仪器a的名称是
(2)小明想用同一套装置分别制取O2和CO2,应选用制取装置为
Ⅱ组:溶液酸碱性的检验和酸碱的化学性质
(3)为了鉴别稀盐酸和NaOH溶液,小英使用pH试纸测得pH=1的溶液是
(4)稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】某化学兴趣小组的同学对实验室制取CO2及相关性质进行一系列的探究活动。
(1)气体制取。
按如图1所示的制取装置进行实验。
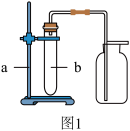
①写出有标号仪器的名称:a__________ ,b ___________ 。
②实验室制取CO2的反应化学方程式是______________________________ 。
③实验室收集CO2的方法是________________________________________ ,
原因是_____________________________________________ 。
(2)实验探究。
[提出问题] 实验室制取CO2时能否采用排水法收集?
[设计实验]
实验一:向一个充满CO2气体的质地较软的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,用力摇晃塑料瓶。可观察到塑料瓶________________________ ,说明CO2能溶于水。
实验二:先用集气瓶装满一瓶蒸馏水(pH=7.0),然后按如图2所示组装装置并进行实验,再用pH计测定从装置C排到烧杯中的液体的pH。

测得烧杯中液体的pH<7.0,说明溶液呈酸性,原因是_____________________ 。
[实验结论] 实验室制取CO2不宜采用排水法收集。
[拓展延伸] 某同学先对图2装置做了以下改进:将装置C中的部分蒸馏水换成植物油,将烧杯换成量筒(如图3所示)。然后利用改进后的装置测定收集到CO2的体积,测得气体的实际体积小于理论值,原因可能是:①__________ ,② ___________ 。

(1)气体制取。
按如图1所示的制取装置进行实验。

①写出有标号仪器的名称:a
②实验室制取CO2的反应化学方程式是
③实验室收集CO2的方法是
原因是
(2)实验探究。
[提出问题] 实验室制取CO2时能否采用排水法收集?
[设计实验]
实验一:向一个充满CO2气体的质地较软的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,用力摇晃塑料瓶。可观察到塑料瓶
实验二:先用集气瓶装满一瓶蒸馏水(pH=7.0),然后按如图2所示组装装置并进行实验,再用pH计测定从装置C排到烧杯中的液体的pH。

测得烧杯中液体的pH<7.0,说明溶液呈酸性,原因是
[实验结论] 实验室制取CO2不宜采用排水法收集。
[拓展延伸] 某同学先对图2装置做了以下改进:将装置C中的部分蒸馏水换成植物油,将烧杯换成量筒(如图3所示)。然后利用改进后的装置测定收集到CO2的体积,测得气体的实际体积小于理论值,原因可能是:①

您最近一年使用:0次


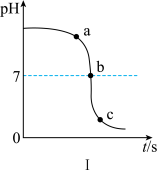
 表示的离子是
表示的离子是

