铜、铁等金属的冶炼和利用大大促进了人类文明的进步。
I.铜、铁的冶炼
(1)古代火法炼制的原理可用下列实验模拟。
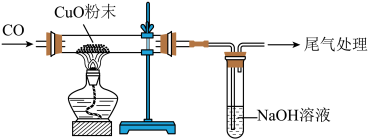
①管中出现红色固体时,发生反应的化学方程式为______ 。
②尾气处理的目的是______ 。
③经分析,实验得到的Cu中还含有少量CuO和Cu2O,三种物质中铜元素的质量比为7:1:2,则混合物中铜元素的质量分数为______ (精确到0.1%)。
(2)西汉时期发明了湿法炼铜,推动了社会生产力发展。
①湿法炼铜的原理为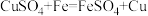 ,该反应能发生的原因是
,该反应能发生的原因是______ 。
②湿法炼铜需要铁。西汉时采用竖炉炼铁,原理与现代高炉炼铁相同。得到的铁中含有碳的原因是______ 。
Ⅱ.铜、铁的使用
(3)古代通常将铜和锡按照一定比例熔化制备青铜。与纯铜相比,加入锡改善了铜的性能,具体表现在______ 。
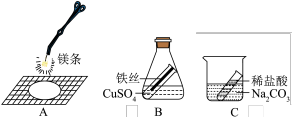
(4)实验小组通过下列实验探究影响钢铁腐蚀的因素。实验如图1、图2表示。______ 。
②实验中腐蚀速率较快的是______ 号锥形瓶中的样品。
③通过本实验你认为提高钢铁的抗腐蚀能力的方法是______ 。
I.铜、铁的冶炼
(1)古代火法炼制的原理可用下列实验模拟。

①管中出现红色固体时,发生反应的化学方程式为
②尾气处理的目的是
③经分析,实验得到的Cu中还含有少量CuO和Cu2O,三种物质中铜元素的质量比为7:1:2,则混合物中铜元素的质量分数为
(2)西汉时期发明了湿法炼铜,推动了社会生产力发展。
①湿法炼铜的原理为
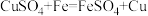 ,该反应能发生的原因是
,该反应能发生的原因是②湿法炼铜需要铁。西汉时采用竖炉炼铁,原理与现代高炉炼铁相同。得到的铁中含有碳的原因是
Ⅱ.铜、铁的使用
(3)古代通常将铜和锡按照一定比例熔化制备青铜。与纯铜相比,加入锡改善了铜的性能,具体表现在
(4)实验小组通过下列实验探究影响钢铁腐蚀的因素。实验如图1、图2表示。
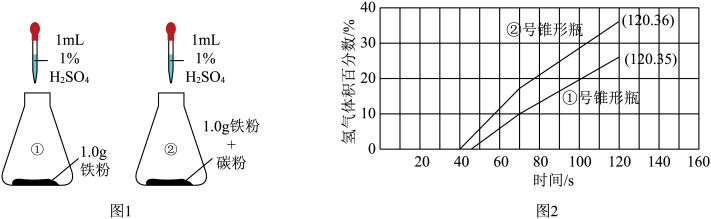
②实验中腐蚀速率较快的是
③通过本实验你认为提高钢铁的抗腐蚀能力的方法是
2024·江苏无锡·一模 查看更多[2]
更新时间:2024-05-08 13:40:03
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
【推荐1】通过一年的学习,你能运用简单的装置和方法制取某些气体。如图是初中化学常见气体的发生、收集装置,请你回答有关问题:

(1)写出图中①的仪器名称:______ 。
(2)实验室用石灰石和稀盐酸反应制取二氧化碳时,应选用的发生装置是______ (填字母);写出该反应的化学方程式:______ 。
(3)加热高锰酸钾制取氧气,用E装置收集氧气的适宜时间是______ (选序号)。
A当导管口刚有气泡冒出时 B当导管口有连续、均匀气泡冒出时
(4)我省有着丰富的天然气资源,许多化肥厂用天然气在高温、催化剂作用下与水蒸气反应来制备氢气和一氧化碳: 。为了证实该反应所生成的混合气体的成分,兴趣小组的同学设计了如图所示装置并进行实验,请你回答下列相关问题:
。为了证实该反应所生成的混合气体的成分,兴趣小组的同学设计了如图所示装置并进行实验,请你回答下列相关问题:
【实验目的】证实混合气体中含有CO和H2
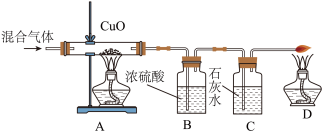
【进行实验】在装置中通入混合气体,点燃酒精灯,如上图所示进行实验。
【实验分析】①若要证实混合气体中有CO,应该观察到A处的现象是______ ,C中相关的化学反应方程式是______ 。
②若要证实混合气体中有H2,且是通过装置B验证的,应采用的方法是______ 。
③有同学认为,根据该混合气体生产的实际情况,混合气体中可能含有水分,因而还应对上述实验装置加以改进。请你提出改进的方案:______ 。

(1)写出图中①的仪器名称:
(2)实验室用石灰石和稀盐酸反应制取二氧化碳时,应选用的发生装置是
(3)加热高锰酸钾制取氧气,用E装置收集氧气的适宜时间是
A当导管口刚有气泡冒出时 B当导管口有连续、均匀气泡冒出时
(4)我省有着丰富的天然气资源,许多化肥厂用天然气在高温、催化剂作用下与水蒸气反应来制备氢气和一氧化碳:
 。为了证实该反应所生成的混合气体的成分,兴趣小组的同学设计了如图所示装置并进行实验,请你回答下列相关问题:
。为了证实该反应所生成的混合气体的成分,兴趣小组的同学设计了如图所示装置并进行实验,请你回答下列相关问题:【实验目的】证实混合气体中含有CO和H2

【进行实验】在装置中通入混合气体,点燃酒精灯,如上图所示进行实验。
【实验分析】①若要证实混合气体中有CO,应该观察到A处的现象是
②若要证实混合气体中有H2,且是通过装置B验证的,应采用的方法是
③有同学认为,根据该混合气体生产的实际情况,混合气体中可能含有水分,因而还应对上述实验装置加以改进。请你提出改进的方案:
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,再用一氧化碳还原氧化铜粉末的实验装置如图所示。

【资料查询】甲酸和浓硫酸混合制备CO的方程式为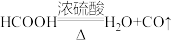 。
。
(1)仪器①的名称是______ 。
(2)装置A和装置B中浓硫酸的作用______ (填“相同”或“不同”),浓硫酸中的溶质是______ 。(填化学式)
(3)装置C中观察到的实验现象是______ 。
(4)装置D中发生反应的化学方程式为______ 。
(5)装置E______ (填“能”或“不能”)用来检验装置D吸收二氧化碳是否完全,理由是______ 。
(6)装置F和G是对实验中尾气的处理,导管接口的顺序为a→______ →______ →e。

【资料查询】甲酸和浓硫酸混合制备CO的方程式为
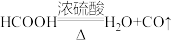 。
。(1)仪器①的名称是
(2)装置A和装置B中浓硫酸的作用
(3)装置C中观察到的实验现象是
(4)装置D中发生反应的化学方程式为
(5)装置E
(6)装置F和G是对实验中尾气的处理,导管接口的顺序为a→
您最近一年使用:0次
【推荐3】实验室中常见的气体制取和收集装置如图所示,请据图回答下列问题。
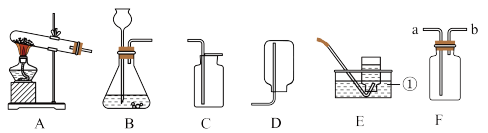
(1)仪器①的名称是________ 。
(2)实验室用高锰酸钾制取氧气的化学方程式为:________ 。若要收集较纯净的氧气,应选择的收集装置是________ (填序号)。
(3)若用装置F收集二氧化碳,气体应从________ (填“a”或“b”)端通入。
(4)为探究碳及其氧化物的某些性质,兴趣小组用如图所示的装置进行实验。先通入干燥的二氧化碳一段时间,然后点燃装置A处的酒精喷灯和装置C、D处的酒精灯。
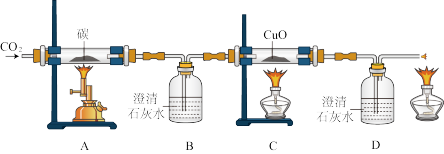
①装置C中玻璃管内的现象是________ 。
②装置B、D的作用是否相同?________ ,理由是________ 。

(1)仪器①的名称是
(2)实验室用高锰酸钾制取氧气的化学方程式为:
(3)若用装置F收集二氧化碳,气体应从
(4)为探究碳及其氧化物的某些性质,兴趣小组用如图所示的装置进行实验。先通入干燥的二氧化碳一段时间,然后点燃装置A处的酒精喷灯和装置C、D处的酒精灯。

①装置C中玻璃管内的现象是
②装置B、D的作用是否相同?
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】金属材料在生产、生活中有着广泛的应用。
(1)地壳中含量最高的金属元素是_____ 。(填化学式)
(2)铁生锈的条件是_____ ,为了防止自行车的支架生锈,常采用的方法是_____ 。
(3)某兴趣小组欲探究Fe、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行了如下实验。

①如图1所示,将四根金属丝同时插入烧杯中。甲中可观察到的现象是铁丝表面产生_____ ,溶液由无色变为浅绿色。乙中发生反应的化学方程式是____
②一段时间后,将烧杯中铁丝替换为R进行实验,如图2所示。若甲中出现气泡,乙中无明显现象,则烧杯乙中的溶质是_____ ,可得出Fe、Cu、Ag、R的活动性顺序由强到弱为____ 。
(1)地壳中含量最高的金属元素是
(2)铁生锈的条件是
(3)某兴趣小组欲探究Fe、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行了如下实验。

①如图1所示,将四根金属丝同时插入烧杯中。甲中可观察到的现象是铁丝表面产生
②一段时间后,将烧杯中铁丝替换为R进行实验,如图2所示。若甲中出现气泡,乙中无明显现象,则烧杯乙中的溶质是
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐2】验证金属Cu、Mg、Zn和Ag活动性顺序的四个实验如图,请根据实验回答下列问题。

(1)上述四个实验,没有必要做的是实验______ (选填“一”、“二”、“三”、“四”或其组合)。
(2)根据上述实验,得出四种金属活动性由强到弱的顺序是______ 。
(3)实验结束后,将四个试管中的所有物质倒入同一个烧杯内,充分反应后过滤,得到无色滤液和滤渣。在滤渣中加入稀盐酸无气泡产生,则滤渣中的成分是______ 。

(1)上述四个实验,没有必要做的是实验
(2)根据上述实验,得出四种金属活动性由强到弱的顺序是
(3)实验结束后,将四个试管中的所有物质倒入同一个烧杯内,充分反应后过滤,得到无色滤液和滤渣。在滤渣中加入稀盐酸无气泡产生,则滤渣中的成分是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐1】某化学兴趣小组设计了一组“吹气球”实验,三套装置如下图:
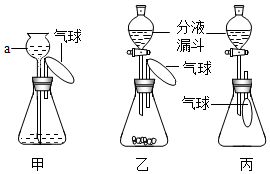
(1)甲装置:根据所学知识知
①仪器a的名称为________________ 。
②向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性___________ 。
(2)乙装置:①若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是__________________ 。
②若生成H2使气球胀大,则反应的化学方程式为___________________________ 。
③若锥形瓶中装有NaOH固体,分液漏斗中加入少量水,则气球胀大的主要原因是________________ 。
(3)丙装置:若锥形瓶中盛满CO2,欲使气球胀大,则分液漏斗中的液体可以是_____________ 。此过程中发生反应的化学方程式为 _____________________________________________ 。

(1)甲装置:根据所学知识知
①仪器a的名称为
②向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性
(2)乙装置:①若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是
②若生成H2使气球胀大,则反应的化学方程式为
③若锥形瓶中装有NaOH固体,分液漏斗中加入少量水,则气球胀大的主要原因是
(3)丙装置:若锥形瓶中盛满CO2,欲使气球胀大,则分液漏斗中的液体可以是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】用如图装置制取氢气,在多孔塑料板上放锌粒,稀硫酸由长颈漏斗加入。若打开弹簧夹,酸液由长颈漏斗中流下与锌粒接触即发生反应,产生的氢气由支管导出,试回答下列问题。

(1)发生反应的化学方程式为_____ 。
(2)检查此装置的气密性时,关闭弹簧夹,从长颈漏斗注入适量的水形成液封后,若看到长颈漏斗内_____ ,则表明装置气密性良好。
(3)反应过程中关闭弹簧夹,容器内继续反应产生的氢气会使容器内_____ ,将酸液压回长颈漏斗中,使酸液与锌粒_____ ,反应即自行停止。
(4)点燃氢气之前,要先检验_____ 。
(5)若在多孔塑料板上放一小块大理石,长颈漏斗中加入稀盐酸,_____ (填“能”或“不能”)用弹簧夹控制CO2的产生和停止。

(1)发生反应的化学方程式为
(2)检查此装置的气密性时,关闭弹簧夹,从长颈漏斗注入适量的水形成液封后,若看到长颈漏斗内
(3)反应过程中关闭弹簧夹,容器内继续反应产生的氢气会使容器内
(4)点燃氢气之前,要先检验
(5)若在多孔塑料板上放一小块大理石,长颈漏斗中加入稀盐酸,
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组进行铁锈蚀的实验探究。
【知识回顾】
铁是一种化学性质较活泼的金属,常温下能与稀盐酸、氧气等物质反应。
(1)铁与稀盐酸反应的化学方程式是___________ 。
(2)铁锈的颜色是___________ 。
【实验探究】
该小组利用如下装置对铁钉锈蚀的条件进行探究、一段时间后,在A和B中没有观察到明显现象,C和D中铁钉有锈蚀。___________ 。
(4)ABD对比,说明铁钉锈蚀需要的物质是___________ ;C中的铁钉比D中的锈蚀更严重,原因是___________ 。
【知识回顾】
铁是一种化学性质较活泼的金属,常温下能与稀盐酸、氧气等物质反应。
(1)铁与稀盐酸反应的化学方程式是
(2)铁锈的颜色是
【实验探究】
该小组利用如下装置对铁钉锈蚀的条件进行探究、一段时间后,在A和B中没有观察到明显现象,C和D中铁钉有锈蚀。

(4)ABD对比,说明铁钉锈蚀需要的物质是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】某同学为探究“氧化铜和铜粉”混合物中氧化铜的质量分数,实验过程如下:先称取一定质量样品,按如图实验装置进行实验(试剂均足量,部分夹持装置已省略,组合装置气密性良好)。回答下列问题:已知:碱石灰能吸收二氧化碳和水蒸气。

(1)装置A中发生反应的化学方程式为______ 。
(2)为保证实验结果的准确性和安全性,开始加热前应排尽管内空气,则弹簧夹K1、K2应如何控制?具体操作是______ 。
(3)装置D的作用是______ 。
(4)实验结束后得到了下列几组数据:
①原样品质量m
②通入玻璃管的CO质量m1
③完全反应后玻璃管内固体质量m2
④完全反应前后B增重的质量m3
请选择适当的数据并计算样品中氧化铜的质量分数为______ 。

(1)装置A中发生反应的化学方程式为
(2)为保证实验结果的准确性和安全性,开始加热前应排尽管内空气,则弹簧夹K1、K2应如何控制?具体操作是
(3)装置D的作用是
(4)实验结束后得到了下列几组数据:
①原样品质量m
②通入玻璃管的CO质量m1
③完全反应后玻璃管内固体质量m2
④完全反应前后B增重的质量m3
请选择适当的数据并计算样品中氧化铜的质量分数为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】化学是一门以实验为基础的学科。根据下列装置图回答。
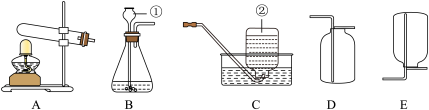
(1)写出图中标号仪器名称:①_______ 。
(2)实验室用高锰酸钾制取并收集较纯净的氧气应选用的装置是_______ (填序号),该反应的化学方程式为_______ 。
(3)实验室用锌粒和稀硫酸(液体)常温下混合制取氢气,应选择的发生装置是_____ 。(填序号)
(4)实验室还可以用分解过氧化氢液体的方法制取氧气。常温下,在试管中分别加入下列物质,把带火星的木条伸入试管,不能使木条复燃的是_______。
(5)某过氧化氢的水溶液,H2O2与水的质量比为1:18,则该溶液中氢、氧原子的个数比为:____ 。
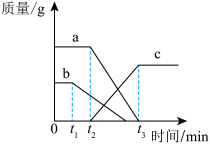
(6)某同学误将少量KMnO4当成MnO2加入KC1O3中进行加热制取氧气,部分物质质量随时间变化如图所示,下列关于该过程的说法正确的是_______(填字母)。

(1)写出图中标号仪器名称:①
(2)实验室用高锰酸钾制取并收集较纯净的氧气应选用的装置是
(3)实验室用锌粒和稀硫酸(液体)常温下混合制取氢气,应选择的发生装置是
(4)实验室还可以用分解过氧化氢液体的方法制取氧气。常温下,在试管中分别加入下列物质,把带火星的木条伸入试管,不能使木条复燃的是_______。
| A.5mL5%的过氧化氢溶液 | B.5mL5%的过氧化氢溶液和少量二氧化锰 |
| C.5mL5%的过氧化氢溶液和少量硫酸铜溶液 | D.5mL5%的过氧化氢溶液和少量红砖粉末 |
(5)某过氧化氢的水溶液,H2O2与水的质量比为1:18,则该溶液中氢、氧原子的个数比为:
(6)某同学误将少量KMnO4当成MnO2加入KC1O3中进行加热制取氧气,部分物质质量随时间变化如图所示,下列关于该过程的说法正确的是_______(填字母)。

| A.c代表氧气 | B.t2时刻,O2开始产生 |
| C.t1时刻,KMnO4开始分解 | D.上述反应过程中MnO2的质量一直保持不变 |
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】同学们参观了某钢铁厂后,设计了如图所示的实验装置,模拟工业炼铁的原理,他们称取10.0g赤铁矿,实验结束后称量剩余固体的质量为7.6g(假设赤铁矿中的杂质均不参与反应)。

(1)请你写出A装置中反应的化学方程式______ 。
(2)赤铁矿中含氧化铁的质量分数为______ 。
(3)下列对该实验的分析正确的是______ 。
①实验开始时,应先加热,再通入一氧化碳
②整套装置有一个明显的不足之处是没有进行尾气处理
③反应结束后,为避免空气污染,应立即停止通入一氧化碳
④如果氢氧化钠溶液足量,还可以利用B装置质量的增加量,计算出含杂质的质量分数

(1)请你写出A装置中反应的化学方程式
(2)赤铁矿中含氧化铁的质量分数为
(3)下列对该实验的分析正确的是
①实验开始时,应先加热,再通入一氧化碳
②整套装置有一个明显的不足之处是没有进行尾气处理
③反应结束后,为避免空气污染,应立即停止通入一氧化碳
④如果氢氧化钠溶液足量,还可以利用B装置质量的增加量,计算出含杂质的质量分数
您最近一年使用:0次