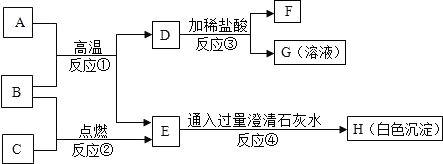
如图是初中化学中六种常见物质之间的转化关系图,已知A、D、F均为单质,其中D、F为金属单质,D的合金是使用最多的金属材料,B为氧化物,C是一种常见的酸,E可用于配制波尔多液。部分生成物及反应条件已略去,试回答下列问题。______ 。
(2)上述反应中,不属于置换反应的是______ (填序号)。
(3)反应①的化学方程式:______ 。
(4)A在生产、生活中的一种用途______ 。
(2)上述反应中,不属于置换反应的是
(3)反应①的化学方程式:
(4)A在生产、生活中的一种用途
更新时间:2024-05-09 15:36:02
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】(1)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。不能用铁质容器配制波尔多液的原因是_______ (用化学方程式表示)。
(2)金属铝比金属铁更耐腐蚀的原因_______ (用化学方程式表示)。
(3)已知M、N、R三种金属存在如下反应:R+NCl2=N+RCl2;M+RCl2=R+MCl2.这两个反应的基本反应类型都是_______ 反应,M、N、R三种金属的活动性由强到弱的顺序为_______ 。
(2)金属铝比金属铁更耐腐蚀的原因
(3)已知M、N、R三种金属存在如下反应:R+NCl2=N+RCl2;M+RCl2=R+MCl2.这两个反应的基本反应类型都是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】工业上炼铁炼钢和轧制钢材的主要流程如图。

已知生铁的含碳量为2%﹣4.3%,钢的含碳量为0.03%﹣2%。
(1)反应:①Fe2O3+3CO 2Fe+3CO2,②Fe2O3+3C
2Fe+3CO2,②Fe2O3+3C 2Fe+3CO。属于置换反应的是
2Fe+3CO。属于置换反应的是_____ ,用于高炉炼铁的原理是_____ (填序号)。
(2)炼铁的固体原料需经过粉碎,其目的是_____ 。
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是_____ 。
(4)炼钢炉中,通入纯氧的目的是_____ 。将钢锭轧成钢板,体现了金属的_____ 性。
(5)钢铁制品可能会生锈,写出用稀盐酸除铁锈的化学方程式_____ 。

已知生铁的含碳量为2%﹣4.3%,钢的含碳量为0.03%﹣2%。
(1)反应:①Fe2O3+3CO
 2Fe+3CO2,②Fe2O3+3C
2Fe+3CO2,②Fe2O3+3C 2Fe+3CO。属于置换反应的是
2Fe+3CO。属于置换反应的是(2)炼铁的固体原料需经过粉碎,其目的是
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是
(4)炼钢炉中,通入纯氧的目的是
(5)钢铁制品可能会生锈,写出用稀盐酸除铁锈的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】向硝酸锌、硝酸铜和硝酸银的混合溶液中,加入一定质量的铁粉,充分反应后过滤,得到滤渣和滤液。回答下列问题:
(1)写出可能发生的反应的化学方程式:______ ,该反应的基本类型为______ ;
(2)滤渣中一定含有的物质的化学式是______ ;滤液中可能含有的阳离子的符号是______ 。
(1)写出可能发生的反应的化学方程式:
(2)滤渣中一定含有的物质的化学式是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】将一定量的锌粉加入到一定量硝酸铜、硝酸银混合溶液中,充分反应后过滤,得到滤液和滤渣。
(1)写出一定能发生反应的方程式。
(2)若想滤渣中加入稀盐酸有气泡产生,则滤液中含有什么溶质?
(3)若滤液呈无色,则过滤出的滤渣一定含有那些金属?
(1)写出一定能发生反应的方程式。
(2)若想滤渣中加入稀盐酸有气泡产生,则滤液中含有什么溶质?
(3)若滤液呈无色,则过滤出的滤渣一定含有那些金属?
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐3】铝、铁、铜、银是生活中常见的金属,回答相关问题。
(1)铝在金属活动顺序表中位于铁之前,但铝比铁耐腐蚀的原因是_______ 。
(2)西汉时期的《淮南万毕术》中就有“曾青得铁则化为铜”的说法,是湿法炼铜的重要方法之一。其含义是把铁片放入硫酸铜溶液中可得到单质铜,此过程发生反应的化学方程式是_______ 。
(3)生铁和钢是铁的两种合金,两者性能差异大的主要原因是_______ 。
(4)某工厂欲从AgNO3和Cu(NO3)2的废液中回收Ag和Cu。取样,向其中加入一定量的锌,充分反应后过滤,得到滤渣和滤液。若向所得滤渣中加入硝酸铜溶液,一段时间后红色固体明显增加,则滤液中的阳离子为_______ 。
(1)铝在金属活动顺序表中位于铁之前,但铝比铁耐腐蚀的原因是
(2)西汉时期的《淮南万毕术》中就有“曾青得铁则化为铜”的说法,是湿法炼铜的重要方法之一。其含义是把铁片放入硫酸铜溶液中可得到单质铜,此过程发生反应的化学方程式是
(3)生铁和钢是铁的两种合金,两者性能差异大的主要原因是
(4)某工厂欲从AgNO3和Cu(NO3)2的废液中回收Ag和Cu。取样,向其中加入一定量的锌,充分反应后过滤,得到滤渣和滤液。若向所得滤渣中加入硝酸铜溶液,一段时间后红色固体明显增加,则滤液中的阳离子为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】人类文明的发展和社会的进步同金属材料关系十分密切。
(1)我国“蛟龙”号载人潜入器上使用了钛合金,钛合金放在海水中数年仍光亮如初,这是因为它_____ 。(填字母代号)
a易加工 b密度小 c熔点高 d耐腐蚀
(2)下列有关金属的说法,正确的是________ (填字母代号)。
a活泼金属与酸反应有气体产生,则与酸反应产生气体的一定是活泼金属
b稀土是储量较少的一类金属的统称,有“工业的维生素”的美誉
c生铁不能完全溶解到足量的稀硫酸(或稀盐酸)中
d可以用相同质量的锌、铁分别与适量的盐酸反应,来比较锌和铁的金属活动性强弱
(3)铁制品在潮湿的空气中容易生锈(主要成分是氧化铁),用盐酸清除铁锈的化学方程式为________ 。
(4)月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下不与酸反应、耐腐蚀等优良的性能,被誉为“未来金属”。我省有大型钒钛磁铁矿,由钒钛磁铁矿提取金属钛的主要工艺过程如下:

a钛铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛的化合价为________ 价。
bTiCl4在高温下与足量镁反应生成金属Ti和另一化合物,请写出该反应的化学方程式:________ 。
c上述生产过程中得到的金属钛中往往混有少量金属杂质,可加入______ 除去。
(1)我国“蛟龙”号载人潜入器上使用了钛合金,钛合金放在海水中数年仍光亮如初,这是因为它
a易加工 b密度小 c熔点高 d耐腐蚀
(2)下列有关金属的说法,正确的是
a活泼金属与酸反应有气体产生,则与酸反应产生气体的一定是活泼金属
b稀土是储量较少的一类金属的统称,有“工业的维生素”的美誉
c生铁不能完全溶解到足量的稀硫酸(或稀盐酸)中
d可以用相同质量的锌、铁分别与适量的盐酸反应,来比较锌和铁的金属活动性强弱
(3)铁制品在潮湿的空气中容易生锈(主要成分是氧化铁),用盐酸清除铁锈的化学方程式为
(4)月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下不与酸反应、耐腐蚀等优良的性能,被誉为“未来金属”。我省有大型钒钛磁铁矿,由钒钛磁铁矿提取金属钛的主要工艺过程如下:

a钛铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛的化合价为
bTiCl4在高温下与足量镁反应生成金属Ti和另一化合物,请写出该反应的化学方程式:
c上述生产过程中得到的金属钛中往往混有少量金属杂质,可加入
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】铝制易拉罐中的主要成分是铝,可能还含有镁、铁。下面是某化学兴趣小组同学对某打磨后的铝制易拉罐成分的探究过程,请完成有关问题。(已知∶铝能与氢氧化钠溶液反应∶2Al+2NaOH+2H2O=2NaAlO2+3H2↑,镁和铁不能与氢氧化钠溶液反应)
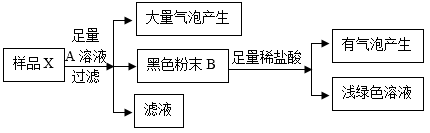
(1)过滤操作中,玻璃棒的作用是_________ 。
(2)A 的名称是_______ ,通过上述流程,可得出样品 X中一定含有的金属是______ 。
(3)写出上述产生浅绿色溶液的化学方程式:________ ,该反应属于_______ (填基本反应类型)。

(1)过滤操作中,玻璃棒的作用是
(2)A 的名称是
(3)写出上述产生浅绿色溶液的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】下图是某种制备高纯硅的工艺流程图:

(1)操作Ⅰ的名称是______ ,用到的玻璃仪器有______ 、烧杯、玻璃棒。
(2)操作Ⅰ后所得粗硅应充分洗涤,以除去表面可能含有的______ (填化学式)。
(3)反应Ⅱ要在无氧环境中进行,原因是______ 。
(4)上述生产流程中,可以循环利用的物质是______ (填化学式)。
(5)若反应Ⅱ中有17kg的SiCl4参加反应,则理论上可生产高纯硅多少kg?(写出计算过程)

(1)操作Ⅰ的名称是
(2)操作Ⅰ后所得粗硅应充分洗涤,以除去表面可能含有的
(3)反应Ⅱ要在无氧环境中进行,原因是
(4)上述生产流程中,可以循环利用的物质是
(5)若反应Ⅱ中有17kg的SiCl4参加反应,则理论上可生产高纯硅多少kg?(写出计算过程)
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】黄铜矿经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4,利用以下实验可制取补血剂原料碳酸亚铁并回收铜。

(1)步骤Ⅰ中,发生反应的化学方程式包括:
①Fe2(SO4)3+Fe=3FeSO4 ,
②________________________________________ ,
③________________________________________ 。
(2)步骤Ⅱ中加入一种试剂可实现其转化,该试剂可以是_________ (填化学式)。
(3)步骤Ⅲ回收铜的实验操作包括:①过滤、②洗涤、③加足量稀硫酸、④干燥,正确的操作排序是_____________ (填序号)。
(4)若废铁屑含有少量铁锈,对实验结果_________ (填“有”或“无”)影响。

(1)步骤Ⅰ中,发生反应的化学方程式包括:
①Fe2(SO4)3+Fe=3FeSO4 ,
②
③
(2)步骤Ⅱ中加入一种试剂可实现其转化,该试剂可以是
(3)步骤Ⅲ回收铜的实验操作包括:①过滤、②洗涤、③加足量稀硫酸、④干燥,正确的操作排序是
(4)若废铁屑含有少量铁锈,对实验结果
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
【推荐2】今年春节期间播出的《舌尖3》,让籍籍无名的章丘铁锅名声大振,章丘手工铁锅制造需要历经十二道工序,再过十八遍火候,一千度高温锤炼,经受三万六千次锻打,其炉渣中主要含FeO、Fe2O3,还有一定量既不溶于水,也不与稀酸反应的杂质。现按如图工艺流程,用炉渣制备绿矾(FeSO4•7H2O)。请按要求回答问题:
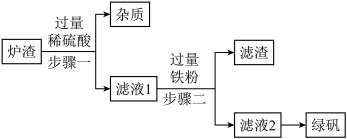
查阅资料:氧化亚铁与稀硫酸、铁与硫酸铁反应均可生成硫酸亚铁。
(1)步骤一中,发生反应的化学方程式为___ 、___ 。
(2)步骤一中的操作名称是___ ,为提高步骤一的反应速率,可采取的措施有增大硫酸的浓度,升高反应物的温度、还可以采取___ (写1条,不考虑“搅拌”和“使用催化剂”)。
(3)步骤二中无气体生成的化学反应方程式为___ ,测得滤液2的pH明显大于滤液1,其原因是___ 。
(4)滤液2得到绿矾可以采取的方法是___ 。
(5)某化学兴趣小组在实验室中利用该炉渣按照上述工艺流程制取绿矾。现取100g炉渣,得到干燥杂质5g,步骤二中加入15.6g铁粉,得到滤渣5.6g。要计算理论上制得绿矾的质量,除要利用上述给定的全部数据外,在实验过程中,还需测定的一个数据是___ 。

查阅资料:氧化亚铁与稀硫酸、铁与硫酸铁反应均可生成硫酸亚铁。
(1)步骤一中,发生反应的化学方程式为
(2)步骤一中的操作名称是
(3)步骤二中无气体生成的化学反应方程式为
(4)滤液2得到绿矾可以采取的方法是
(5)某化学兴趣小组在实验室中利用该炉渣按照上述工艺流程制取绿矾。现取100g炉渣,得到干燥杂质5g,步骤二中加入15.6g铁粉,得到滤渣5.6g。要计算理论上制得绿矾的质量,除要利用上述给定的全部数据外,在实验过程中,还需测定的一个数据是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
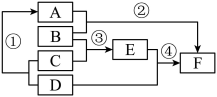
【推荐3】A、B、C、D均含有同一种金属元素,它们之间的转化关系如图(“→”表示反应可一步实现,部分物质和反应条件略去)。已知A是目前世界年产量最高的金属;B属于氧化物,其中金属元素质量分数为70%。

(1)这种金属元素属于人体必需的______ (填“常量元素”或 “微量元素”)。
(2)C的化学式为______ ;B→A的化学方程式为______ 。
(3)A与氧气、水可以发生化合反应生成D,该反应的化学方程式为______ 。

(1)这种金属元素属于人体必需的
(2)C的化学式为
(3)A与氧气、水可以发生化合反应生成D,该反应的化学方程式为
您最近一年使用:0次