醋酸钙虽然钙含量较低.但具有水溶性好、易吸收,胃肠道反应小的特点。因此.肠胃功能欠佳的患者通常建议选用作补钙剂。通常醋酸钙可由以下方法制得: 。
。
(1)醋酸钙中钙元素的质量分数是______ (结果保留两位小数)。
(2)取20g质量分数为30%的醋酸加入足量的氢氧化钙可制得多少醋酸钙?
 。
。(1)醋酸钙中钙元素的质量分数是
(2)取20g质量分数为30%的醋酸加入足量的氢氧化钙可制得多少醋酸钙?
更新时间:2024-05-26 11:58:12
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】2015年10月05日诺贝尔生理学或医学奖被授予,美国、日本和中国的三位科学家,美国科学家William C Campbell、日本科学家大村智和中国科学家屠呦呦分享了该奖项。屠呦呦则因青蒿素(化学C15H22O5)获奖,被誉为“拯救2亿人口”的发现。按要求完成下列问题:
(1)青蒿素的相对分子质量为________ 。
(2)青蒿素中碳、氢、氧原子的个数比为________ 。
(3)青蒿素中碳、氢、氧元素的质量比为__________ 。
(4)青蒿素中碳元素的质量分数是多少(计算结果保留一位小数)?
(5)100g青蒿素中含碳元素质量是多少?
(1)青蒿素的相对分子质量为
(2)青蒿素中碳、氢、氧原子的个数比为
(3)青蒿素中碳、氢、氧元素的质量比为
(4)青蒿素中碳元素的质量分数是多少(计算结果保留一位小数)?
(5)100g青蒿素中含碳元素质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】科学家经过研究,发现二氧化碳也是一种宝贵的碳氧资源.以CO2和NH3为原料合成尿素[CO(NH2)2]是故定和利用CO2的成功范例.它还可以与氢气反应生成多种有 机物,如甲烷(CH4)、乙烯(C2H4)等.试计算:
(1)CH4中碳、氢元素的质量比 .
(2) CO(NH2)2中氮元素的质量分数 .(计算结果精确到0.1%)
(3) CO2转化为C2H4的化学方程式为:2CO2+6H2 C2H4+4H2O,若用24g H2转化CO2,则理论上能生成C2H4多少克(列式计算)?
C2H4+4H2O,若用24g H2转化CO2,则理论上能生成C2H4多少克(列式计算)?
(1)CH4中碳、氢元素的质量比 .
(2) CO(NH2)2中氮元素的质量分数 .(计算结果精确到0.1%)
(3) CO2转化为C2H4的化学方程式为:2CO2+6H2
 C2H4+4H2O,若用24g H2转化CO2,则理论上能生成C2H4多少克(列式计算)?
C2H4+4H2O,若用24g H2转化CO2,则理论上能生成C2H4多少克(列式计算)?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】同学们为测定实验室里一瓶过氧化氢溶液中过氧化氢的质量,将 该过氧化氢溶液与
该过氧化氢溶液与 二氧化锰混合,完全反应后,固液残留物共
二氧化锰混合,完全反应后,固液残留物共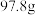 ,请计算:
,请计算:
(1)生成氧气______ 。
(2)该过氧化氢溶液中过氧化氢的质量分数(写出计算过程)。
 该过氧化氢溶液与
该过氧化氢溶液与 二氧化锰混合,完全反应后,固液残留物共
二氧化锰混合,完全反应后,固液残留物共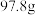 ,请计算:
,请计算:(1)生成氧气
(2)该过氧化氢溶液中过氧化氢的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】欲测定一瓶标签破损的稀盐酸的溶质质量分数,现取20g稀盐酸样品于烧杯中,将10%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示。回答下列问题:

(1)a点溶液中的溶质是______ (填化学式);
(2)计算该稀盐酸的溶质质量分数(写出计算过程)。

(1)a点溶液中的溶质是
(2)计算该稀盐酸的溶质质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】为测定某胃药中碳酸氢钠的含量,向一锥形瓶中加入10g该胃药,再加入100g一定质量分数的稀盐酸,恰好完全反应,气体全部逸出,反应后锥形瓶内物质的总质量为105.6g。(胃药中的其他成分不参与反应,不考虑稀盐酸挥发)。回答下列问题:

(1)反应结束共产生气体的质量是______g。
(2)若实验室用质量分数为34%的浓盐酸配制该实验所需桥盐酸,主要步骤有:计算、量取、______、装瓶并贴上标签。在配制过程中,用量筒量取水时俯视读数,但其它操作无误,用配制得到的盐酸按上述方法测定胃药中碳酸钠的含量,其结果会______。(填“偏大”、“不变”或“偏小”)
(3)该胃药中碳酸氢钠的质量分数(写出计算过程)。

(1)反应结束共产生气体的质量是______g。
(2)若实验室用质量分数为34%的浓盐酸配制该实验所需桥盐酸,主要步骤有:计算、量取、______、装瓶并贴上标签。在配制过程中,用量筒量取水时俯视读数,但其它操作无误,用配制得到的盐酸按上述方法测定胃药中碳酸钠的含量,其结果会______。(填“偏大”、“不变”或“偏小”)
(3)该胃药中碳酸氢钠的质量分数(写出计算过程)。
您最近一年使用:0次



