化学活动小组的同学们研究某碳酸钠样品中碳酸钠的含量,并将其转化为氯化钠(杂质不溶于水、也不与其它物质反应、高温也不分解),请根据反应流程图回答问题:______ ;
(2)样品中碳酸钠的质量分数为______ ;
(3)向 溶液中加入
溶液中加入______  水,可得到
水,可得到 烧杯中
烧杯中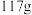 质量分数
质量分数 的氯化钠溶液;
的氯化钠溶液;
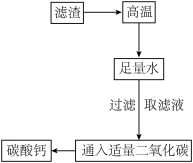
(4)将上述滤渣经过如下图所示的步骤进行处理,理论上可得到纯净的碳酸钙的质量为______ ; 的氯化钠溶液,正确的实验步骤是______(填字母)。
的氯化钠溶液,正确的实验步骤是______(填字母)。
A.称量 B.量取 C.计算 D.混匀 E.溶解
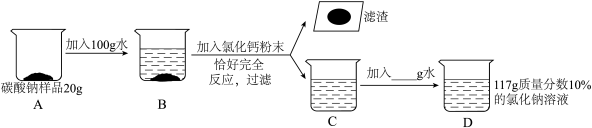
(2)样品中碳酸钠的质量分数为
(3)向
 溶液中加入
溶液中加入 水,可得到
水,可得到 烧杯中
烧杯中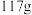 质量分数
质量分数 的氯化钠溶液;
的氯化钠溶液;(4)将上述滤渣经过如下图所示的步骤进行处理,理论上可得到纯净的碳酸钙的质量为
 的氯化钠溶液,正确的实验步骤是______(填字母)。
的氯化钠溶液,正确的实验步骤是______(填字母)。A.称量 B.量取 C.计算 D.混匀 E.溶解
更新时间:2024-05-23 23:17:38
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
【推荐1】根据下面的实验过程和提供的数据,回答下列问题。(不考虑反应中水分的蒸发,假设生成的气体全部逸出)
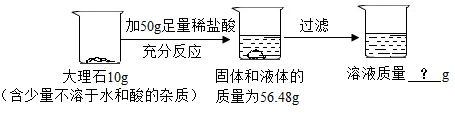
① 生成二氧化碳的物质的量____________ mol 。
② 通过化学方程式计算大理石中碳酸钙的质量分数________ 。(写出计算过程)
③ 过滤后溶液的质量为_____________ g。

① 生成二氧化碳的物质的量
② 通过化学方程式计算大理石中碳酸钙的质量分数
③ 过滤后溶液的质量为
您最近一年使用:0次
【推荐2】过氧化钙(CaO2)是一种增氧剂,它与水反应生成相应的碱和O2,请写出该反应的化学方程式_________________________________ 。某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将50 g该混合物高温煆烧至固体质量不再改变,则生成二氧化碳的质量是__________________ g
您最近一年使用:0次
【推荐3】铁及其化合物在生活生产中有重要的应用。请回答下列问题:
(1)2022年北京冬奥会国家速滑馆“冰丝带”采用世界跨度最大的单层双向正交马鞍形索网屋面,用钢量仅为传统屋面的四分之一、下列关于钢铁的说法错误的是 。
(2)把铁粉和碳粉的混合物放入硝酸银溶液中,充分反应后,过滤,为确定滤渣和滤液的成分,甲同学向滤渣中滴加稀盐酸,无气泡产生;乙同学向滤液中滴加稀盐酸,产生白色沉淀。根据两同学实验的现象,分析下列结论不正确的是 (填序号)。
(3)废铁屑的主要成分是铁,同时还有少量铁锈(Fe2O3),生产动物饲料添加剂硫酸亚铁的工艺流程之一如下图所示:

在反应器中发生反应的化学方程式有:
①Fe+H2SO4═FeSO4+H2↑、②_______ 、③Fe2(SO4)3+Fe═3FeSO4。
滤液M中肯定含有的溶质的化学式是_______ ;
(4)取生铁5.8g(除碳外,无其它杂质),加入到足量的20.0g的稀硫酸中,充分反应后,所得混合物的总质量为25.6g。则生铁中铁的质量为_______ g。
(1)2022年北京冬奥会国家速滑馆“冰丝带”采用世界跨度最大的单层双向正交马鞍形索网屋面,用钢量仅为传统屋面的四分之一、下列关于钢铁的说法错误的是 。
| A.铁是目前年产量最高的金属 | B.钢铁在潮湿的空气中不发生锈蚀 |
| C.用磁铁可区分铁制品和铝制品 | D.钢的许多性能优于生铁 |
| A.滤渣中只含银 | B.滤渣中可能含有银,一定含有碳 |
| C.滤液中一定有Ag+、Fe2+ | D.滤液中只含Ag+,不含Fe2+ |

在反应器中发生反应的化学方程式有:
①Fe+H2SO4═FeSO4+H2↑、②
滤液M中肯定含有的溶质的化学式是
(4)取生铁5.8g(除碳外,无其它杂质),加入到足量的20.0g的稀硫酸中,充分反应后,所得混合物的总质量为25.6g。则生铁中铁的质量为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】如图所示是三种物质的溶解度曲线。请回答:

(1)溶解度随温度升高而降低的是_______ ;30℃时溶解度最大的是____ 。
(2)80℃时硝酸钠饱和溶液的溶质质量分数为____ 。使硝酸钠不饱和溶液变为饱和溶液,可采取的措施有_______ (写一种)。
(3)某硝酸钾固体中混有少量硫酸钠杂质,分离提纯硝酸钾的操作是:配成高温下的硝酸钾饱和溶液、______ 、过滤、洗涤、干燥。
(4)30℃用等质量的硝酸钾、硝酸钠配制两种物质的饱和溶液需要水的质量硝酸钾____ 硝酸钠(填“>”“<”或“=”);
(5)配制一定溶质质量分数的硝酸钾溶液,以下操作中会导致所配制溶液溶质质量分数偏低的是____ 。
A 量筒量取水时仰视读数
B 配制好的溶液向细口瓶转移时溅出
C 硝酸钾固体中含有杂质
D 烧杯事先用水润洗过,内壁有水

(1)溶解度随温度升高而降低的是
(2)80℃时硝酸钠饱和溶液的溶质质量分数为
(3)某硝酸钾固体中混有少量硫酸钠杂质,分离提纯硝酸钾的操作是:配成高温下的硝酸钾饱和溶液、
(4)30℃用等质量的硝酸钾、硝酸钠配制两种物质的饱和溶液需要水的质量硝酸钾
(5)配制一定溶质质量分数的硝酸钾溶液,以下操作中会导致所配制溶液溶质质量分数偏低的是
A 量筒量取水时仰视读数
B 配制好的溶液向细口瓶转移时溅出
C 硝酸钾固体中含有杂质
D 烧杯事先用水润洗过,内壁有水
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】2015年3月22日是第二十三个“世界水日”。关于水的知识有下列话题。请按要求填空:
(1)在净化水的过程中,明矾所起的作用是除去水中的_____ 。
(2)生活中可用_____ 来检验地下水是硬水还是软水。常用_____ 的方法来降低水的硬度。
(3)测定某地下水的酸碱度,最简单的方法是使用_____ 。
(4)在生产生活中,水是最常用的溶剂。实验室用氯化钠配制一定溶质质量分数的溶液时。可能涉及以下操作:
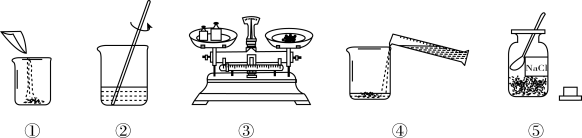
①上图操作中有错误的是_____ (填序号)。
②改正错误后,正确的操作顺序是_____ (填序号)。
A ⑤②①③④
B ⑤①②③④
C ⑤③②④①
D ⑤③①④②
(1)在净化水的过程中,明矾所起的作用是除去水中的
(2)生活中可用
(3)测定某地下水的酸碱度,最简单的方法是使用
(4)在生产生活中,水是最常用的溶剂。实验室用氯化钠配制一定溶质质量分数的溶液时。可能涉及以下操作:

①上图操作中有错误的是
②改正错误后,正确的操作顺序是
A ⑤②①③④
B ⑤①②③④
C ⑤③②④①
D ⑤③①④②
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如下图是实验室配制一定溶质质量分数的KNO3溶液的流程图。请回答:
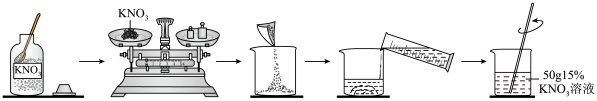
(1)计算:用托盘天平应称量_____ gKNO3。
(2)称量:若称量KNO3固体时指针向左偏转,则应_____ (填字母),直到天平平衡。
A增加砝码B移动游码C减少KNO3固体D增加KNO3固体
(3)量取:量取水时,应选择_____ (填“10mL”、“50mL”或“100mL”)的量筒。
(4)溶解:若KNO3已结块,为了较快地溶解,合理的方法有_____ (填数字序号)。
①将硝酸钾研碎②用热水溶解③加入更多的水④用玻璃棒搅拌
(5)下列操作中可能导致配制硝酸钾溶液的溶质质量分数偏小的是_____ (填序号)。
A硝酸钾中含有杂质
B量取水时仰视
C用已有少量水的烧杯溶解硝酸钾
D转移时,有少量溶液溅出
(6)取上述溶液10g,需加_____ g水稀释,可得到5%的硝酸钾溶液。

(1)计算:用托盘天平应称量
(2)称量:若称量KNO3固体时指针向左偏转,则应
A增加砝码B移动游码C减少KNO3固体D增加KNO3固体
(3)量取:量取水时,应选择
(4)溶解:若KNO3已结块,为了较快地溶解,合理的方法有
①将硝酸钾研碎②用热水溶解③加入更多的水④用玻璃棒搅拌
(5)下列操作中可能导致配制硝酸钾溶液的溶质质量分数偏小的是
A硝酸钾中含有杂质
B量取水时仰视
C用已有少量水的烧杯溶解硝酸钾
D转移时,有少量溶液溅出
(6)取上述溶液10g,需加
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】牙膏中的摩擦剂碳酸钙可以用石灰石来制备,小华同学设计了下列实验方案:

(1)理论上,所得碳酸钙的质量_______ 石灰石中碳酸钙的质量(选填“大于”“等于”或“小于”之一)
(2)写出步骤②的化学方程式_______ ,该反应属于_______ (选填“化合”“分解”“置换”或“复分解”之一)反应。
(3)取12.5g石灰石(主要成分碳酸钙,杂质不溶于水也不参加反应),加入100g7.3%的稀盐酸,恰好完全反应,求生成二氧化碳气体____ 克?

(1)理论上,所得碳酸钙的质量
(2)写出步骤②的化学方程式
(3)取12.5g石灰石(主要成分碳酸钙,杂质不溶于水也不参加反应),加入100g7.3%的稀盐酸,恰好完全反应,求生成二氧化碳气体
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】将氢氧化溶液加入稀硫酸的反应,溶液pH的变化如图所示。
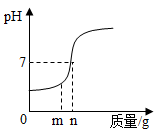
(1)当所加溶液的质量为mg时,所得溶液中溶质为______ (写化学式)。
(2)完全中和一定质量的某硫酸溶液,需要100g 8%的氢氧化钠溶液,若改用100g 8%的氢氧化钾溶液,则反应后溶液的pH______ 7(填“>”、“<”或“=”)。

(1)当所加溶液的质量为mg时,所得溶液中溶质为
(2)完全中和一定质量的某硫酸溶液,需要100g 8%的氢氧化钠溶液,若改用100g 8%的氢氧化钾溶液,则反应后溶液的pH
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】Fe(OH)3可用于制造医药、颜料等,其胶体可用于净水。某化学兴趣小组利用废铁屑来制备Fe(OH)3粉末的流程如下:
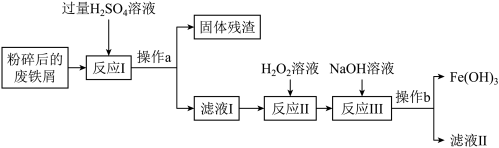
资料:①废铁屑主要为表面附有大量铁锈的铁。
②Fe(OH)3难溶于水,加热时会分解生成氧化铁和水。
③H2O2溶液可以将Fe2+氧化成Fe3+。
(1)操作a的名称为_______ 。
(2)滤液I中除了 外,还存在着的离子是
外,还存在着的离子是_______ 。(写离子符号)
(3)反应I中,需要_______ g20%的H2SO4溶液才能与5.6g铁恰好完全反应。

资料:①废铁屑主要为表面附有大量铁锈的铁。
②Fe(OH)3难溶于水,加热时会分解生成氧化铁和水。
③H2O2溶液可以将Fe2+氧化成Fe3+。
(1)操作a的名称为
(2)滤液I中除了
 外,还存在着的离子是
外,还存在着的离子是(3)反应I中,需要
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
【推荐1】现探究一固体混合物的成分,已知其中可能含有Na2CO3、CuSO4、BaCl2、K2SO4、NaCl五种物质中的一种或几种,按图所示进行实验操作,现象如图中所述(设过程中所有可能发生的反应都完全进行)。
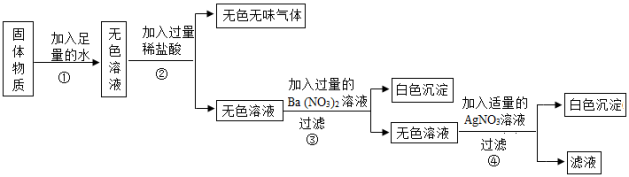
试根据实验过程和发生的现象做出判断,完成下列问题:
(1)根据操作①所得现象,判断出物质中一定没有______ 。
(2)根据操作②所得现象,判断出物质中一定含有______ ,一定没有______ 。
(3)根据操作③所得现象,判断出物质中一定有______ 。
(4)实验过程中不能确定是否存在的物质是______ ,为了使实验流程能够确定该物质是否存在,则原实验流程需要做怎样的改进?______ 。

试根据实验过程和发生的现象做出判断,完成下列问题:
(1)根据操作①所得现象,判断出物质中一定没有
(2)根据操作②所得现象,判断出物质中一定含有
(3)根据操作③所得现象,判断出物质中一定有
(4)实验过程中不能确定是否存在的物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】已知粗盐中含有泥沙、氯化钙和硫酸镁等杂质。为情得纯净的氯化钠固体。某化学兴趣小组进行了如下操作:
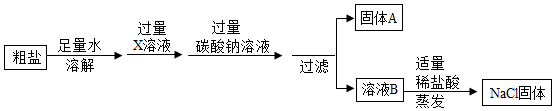
(1)写出X溶液中溶质的化学式。
(2)最后制得氯化钠的质量大于粗盐中氯化钠的质量,写出一个可使氯化钠质量增加的化学方程式。

(1)写出X溶液中溶质的化学式。
(2)最后制得氯化钠的质量大于粗盐中氯化钠的质量,写出一个可使氯化钠质量增加的化学方程式。
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
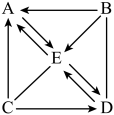
【推荐3】某同学学过酸碱盐的知识后,构建了如图以某种盐为中心的关系图。A、B、C、D属于四种不同类别的化合物;E是一种白色难溶于水的物质,其中金属元素的质量分数为40%,C是胃酸的主要成分,D在空气中含量过高会导致温室效应加剧。
(1)C的化学式为_______ 。
(2)A→E反应所属基本反应类型为_______ 。
(3)写出B和D反应的化学方程式:_______ 。
(1)C的化学式为
(2)A→E反应所属基本反应类型为
(3)写出B和D反应的化学方程式:
您最近一年使用:0次



