见证科技发展,感受民族复兴。
Ⅰ.能源是人类进行生产的原动力,能源革命在演变。
(1)古代,原始人类通过“钻木取火”,迈进了植物能源时代,钻木取火中“钻木”过程满足了木头燃烧所需要的条件是_______ 。
(2)18世纪,化石能源取代植物能源,常见的化石燃料有煤、石油、天然气等,写出天然气(主要成分为甲烷)燃烧的化学方程式_______ 。
(3)当前,是新能源和可再生能源的革命。我国氢能按如图规划发展迅速:

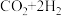 发生,该反应属于
发生,该反应属于_______ 反应(填基本反应类型),反应中体现还原性的物质是______ (填化学式)。
②蓝氢是将天然气重整制成。通过碳捕捉先进技术,减轻了___ (填物质名称)对地球环境的影响。该气体被捕捉后封存在含氢氧化钙的地下水层中,可慢慢转化为固态碳酸盐,该碳酸盐的化学式是____ 。
③通过“可再生能源”分解水可制得绿氢,写出相关的化学方程式_______ 。
Ⅱ.依据粗盐中不溶性杂质(泥沙)及可溶性杂质(MgCl2)的去除,某同学建构了“物质除杂”的思维模型。_______ 。
(5)采用“反应转化法”,可除去粗盐水中的MgCl2,写出应加入的除杂试剂_______ 。
(6)通过向(5)的滤液中滴加盐酸,可除去过量的除杂试剂,利用数字化实验测定溶液的pH变化如图2所示。则M点时溶液中溶质的成分是_______ (填化学式)
Ⅰ.能源是人类进行生产的原动力,能源革命在演变。
(1)古代,原始人类通过“钻木取火”,迈进了植物能源时代,钻木取火中“钻木”过程满足了木头燃烧所需要的条件是
(2)18世纪,化石能源取代植物能源,常见的化石燃料有煤、石油、天然气等,写出天然气(主要成分为甲烷)燃烧的化学方程式
(3)当前,是新能源和可再生能源的革命。我国氢能按如图规划发展迅速:

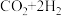 发生,该反应属于
发生,该反应属于②蓝氢是将天然气重整制成。通过碳捕捉先进技术,减轻了
③通过“可再生能源”分解水可制得绿氢,写出相关的化学方程式
Ⅱ.依据粗盐中不溶性杂质(泥沙)及可溶性杂质(MgCl2)的去除,某同学建构了“物质除杂”的思维模型。

(5)采用“反应转化法”,可除去粗盐水中的MgCl2,写出应加入的除杂试剂
(6)通过向(5)的滤液中滴加盐酸,可除去过量的除杂试剂,利用数字化实验测定溶液的pH变化如图2所示。则M点时溶液中溶质的成分是
更新时间:2024-05-24 16:33:20
|
相似题推荐
综合应用题
|
较易
(0.85)
解题方法
【推荐1】化学与人类生产、生活关系密切。
Ⅰ. 生活:
(1)枸杞富含葡萄糖等枸杞多糖,维生素B1、B2等多种维生素,氨基乙磺酸等氨基酸,以及钾、钠、钙、镁、锌、铁等人体必需的元素,具有促进新陈代谢,改善肝功能和心脏功能的功效。
①枸杞中含有人体必需的微量元素有______________________ 。
②在种植枸杞的过程中,发现枸杞树叶颜色发黄,应该施加的化肥种类是______________ 。
(2)央视四套播出的“记住乡愁”栏目中介绍 “天水茶”。所谓“天水”即雨水,雨水经纱网进行两次过滤后,存入水缸中继续沉降,留待制作“天水茶”。
①“天水”与井水、河水相比,用水壶烧开后水垢很少,说明“天水”里可溶性杂质较少,属于___________ (填“软水”或“硬水”),因而带来了口感等方面的巨大不同。
② 通过“煮沸”可将井水中的可溶性杂质转化为水垢来降低井水的硬度。该“煮沸”过程属于____________ (填“物理”或“化学”)变化。
Ⅱ. 工业:
(3)①轮船上使用的特种钢中含有少量Mn。MnO2和Al粉的混合物在高温下反应可得到Mn和Al2O3,该反应的化学方程式为______________ 。
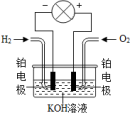
②氢氧燃料电池是符合绿色化学理念的新型电池。如图是氢氧燃料电池的示意图,工作时H2和O2反应生成水,同时提供电能,氢氧燃料电池工作的过程中,参加反应的氢气和氧气的质量比为_______ ,此时溶液的pH值_____________ (填“变大”、“变小”或“不变”)。
(4)农作物秸秆综合利用对于促进环境保护、资源节约以及农业经济可持续发展意义重大。
① 以秸秆[主要成分纤维素(C6H10O5)n]为原料可生产出可降解塑料餐盒,该塑料属于________ (填“合成”或“天然”)有机高分子材料。
② 农民利用秸秆、杂草、人畜粪便等废弃物在密闭的沼气池中发酵,产生沼气。沼气的主要成分是甲烷。利用甲烷隔绝空气高温加热制取炭黑,同时得到自然界最轻的气体,该反应化学方程式为__________________ 。
Ⅰ. 生活:
(1)枸杞富含葡萄糖等枸杞多糖,维生素B1、B2等多种维生素,氨基乙磺酸等氨基酸,以及钾、钠、钙、镁、锌、铁等人体必需的元素,具有促进新陈代谢,改善肝功能和心脏功能的功效。
①枸杞中含有人体必需的微量元素有
②在种植枸杞的过程中,发现枸杞树叶颜色发黄,应该施加的化肥种类是
(2)央视四套播出的“记住乡愁”栏目中介绍 “天水茶”。所谓“天水”即雨水,雨水经纱网进行两次过滤后,存入水缸中继续沉降,留待制作“天水茶”。
①“天水”与井水、河水相比,用水壶烧开后水垢很少,说明“天水”里可溶性杂质较少,属于
② 通过“煮沸”可将井水中的可溶性杂质转化为水垢来降低井水的硬度。该“煮沸”过程属于
Ⅱ. 工业:
(3)①轮船上使用的特种钢中含有少量Mn。MnO2和Al粉的混合物在高温下反应可得到Mn和Al2O3,该反应的化学方程式为
②氢氧燃料电池是符合绿色化学理念的新型电池。如图是氢氧燃料电池的示意图,工作时H2和O2反应生成水,同时提供电能,氢氧燃料电池工作的过程中,参加反应的氢气和氧气的质量比为
(4)农作物秸秆综合利用对于促进环境保护、资源节约以及农业经济可持续发展意义重大。
① 以秸秆[主要成分纤维素(C6H10O5)n]为原料可生产出可降解塑料餐盒,该塑料属于
② 农民利用秸秆、杂草、人畜粪便等废弃物在密闭的沼气池中发酵,产生沼气。沼气的主要成分是甲烷。利用甲烷隔绝空气高温加热制取炭黑,同时得到自然界最轻的气体,该反应化学方程式为
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐2】近年来,我国已突破掌握载人航天领域重大技术,载人航天重大工程建设顺利推进。请根据所学知识回答下列问题:
Ⅰ:航天器使用的动力
(1)我国载人飞船均由长征二号F运载火箭发射升空。运载火箭由三级火箭组成。一级和二级火箭的推进剂为偏二甲膜(C2H8N2)和四氧化二氮(N2O4),其反应的化学方程式为: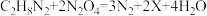 ,则X的化学式为
,则X的化学式为______ ;三级火箭的推进剂为液氢和液氧,用氢气作燃料的优点是______ (一条即可)。
(2)进入太空后,动力由太阳能电池提供。神舟飞船使用的太阳能电池是砷化镓电池,砷、镓的原子结构示意图如图所示,下列有关说法不正确的是______ (填字母)。
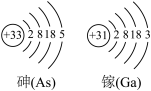
a.砷元素属于非金属元素 b.镓原子在化学反应中易失电子
c.两种元素位于同一周期 d.砷化镓的化学式为Ga3As5
Ⅱ:航天器使用的材料
(3)飞船的主要制造材料是铝,燃料舱、载人舱(逃逸舱)、轨道舱等部件都使用了大量的铝合金。铝合金属于______ (填“金属材料”或“合成材料”)。铝具有优良的抗腐蚀性能,其原因是______ 。
(4)飞船上还使用了记忆合金、SiC颗粒增强铝基复合材料、橡塑材料、超高强度钢等新材料。超高强度铜材料中含金属锰,若将锰投入到硫酸亚铁溶液中,有物质析出,说明锰的金属活动性比铁______ (填“强”或“弱”)。
Ⅲ:航天器的生命保障系统
(5)飞船中航天员呼吸的氧气是将从尿处理系统输送来的水进行电解制取的,写出电解水的化学方程式______ 。
(6)航天员呼出的二氧化碳是在高温下,通过催化剂的作用与氧气反应,生成水和甲烷进行处理,其中水可以被送往饮用水系统供航天员饮用。若每天航天员能呼出3.3kg二氧化碳,则通过上述反应可产生水的质量是多少?
Ⅰ:航天器使用的动力
(1)我国载人飞船均由长征二号F运载火箭发射升空。运载火箭由三级火箭组成。一级和二级火箭的推进剂为偏二甲膜(C2H8N2)和四氧化二氮(N2O4),其反应的化学方程式为:
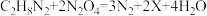 ,则X的化学式为
,则X的化学式为(2)进入太空后,动力由太阳能电池提供。神舟飞船使用的太阳能电池是砷化镓电池,砷、镓的原子结构示意图如图所示,下列有关说法不正确的是

a.砷元素属于非金属元素 b.镓原子在化学反应中易失电子
c.两种元素位于同一周期 d.砷化镓的化学式为Ga3As5
Ⅱ:航天器使用的材料
(3)飞船的主要制造材料是铝,燃料舱、载人舱(逃逸舱)、轨道舱等部件都使用了大量的铝合金。铝合金属于
(4)飞船上还使用了记忆合金、SiC颗粒增强铝基复合材料、橡塑材料、超高强度钢等新材料。超高强度铜材料中含金属锰,若将锰投入到硫酸亚铁溶液中,有物质析出,说明锰的金属活动性比铁
Ⅲ:航天器的生命保障系统
(5)飞船中航天员呼吸的氧气是将从尿处理系统输送来的水进行电解制取的,写出电解水的化学方程式
(6)航天员呼出的二氧化碳是在高温下,通过催化剂的作用与氧气反应,生成水和甲烷进行处理,其中水可以被送往饮用水系统供航天员饮用。若每天航天员能呼出3.3kg二氧化碳,则通过上述反应可产生水的质量是多少?
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐3】我国争取在2030年实现碳达峰,2060年实现碳中和。采用物理或化学方法捕集CO2并将其资源化利用,正成为CO2控制排放的有效措施。
I.CO2排放
(1)动植物呼吸和化石燃料煤、石油和______ 的燃烧都会释放CO2。
II.CO2的捕集(图1) CaO+CO2↑+X↑+H2O↑。其中X的化学式为
CaO+CO2↑+X↑+H2O↑。其中X的化学式为______ 。该反应生成的CaO更加疏松多孔,有利于CaO捕集CO2,主要原因是_______ 。
(3)利用CaO捕集CO2。
温度对CO2的转化率影响较大,由上图2可知,捕集器内温度应控制在______ (填“650”或“750)℃为宜;捕集器内生成的CaCO3在煅烧炉中分解得到CaO和高浓度CO2,该反应的化学方程式为______ ;将分解所得CaO投入捕集器循环使用,循环使用的优点是______ 。
Ⅲ.CO2的资源化利用
中科院大连化学物理研究所研制出一种新型多功能复合催化剂,将CO2成功转化为汽油。______ 。
(5)对该成果的评价正确的是 。
I.CO2排放
(1)动植物呼吸和化石燃料煤、石油和
II.CO2的捕集(图1)
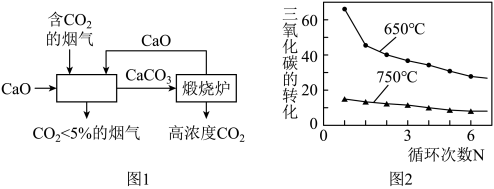
 CaO+CO2↑+X↑+H2O↑。其中X的化学式为
CaO+CO2↑+X↑+H2O↑。其中X的化学式为(3)利用CaO捕集CO2。
温度对CO2的转化率影响较大,由上图2可知,捕集器内温度应控制在
Ⅲ.CO2的资源化利用
中科院大连化学物理研究所研制出一种新型多功能复合催化剂,将CO2成功转化为汽油。
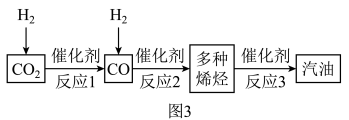
(5)对该成果的评价正确的是 。
| A.该成果有助于缓解全球温室效应 |
| B.该成果可减少对化石燃料的依赖 |
| C.CO2资源化利用过程中,催化剂对转化过程起到举足轻重的作用 |
您最近一年使用:0次
【推荐1】2023年10月26日,我国“神舟十七号”载人飞船成功发射,这是中国载人航天工程的第12次载人飞行任务,20年的奋斗,实现了从“太空一日”到6个月的长期驻留的突破。展现了“特别能吃苦,特别能战斗,特别能奉献,特别能攻关”的航天人精神。
(1)科学家们研制“人造空气”来供航天员呼吸。“人造空气”中氮气含量约占70%,氧气占20%以上,还有二氧化碳等气体,非常接近空气的比例。下列说法正确的是______(填序号)
(2)我国“长征”系列运载火箭燃料中的偏二甲肼的化学式为C2H8N2,偏二甲肼的相对分子质量为______ ,碳与氢元素的质量比为______ ,碳元素的质量分数为______ 。
(3)运载火箭燃料中的偏二甲肼,与四氧化二氮相混合后点燃便会剧烈燃烧,生成二氧化碳、水和一种空气中含量最多的气体,反应的化学方程式为______ ,通过此反应谈谈你对燃烧的概念有什么新的认识?______ 。
(1)科学家们研制“人造空气”来供航天员呼吸。“人造空气”中氮气含量约占70%,氧气占20%以上,还有二氧化碳等气体,非常接近空气的比例。下列说法正确的是______(填序号)
| A.空气中的二氧化碳含量虽然很小,但是在自然界中是必不可少的 |
| B.在航天飞船上,应把空气中的其他成分都分离出去,只留下氧气,会更有益于人的呼吸 |
| C.我们周围的空气中的各成份的体积分数是不变的,不随地域和季节的变化而变化 |
| D.空气中的氮气对人类呼吸没有任何作用,因此人造空气中可以没有这种气体 |
(3)运载火箭燃料中的偏二甲肼,与四氧化二氮相混合后点燃便会剧烈燃烧,生成二氧化碳、水和一种空气中含量最多的气体,反应的化学方程式为
您最近一年使用:0次
【推荐2】2024年4月24日是第九个中国航天日,主题为“极目楚天,共襄星汉”。中国人探索宇宙的脚步驰而不息。
(1)空间站种菜。航天员在太空吃到了自己种的蔬菜。蔬菜能为航天员提供______ (写1种主要的营养素)。为使蔬菜枝叶茂盛,可以施用的一种化肥是______ (写化学式)。太空蔬菜在塑料网篮中种植,塑料属于______ (填序号)。
A.无机非金属材料 B.有机高分子材料 C.金属材料 D.复合材料
(2)固体火箭发射卫星。我国在海阳市附近海域使用引力一号运载火箭将3颗卫星顺利送入预定轨道,刷新了全球最大固体运载火箭记录。高氯酸铵、铝粉等是固体运载火箭的主要推进剂,发射时高氯酸铵发生的化学反应是: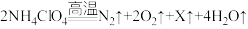
______ ,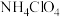 中氯元素的化合价是
中氯元素的化合价是______ 。
②铝粉在氧气中燃烧的化学方程式是______ 。
(3)太空燃烧实验。航天员在燃烧科学实验柜中以甲烷为燃料进行在轨点火燃烧实验,观察到甲烷火焰与地面上对照实验的火焰相比,显得短而圆,且微弱。______ (写1条)。
②从燃烧的条件分析,点火的作用是______ 。
③下列对燃烧实验分析正确的是______ (填序号)。
A.空间站甲烷燃烧,不需要氧气
B.空间站失重条件下燃烧产生的热气流向四周扩散,地面上热气流向上扩散
C.空间站失重条件下空气流动性差,甲烷燃烧的火焰比较微弱
(1)空间站种菜。航天员在太空吃到了自己种的蔬菜。蔬菜能为航天员提供
A.无机非金属材料 B.有机高分子材料 C.金属材料 D.复合材料
(2)固体火箭发射卫星。我国在海阳市附近海域使用引力一号运载火箭将3颗卫星顺利送入预定轨道,刷新了全球最大固体运载火箭记录。高氯酸铵、铝粉等是固体运载火箭的主要推进剂,发射时高氯酸铵发生的化学反应是:
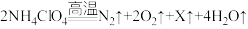

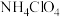 中氯元素的化合价是
中氯元素的化合价是②铝粉在氧气中燃烧的化学方程式是
(3)太空燃烧实验。航天员在燃烧科学实验柜中以甲烷为燃料进行在轨点火燃烧实验,观察到甲烷火焰与地面上对照实验的火焰相比,显得短而圆,且微弱。

②从燃烧的条件分析,点火的作用是
③下列对燃烧实验分析正确的是
A.空间站甲烷燃烧,不需要氧气
B.空间站失重条件下燃烧产生的热气流向四周扩散,地面上热气流向上扩散
C.空间站失重条件下空气流动性差,甲烷燃烧的火焰比较微弱
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐1】能源对社会的发展有着重要的影响。
(1)目前使用的煤、石油、天然气均为__________ (填“可再生”或“不可再生”)能源。
(2)我国海域可燃冰资源丰富,写出可燃冰中甲烷燃烧的化学方程式_______ 。
(3)从环境保护的角度思考,下列燃料中最理想的是______ (填序号)。
(4)下列关于能源与环境说法正确的是________(填序号)。
(1)目前使用的煤、石油、天然气均为
(2)我国海域可燃冰资源丰富,写出可燃冰中甲烷燃烧的化学方程式
(3)从环境保护的角度思考,下列燃料中最理想的是______ (填序号)。
| A.氢气 | B.天然气 | C.酒精 | D.汽油 |
| A.为治理雾霾,应禁止使用煤 | B.城市道路使用太阳能景观灯,节能又环保 |
| C.发展新能源汽车,有利于缓解温室效应 | |
您最近一年使用:0次
【推荐2】2020年世界环境日中国的主题是“绿水青山就是金山银山”
(1)减少污染物排放—空气清新
引起酸雨的主要物质是_________ ,低碳生活可以减缓________ 引起的温室效应。
(2)自来水来之不易—节约用水
自来水生产流程:天然水 沉降→过滤→吸附
沉降→过滤→吸附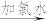 自来水
自来水
通常加入__________ 吸附水中的异味和色素,氯气的作用是________ 。
(3)清洁高效能源—天然气
天然气的主要成分是_______ (化学式),燃烧的化学方程式是_________ 。
(1)减少污染物排放—空气清新
引起酸雨的主要物质是
(2)自来水来之不易—节约用水
自来水生产流程:天然水
 沉降→过滤→吸附
沉降→过滤→吸附 自来水
自来水通常加入
(3)清洁高效能源—天然气
天然气的主要成分是
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐3】2021年3月政府工作报告提出要扎实做好碳达峰、碳中和各项工作。“中国将力争碳排放于2030年前达到峰值,争取在2060年前实现碳中和。”在降低“碳排放”过程中,化学起着不可替代的作用。
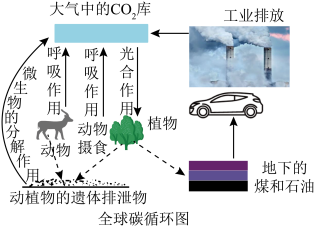
(1)实现“碳中和”,需要通过能源结构的调整和替代实现。
①能源的清洁低碳化,页岩气是蕴藏于页岩层可供开采的天然气资源,其成分以甲烷为主,是一种清洁、高效的能源资源,请写出甲烷在空气中完全燃烧的化学方程式______ 。
②完善能源双控制度,构建以新能源为主体的新型电力系统。下列选项中,不属于新能源的是______ (填序号)。
A.氢能 B.风能 C.太阳能 D.石油
(2)在全球碳循环图中,能消耗CO2的途径是______ ,化石燃料燃烧会产生CO2,因为化石燃料中含有______ 元素。
(3)利用庞大的水体使海洋成为封存CO2的容器,但会引起海水______ 。
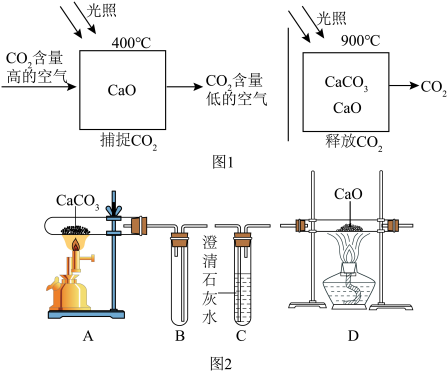
(4)实现碳达峰,碳中和是一场硬仗,科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(上图1所示)。某化学小组的同学对此非常感兴趣,在老师指导下,设计如图2装置探究上述设想的反应原理。
①能证明装置A“释放CO2”的现象是______ 。
②装置B在实验结束撤掉酒精喷灯时的作用是______ 。
③实验后小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
Ⅰ、甲同学取样D中固体于试管中,加入一定量的水,振荡,有白色不溶物,甲同学认为试管中的固体为碳酸钙。乙同学认为上述实验不足以证明D中固体为碳酸钙,其理由是______ 。
Ⅱ、乙同学取样D中固体于试管中,加入少量的水,触摸试管外壁感觉______ ,认为固体中肯定有氧化钙,但无法确定是否有碳酸钙。
Ⅲ、丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,丙同学将甲、乙两同学的试管内物质混合后过滤,向滤液中滴入酚酞,向滤渣中加入盐酸。根据______ 现象,得出D固体中含有氧化钙和碳酸钙。


(1)实现“碳中和”,需要通过能源结构的调整和替代实现。
①能源的清洁低碳化,页岩气是蕴藏于页岩层可供开采的天然气资源,其成分以甲烷为主,是一种清洁、高效的能源资源,请写出甲烷在空气中完全燃烧的化学方程式
②完善能源双控制度,构建以新能源为主体的新型电力系统。下列选项中,不属于新能源的是
A.氢能 B.风能 C.太阳能 D.石油
(2)在全球碳循环图中,能消耗CO2的途径是
(3)利用庞大的水体使海洋成为封存CO2的容器,但会引起海水
(4)实现碳达峰,碳中和是一场硬仗,科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(上图1所示)。某化学小组的同学对此非常感兴趣,在老师指导下,设计如图2装置探究上述设想的反应原理。
①能证明装置A“释放CO2”的现象是
②装置B在实验结束撤掉酒精喷灯时的作用是
③实验后小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
Ⅰ、甲同学取样D中固体于试管中,加入一定量的水,振荡,有白色不溶物,甲同学认为试管中的固体为碳酸钙。乙同学认为上述实验不足以证明D中固体为碳酸钙,其理由是
Ⅱ、乙同学取样D中固体于试管中,加入少量的水,触摸试管外壁感觉
Ⅲ、丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,丙同学将甲、乙两同学的试管内物质混合后过滤,向滤液中滴入酚酞,向滤渣中加入盐酸。根据
您最近一年使用:0次
【推荐1】氯化钠在工业、农业、生活和医疗等方面有着广泛的用途。
(1)医疗上将溶质质量分数为0.9%的NaC1溶液用作生理盐水,生理盐水中氯化钠的存在形式是______ (填化学符号)。
(2)已知饱和氯化钠溶液在通电条件下反应生成一种碱、一种密度最小的气体和相对分子质量为71的气体,请写出该反应的化学方程式:______ 。
(3)欲配制100g质量分数为10%的氯化钠溶液。必须要用到的仪器组合是______。
①托盘天平②烧杯③玻璃棒入④100mL量筒
(4)为了除去NaCl溶液中少量的Na2SO4、CaCl2、MgCl2等可溶性杂质,某化学小组选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示实验。

①该实验过程中发生复分解反应的个数为______ 。
②向滤液B中滴入适量Z的作用是什么?______ 。
③用实际参加反应的离子符号来表示反应的式子叫作离子方程式。请用离子方程式表示加入过量试剂X发生的反应的实质______ 。(任写一个)
④将50g碳酸钠溶液加入50g稀盐酸中,两者恰好完全反应,反应后所得溶液的质量为97.8g,请计算反应生成氯化钠的质量______ 。
(1)医疗上将溶质质量分数为0.9%的NaC1溶液用作生理盐水,生理盐水中氯化钠的存在形式是
(2)已知饱和氯化钠溶液在通电条件下反应生成一种碱、一种密度最小的气体和相对分子质量为71的气体,请写出该反应的化学方程式:
(3)欲配制100g质量分数为10%的氯化钠溶液。必须要用到的仪器组合是______。
①托盘天平②烧杯③玻璃棒入④100mL量筒
| A.①② | B.①④ | C.①②③ | D.①②③④ |

①该实验过程中发生复分解反应的个数为
②向滤液B中滴入适量Z的作用是什么?
③用实际参加反应的离子符号来表示反应的式子叫作离子方程式。请用离子方程式表示加入过量试剂X发生的反应的实质
④将50g碳酸钠溶液加入50g稀盐酸中,两者恰好完全反应,反应后所得溶液的质量为97.8g,请计算反应生成氯化钠的质量
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐2】酸、碱、盐在生产、生活中发挥着重要作用。请回答下列问题。
(1)胃液可以帮助消化的主要成分的化学式是_______ 。
(2)氢氧化钠和氢氧化钙具有相似的化学性质,是因为它们在溶液中都能解离出_______(填字母序号)。
(3)某化学小组利用数字化设备,测定氢氧化钠溶液与稀硫酸反应时溶液pH的变化,实验结果如图所示。

①写出实验中发生化学方程式为_______ 。
②区分x点和y点所对应溶液,可选用的一种试剂为_______ 。
(4)我国海水晒盐的历史悠久。某化学兴趣小组称取一定质量粗盐样品(粗盐中含有可溶性杂质MgCl2、CaCl2、Na2SO4和泥沙等杂质),进行如图提纯操作。
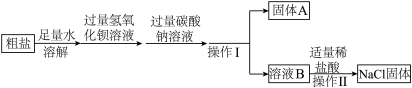
①请写出加入氢氧化钡溶液时发生反应的化学方程式____ 。(写出1个即可)
②如何验证溶液B中杂质的成分?____ (写出实验步骤和现象)
③根据流程分析“操作Ⅱ”的名称____ 。
(5)将50g碳酸钠溶液加入50g稀盐酸中,两者恰好完全反应,反应后所得溶液的质量为97.8g,请计算反应生成氯化钠的质量。
(1)胃液可以帮助消化的主要成分的化学式是
(2)氢氧化钠和氢氧化钙具有相似的化学性质,是因为它们在溶液中都能解离出_______(填字母序号)。
| A.水分子 | B.氢离子 |
| C.酸根离子 | D.氢氧根离子 |
(3)某化学小组利用数字化设备,测定氢氧化钠溶液与稀硫酸反应时溶液pH的变化,实验结果如图所示。

①写出实验中发生化学方程式为
②区分x点和y点所对应溶液,可选用的一种试剂为
(4)我国海水晒盐的历史悠久。某化学兴趣小组称取一定质量粗盐样品(粗盐中含有可溶性杂质MgCl2、CaCl2、Na2SO4和泥沙等杂质),进行如图提纯操作。

①请写出加入氢氧化钡溶液时发生反应的化学方程式
②如何验证溶液B中杂质的成分?
③根据流程分析“操作Ⅱ”的名称
(5)将50g碳酸钠溶液加入50g稀盐酸中,两者恰好完全反应,反应后所得溶液的质量为97.8g,请计算反应生成氯化钠的质量。
您最近一年使用:0次
【推荐3】生活中常见物质的性质、制法、用途等是化学研究的重要内容,请回答以下问题。
(1)下面是实验室制取气体的常用装置:
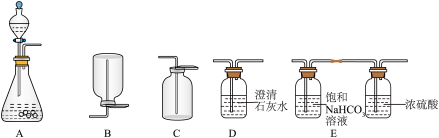
①实验室制取二氧化碳的化学方程式为______ 。
②若要制取并收集一瓶干燥纯净的二氧化碳,所选装置正确的连接顺序是______ →______ →______ 。
③装置D用于检验二氧化碳气体的原理是______ (用化学方程式表示)。
(2)为除去粗盐中的泥沙和CaCl2、MgSO4杂质某化学兴趣小组的同学先将粗盐样品溶解、过滤除去泥沙后,取粗盐水按以下流程进行实验探究。

①以上操作中所发生的复分解反应共有______ 个。
②写出一个操作过程中使氯化钠质量增加的化学方程式______ 。
(3)碳酸氢钠常用于焙制糕点。碳酸氢钠受热分解会生成水、二氧化碳和一种白色固体。
①对于白色固体的成分,有下列猜想:
Ⅰ、氢氧化钠; Ⅱ、碳酸钠; Ⅲ、氢氧化钠和碳酸钠的混合物。
请设计实验方案证明猜想Ⅱ正确,其余猜想不正确,简要写出所用试剂、实验步骤、现象和结论______ 。
②写出碳酸氢钠受热分解的化学方程式______ 。
(4)某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液8g,洗涤后的溶液pH=7。这一定量石油产品中含H2SO4的质量是多少?______
(1)下面是实验室制取气体的常用装置:

①实验室制取二氧化碳的化学方程式为
②若要制取并收集一瓶干燥纯净的二氧化碳,所选装置正确的连接顺序是
③装置D用于检验二氧化碳气体的原理是
(2)为除去粗盐中的泥沙和CaCl2、MgSO4杂质某化学兴趣小组的同学先将粗盐样品溶解、过滤除去泥沙后,取粗盐水按以下流程进行实验探究。

①以上操作中所发生的复分解反应共有
②写出一个操作过程中使氯化钠质量增加的化学方程式
(3)碳酸氢钠常用于焙制糕点。碳酸氢钠受热分解会生成水、二氧化碳和一种白色固体。
①对于白色固体的成分,有下列猜想:
Ⅰ、氢氧化钠; Ⅱ、碳酸钠; Ⅲ、氢氧化钠和碳酸钠的混合物。
请设计实验方案证明猜想Ⅱ正确,其余猜想不正确,简要写出所用试剂、实验步骤、现象和结论
②写出碳酸氢钠受热分解的化学方程式
(4)某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液8g,洗涤后的溶液pH=7。这一定量石油产品中含H2SO4的质量是多少?
您最近一年使用:0次



