某小组用稀硫酸测定粗锌中锌的质量分数(杂质不参加反应)。将稀硫酸分二次加入电子天平上盛有粗锌的烧杯(烧杯质量105.6g)中,实验数据如下表:
请计算:
(1)生成氢气的总质量为___________ g。
(2)粗锌中锌的质量分数。
| 反应前 | 第一次 | 第二次 | |
| 加入稀硫酸质量/g | 0 | 100 | 100 |
| 天平示数/g | 115.6 | 215.4 | 315.4 |
(1)生成氢气的总质量为
(2)粗锌中锌的质量分数。
更新时间:2024-05-24 23:59:42
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】某样品由氧化铜和铜组成。甲同学取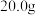 固体混合物置于烧杯中,将
固体混合物置于烧杯中,将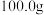 稀硫酸分为四等份依次加入其中进行实验,测得数据如表:
稀硫酸分为四等份依次加入其中进行实验,测得数据如表:
请计算:
(1)表中a的值为___________ 。
(2)计算所用稀硫酸的溶质质量分数。(写出计算过程,结果精确到 )
)
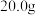 固体混合物置于烧杯中,将
固体混合物置于烧杯中,将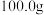 稀硫酸分为四等份依次加入其中进行实验,测得数据如表:
稀硫酸分为四等份依次加入其中进行实验,测得数据如表:| 次序 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀硫酸的质量 | 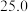 | 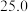 | 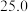 | 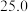 |
剩余固体的质量 | 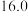 |  |  |  |
(1)表中a的值为
(2)计算所用稀硫酸的溶质质量分数。(写出计算过程,结果精确到
 )
)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】实验室用过氧化氢溶液制取氧气,某化学探究小组将气体制备装置于电子天平上进行相关的实验,测得数据如下:
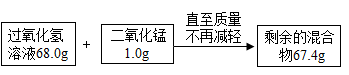
(1)当反应结束后,过滤,洗涤并烘干滤渣,称得滤渣的质量为___________ g。
(2)根据质量守恒定律,反应生成氧气的质量为___________ g。
(3)过氧化氢的质量分数是多少?(过氧化氢质量占过氧化氢溶液质量的百分比)

(1)当反应结束后,过滤,洗涤并烘干滤渣,称得滤渣的质量为
(2)根据质量守恒定律,反应生成氧气的质量为
(3)过氧化氢的质量分数是多少?(过氧化氢质量占过氧化氢溶液质量的百分比)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】海南四周环海,海洋资源极为丰富,从海水中提取镁的第一步反应的化学方程式为
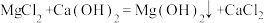 。现有海水样品(含 NaCl、MgCl2、CaCl2)400g,加入足量澄清石灰水,充分反应后得沉淀1.16g,求海水中MgCl2 的质量分数。
。现有海水样品(含 NaCl、MgCl2、CaCl2)400g,加入足量澄清石灰水,充分反应后得沉淀1.16g,求海水中MgCl2 的质量分数。
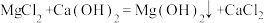 。现有海水样品(含 NaCl、MgCl2、CaCl2)400g,加入足量澄清石灰水,充分反应后得沉淀1.16g,求海水中MgCl2 的质量分数。
。现有海水样品(含 NaCl、MgCl2、CaCl2)400g,加入足量澄清石灰水,充分反应后得沉淀1.16g,求海水中MgCl2 的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组的同学要探究黄铜(铜和锌的合金)中铜的质量分数,进行了如下实验:
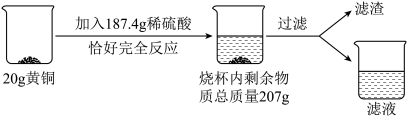
(1)生成氢气的质量为______ g,黄铜中铜的质量分数为______ 。
(2)过滤后所得滤液中溶质的质量分数。(请写出计算过程,计算结果精确到0.1%)

(1)生成氢气的质量为
(2)过滤后所得滤液中溶质的质量分数。(请写出计算过程,计算结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】农业的发展离不开化肥,某同学用某品牌的硝酸钙化肥进行如下实验:取9g化肥样品溶解于盛有41g蒸馏水的烧杯中,向其中加入Na2CO3溶液,充分反应至不再产生沉淀,消耗Na2CO3溶液的质量为80g,过滤,称得滤液的质量为126g。该过程中发生的反应为:Ca(NO3)2+ Na2CO3=CaCO3↓+2NaNO3。(化肥中其他成分易溶于水,且不会与碳酸钠发生反应)
请完成下列分析及计算:
(1)硝酸钙属于______ (填“氮”“磷”或“钾”)肥。
(2)生成沉淀的质量为______ g。
(3)该化肥样品中硝酸钙的质量分数。(计算结果保留至0.1%)
请完成下列分析及计算:
(1)硝酸钙属于
(2)生成沉淀的质量为
(3)该化肥样品中硝酸钙的质量分数。(计算结果保留至0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将8.7克未打磨的铝片放入足量稀盐酸中,完全反应后收集到氢气质量如图所示,回答下列问题:
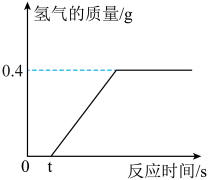
(1)0~t时刻没有产生气体的原因是_________ 。
(2)求该铝片中铝元素的质量。

(1)0~t时刻没有产生气体的原因是
(2)求该铝片中铝元素的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金。为了测定某黄铜中铜的质量分数,称取10.0g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时共用去49.0g稀硫酸,过滤后烘干称量还剩余固体3.5g。试计算:
(1)该黄铜中锌的质量多少克。
(2)生成氢气的质量多少克。
(1)该黄铜中锌的质量多少克。
(2)生成氢气的质量多少克。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】硅钢是变压器、充电器中的核心材料,其主要成份是Fe和Si。某学生用硅钢样品做了如下实验:取2.8g硅钢样品,将40g稀硫酸分4次加入样品中(其中稀硫酸与硅及其它杂质不反应),充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)从以上数据可知,稀硫酸加入第__________ 次充分反应后,铁恰好完全反应。
(2)表格中M=___________ 。
(3)计算所用稀硫酸中溶质的质量分数_____ 。
| 实验次数 | 一 | 二 | 三 | 四 |
| 稀硫酸的用量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | M | 1.4 | 0.7 | 0.7 |
(1)从以上数据可知,稀硫酸加入第
(2)表格中M=
(3)计算所用稀硫酸中溶质的质量分数
您最近一年使用:0次



