实验中学化学兴趣小组为了测定某含铁样品中铁的质量分数,取10克样品放入烧杯中,再取稀盐酸分五次加入烧杯中,每次均充分反应(杂质不溶于水,也不参加反应),测得实验数据如下:
求:
(1)此含铁样品中铁的质量分数________ 。
(2)恰好完全反应时所得溶液中溶质的质量分数________ 。
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 加入稀盐酸的质量(g) | 23.6 | 23.6 | 23.6 | 23.6 | 23.6 |
| 剩余固体的质量(g) | 8.6 | 7.2 | 5.8 | 4.4 | 4.4 |
(1)此含铁样品中铁的质量分数
(2)恰好完全反应时所得溶液中溶质的质量分数
更新时间:2016-11-28 12:42:48
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:

(1)产生二氧化碳的质量为_____。
(2)B点所对的溶液中的溶质是_____。
(3)求试样中碳酸钠的质量分数_____(写出计算过程,结果精确到0.1%)。

(1)产生二氧化碳的质量为_____。
(2)B点所对的溶液中的溶质是_____。
(3)求试样中碳酸钠的质量分数_____(写出计算过程,结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】铝不仅能与酸反应,还能与强碱反应(如 ),而铜不能与强碱反应。某种铝制品的主要成分是金属铝和铜,同学们将180 gNaOH溶液不断加到40g铝制品中,充分反应后,得到如下实验数据:
),而铜不能与强碱反应。某种铝制品的主要成分是金属铝和铜,同学们将180 gNaOH溶液不断加到40g铝制品中,充分反应后,得到如下实验数据:
(1)40g铝制品中含有__________ g金属铜。
(2)求所用NaOH溶液的溶质质量分数。(写出计算过程)
 ),而铜不能与强碱反应。某种铝制品的主要成分是金属铝和铜,同学们将180 gNaOH溶液不断加到40g铝制品中,充分反应后,得到如下实验数据:
),而铜不能与强碱反应。某种铝制品的主要成分是金属铝和铜,同学们将180 gNaOH溶液不断加到40g铝制品中,充分反应后,得到如下实验数据:第1次 | 第2次 | 第3次 | 第4次 | |
加入NaOH溶液的质量/g | 45 | 45 | 45 | 45 |
剩余固体的质量g | 28 | 16 | 4 | 4 |
(1)40g铝制品中含有
(2)求所用NaOH溶液的溶质质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】向 20g 铜锌合金中不断加入一定溶质质量分数的稀盐酸,加入稀盐酸的质量与固体质量的关系如图所示。请计算:
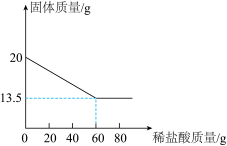
(1)反应属于的基本反应类型为______。
(2)合金中锌的质量分数为多少。(写计算结果)
(3)所用稀盐酸的溶质质量分数。(计算结果保留一位小数)

(1)反应属于的基本反应类型为______。
(2)合金中锌的质量分数为多少。(写计算结果)
(3)所用稀盐酸的溶质质量分数。(计算结果保留一位小数)
您最近一年使用:0次
计算题
|
适中
(0.65)
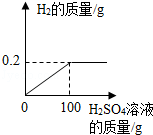
【推荐2】黄铜是一种重要的金属材料,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
按要求回答下列问题:
(1)根据实验数据分析,从第________ 份开始,金属已经反应完全了.
(2)列式计算该黄铜样品中金属锌的质量分数________ .(要求写出计算过程)
(3)在给出的坐标纸上,画出40.0g样品中加稀硫酸的质量与产生气体质量的关系曲线.________ 
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
| 取样品质量/g | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
| 取稀硫酸质量/g | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
| 产生气体质量/g | 0.3 | 0.6 | 0.9 | 1.0 | 1.0 |
(1)根据实验数据分析,从第
(2)列式计算该黄铜样品中金属锌的质量分数
(3)在给出的坐标纸上,画出40.0g样品中加稀硫酸的质量与产生气体质量的关系曲线.

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】小华同学为测定某稀盐酸中溶质的质量分数,在烧杯里放入一定质量的大理石,然后分次加入该稀盐酸,充分反应后测得生成二氧化碳的质量如下表所示
(1)两次加稀盐酸后,生成二氧化碳的总质量是______ 。
(2)该稀盐酸中溶质的质量分数。
| 加盐酸的次数 | 第一次 | 第二次 |
| 加盐酸的质量/g | 100 | 100 |
| 生成二氧化碳的质量/g | 4.4 | 2.2 |
(2)该稀盐酸中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室里现有一包氯化镁和氯化钠的固体混合物样品,某同学取该样品12.8 g,使之完全溶解在50 g水中,再向其中加入40 g20%的氢氧化钠溶液,恰好完全反应。求:
(1)样品中氯化镁的质量。
(1)反应后所得溶液中氯化钠的质量分数。(保留到小数点后一位数字)
(1)样品中氯化镁的质量。
(1)反应后所得溶液中氯化钠的质量分数。(保留到小数点后一位数字)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某山区盛产石灰石,其中含有的杂质为二氧化硅(不溶于水、高温下难以分解的酸性氧化物).S中学初三化学研究性学习小组的同学为了测定某矿山石灰石的纯度,取2.0g该矿山石灰石样品,将20.0g盐酸平均分成4份,分4次加入到样品中,充分反应后测定剩余固体的质量,数据见表.试求:
(1)2.0g石灰石样品中杂质的质量______g。
(2)加入的盐酸中溶质的质量分数是______?
| 次数 | 1 | 2 | 3 | 4 |
| 加入盐酸质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固体质量/g | 1.3 | 0.6 | 0.2 | 0.2 |
(1)2.0g石灰石样品中杂质的质量______g。
(2)加入的盐酸中溶质的质量分数是______?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】计算
(1)要使CO与CO2中含有等质量的氧元素,则需要CO与CO2的质量比为___________ 。26.国家质量标准规定市售尿素的含量在96%以上为达标一级产品。现某化工集团公司生产的尿素外包装标签如图所示。
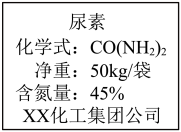
(2)尿素的化学式量为___________ 。
(3)该公司生产的市售尿素是___________ (填“纯净物或混合物”)。
(4)通过计算说明,该尿素是否可以按一级品出售?
(1)要使CO与CO2中含有等质量的氧元素,则需要CO与CO2的质量比为

(2)尿素的化学式量为
(3)该公司生产的市售尿素是
(4)通过计算说明,该尿素是否可以按一级品出售?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计)。为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸。当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示。试计算:_______ 。
(2)试样中碳酸钠的质量分数_______ (结果精确至0.1%)。

(2)试样中碳酸钠的质量分数
您最近一年使用:0次