现有一瓶久置的标有质量分数为10%的NaOH溶液样品,为探究其变质(NaOH易和空气中的CO2反应生成Na2CO3)的相关问题,利用U形管设计如下图所示的装置进行实验。

(1)如图甲所示,若此溶液变质,分别在U形管的两端滴入HCl溶液和澄清的石灰水时,观察到的现象:a端_____________________,b端___________________。
(2)如图乙所示,取此NaOH样品溶液20g放于U形管中,并在其中加入适量的酚酞试液,通过分液漏斗向U形管中滴入HCl溶液,当滴入20gHCl溶液时,恰好反应完全。
①滴入稀盐酸过程中,U形管中的溶液颜色变化为______________________________。
②恰好完全反应时,生产气体0.22g,试计算该溶液中Na2CO3的质量分数。

(1)如图甲所示,若此溶液变质,分别在U形管的两端滴入HCl溶液和澄清的石灰水时,观察到的现象:a端_____________________,b端___________________。
(2)如图乙所示,取此NaOH样品溶液20g放于U形管中,并在其中加入适量的酚酞试液,通过分液漏斗向U形管中滴入HCl溶液,当滴入20gHCl溶液时,恰好反应完全。
①滴入稀盐酸过程中,U形管中的溶液颜色变化为______________________________。
②恰好完全反应时,生产气体0.22g,试计算该溶液中Na2CO3的质量分数。
更新时间:2016-11-28 12:59:02
|
相似题推荐
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】振衡中学校办工厂利用熟石灰与纯碱反应生产工业烧碱,学校化学兴趣小组到校办工厂检验刚生产出的一批产品的纯度(氢氧化钠的质量分数).检验时称取样品20.00g,溶于100.00g水中。向其中逐滴加入氢氧化钡[(Ba(OH)2)]溶液,当恰好不再产生沉淀(BaCO3)时,用去溶质的质量分数为10.0%的氢氧化钡溶液8.55g,试求:
(1)反应中生成的碳酸钡的质量(保留2位小数)。
(2)该批产品中氢氧化钠的质量分数(精确到0.1% )。
(3)反应后所得溶液中氢氧化钠的质量分数(精确到0.1% )。
(1)反应中生成的碳酸钡的质量(保留2位小数)。
(2)该批产品中氢氧化钠的质量分数(精确到0.1% )。
(3)反应后所得溶液中氢氧化钠的质量分数(精确到0.1% )。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】氯酸钾(KClO3)在二氧化锰(MnO2)作催化剂并加热的条件下能较快地分解生成氯化钾和氧气,若12.25g氯酸钾与2g二氧化锰混合加热到质量不再变化时为止,请你通过化学方程式计算能产生氧气多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】为了测定贝壳中碳酸钙的质量分数,取贝壳25g,加入200g的稀盐酸,恰好完全反应,称得反应后物质的总质量为216.2g (假设贝壳中其它物质不与盐酸反应且不溶于水)。请你计算:
(1)贝壳中碳酸钙的质量分数;
(2)反应后所得溶液中溶质的质量分数(精确到0.1%)。
(1)贝壳中碳酸钙的质量分数;
(2)反应后所得溶液中溶质的质量分数(精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某活动小组对失去标签的稀硫酸溶液的浓度进行测定:取稀硫酸50g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如下图所示。
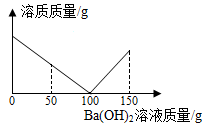
(1)参加反应的Ba(OH)2溶质质量共有______ g。
(2)滴加Ba(OH)2至50g时,烧杯内溶液的pH______ 7(填“>”、“<”或“=”)。
(3)求该硫酸溶液的溶质质量分数?(写出计算过程,结果精确到0.01%)。

(1)参加反应的Ba(OH)2溶质质量共有
(2)滴加Ba(OH)2至50g时,烧杯内溶液的pH
(3)求该硫酸溶液的溶质质量分数?(写出计算过程,结果精确到0.01%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】兴趣小组的同学向含4 g NaOH的溶液中加入10%的盐酸,进行中和反应探究。
(1)计算恰好完全反应所需盐酸的质量。
(2)向NaOH溶液中滴几滴酚酞溶液,再逐滴加入稀盐酸至变成无色,此时溶液一定显中性吗?请判断并解释_______________ 。
(1)计算恰好完全反应所需盐酸的质量。
(2)向NaOH溶液中滴几滴酚酞溶液,再逐滴加入稀盐酸至变成无色,此时溶液一定显中性吗?请判断并解释
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数。现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液加入,溶液的pH的变化如图所示。试回答:

(1)A点溶液中含有的离子有_________ 。
(2)当pH=7时,消耗NaOH溶液中溶质的质量为________ 。
(3)当加入NaOH溶液质量超过40g时,取出试剂少许于试管中,并滴入酚酞试剂,此时溶液将呈______ 色。
(4)计算恰好完全反应时溶质质量分数_____ 。(写出计算过程,结果精确到0.1%)。

(1)A点溶液中含有的离子有
(2)当pH=7时,消耗NaOH溶液中溶质的质量为
(3)当加入NaOH溶液质量超过40g时,取出试剂少许于试管中,并滴入酚酞试剂,此时溶液将呈
(4)计算恰好完全反应时溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数.现取10g稀硫酸样品,将5%的NaOH溶液逐滴加到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示.试回答:

(1)取a点溶液,滴加石蕊试液,现象是 1
(2)当两者恰好反应时,消耗NaOH溶液中的NaOH的质量为 2 g.
(3)计算稀H2SO4的溶质质量分数 3 (写出解题过程)

(1)取a点溶液,滴加石蕊试液,现象是
(2)当两者恰好反应时,消耗NaOH溶液中的NaOH的质量为
(3)计算稀H2SO4的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐1】实验室有一瓶长期存放的固体氢氧化钠,由于保管不当已经变质.某兴趣小组的同学欲通过实验测定其变质的情况.实验过程如下,取样品25g放入烧杯中,向其中加入280g过量的稀盐酸,得到296.2g溶液.试计算25g样品中碳酸钠的质量.
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】丁强同学想利用化学反应: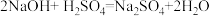 来测定一瓶NaoH溶液的质量分数。他取100g该溶液于烧杯中,滴入几滴酚酞溶液,然后逐滴加入稀硫酸并不断搅拌,直到溶液由红色刚刚变成无色。(已知消耗稀硫酸中溶质——纯硫酸的质量为9.8g)
来测定一瓶NaoH溶液的质量分数。他取100g该溶液于烧杯中,滴入几滴酚酞溶液,然后逐滴加入稀硫酸并不断搅拌,直到溶液由红色刚刚变成无色。(已知消耗稀硫酸中溶质——纯硫酸的质量为9.8g)
(1)理论计算:该瓶NaOH溶液的质量分数是多少?【不考虑(2)中因素的影响】
(2)实验分析:细心的丁强发现实验过程中溶液中有少量的气泡出现,请你帮他分析产生气泡的原因是___________ 。若要证明你的分析正确,可取少量该NaOH溶液于试管中,再加入适量的___________ ,观察到有白色沉淀生成即可。
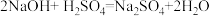 来测定一瓶NaoH溶液的质量分数。他取100g该溶液于烧杯中,滴入几滴酚酞溶液,然后逐滴加入稀硫酸并不断搅拌,直到溶液由红色刚刚变成无色。(已知消耗稀硫酸中溶质——纯硫酸的质量为9.8g)
来测定一瓶NaoH溶液的质量分数。他取100g该溶液于烧杯中,滴入几滴酚酞溶液,然后逐滴加入稀硫酸并不断搅拌,直到溶液由红色刚刚变成无色。(已知消耗稀硫酸中溶质——纯硫酸的质量为9.8g)(1)理论计算:该瓶NaOH溶液的质量分数是多少?【不考虑(2)中因素的影响】
(2)实验分析:细心的丁强发现实验过程中溶液中有少量的气泡出现,请你帮他分析产生气泡的原因是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】下图是某省生产的某种加钙食盐包装标签上的部分文字。请仔细阅读后完成以下问题:
(1)包装标签上钙含量是指____________ (填“单质钙”“碳酸钙”或“钙元素”中)。
(2)为了检验此盐中是否含有碳酸钙,在家庭厨房里可选用的物质是____________ 。
(3)为了测定此盐中的钙元素含量,取10 g这种盐溶于水,加入足量盐酸,生成0.132 g二氧化碳。请计算此加钙食盐中钙元素的质量分数____________ 。
| 配料表:氯化钠、食用碳酸钙、碘酸钾 净含量:500 g 成分表:氯化钠≥88% 钙(以Ca计)(0.5—1.3)% 碘(以I计)(20—50) mg/ kg |
(2)为了检验此盐中是否含有碳酸钙,在家庭厨房里可选用的物质是
(3)为了测定此盐中的钙元素含量,取10 g这种盐溶于水,加入足量盐酸,生成0.132 g二氧化碳。请计算此加钙食盐中钙元素的质量分数
您最近一年使用:0次

 ,生成强碱KOH从而去油污。现有50gK2CO3溶液样品,为测定其溶质质量分数,向其中加入足量Ca(OH)2溶液,生成了5g沉淀。请计算K2CO3溶液样品的溶质质量分数。
,生成强碱KOH从而去油污。现有50gK2CO3溶液样品,为测定其溶质质量分数,向其中加入足量Ca(OH)2溶液,生成了5g沉淀。请计算K2CO3溶液样品的溶质质量分数。


