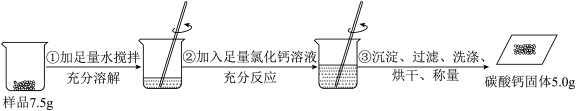
某碳酸钠样品中混有少量氯化钠,根据如图所示信息计算该样品中碳酸钠的质量分数。(计算结果精确到0.1%)(反应的化学方程式:CaCl2+Na2CO3===CaCO3↓+2NaCl)

2015·福建·中考真题 查看更多[12]
2015年初中毕业升学考试(福建卷)化学鲁教版2018届九年级下册化学同步练习:第八单元 第三节 海水“制碱”1湖北省黄冈外校2019届九年级下学期中考一模考试化学试题广东省揭阳市揭西县2019-2020学年九年级上学期期末化学试题2020年河北省中考模拟化学试题(已下线)【万唯原创】2016年河北省中考化学面对面卷九年级热点题型突破题型七(已下线)【万唯原创】2016年陕西省中考化学面对面卷(科广版)讲解册热点题型突破-题型七(已下线)【万唯原创】2016年陕西省中考化学面对面卷(鲁教版)讲解册九年级热点题型突破题型七(已下线)【万唯原创】2016年山西省中考化学面对面卷九年级讲解册重点专题攻略专题七(已下线)【万唯原创】2016年山西省中考化学试题研究卷模块一第11讲(已下线)课题5.3.2 利用化学方程式的简单计算-2021-2022学年九年级化学上册同步分层作业(人教版)2017年福建省南平市邵武市初中毕业班适应性检测化学试题
更新时间:2016-11-28 13:00:59
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】为测定某CuSO4溶液的溶质质量分数,某化学小组的同学取CuSO4溶液100g,向其中滴加一定浓度的NaOH溶液,可观察到产生蓝色沉淀,至两者恰好完全反应时,共用去NaOH溶液80g,过滤,得到滤液175.1g。请计算:
(1)该反应生成Cu(OH)2沉淀_____g;
(2)该CuSO4溶液中溶质的质量分数____。
温馨提示:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
(1)该反应生成Cu(OH)2沉淀_____g;
(2)该CuSO4溶液中溶质的质量分数____。
温馨提示:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】含有少量的氯化钠,某同学为测定该纯碱样品中,取15g样品,全部溶解在100g水中,再加入217g氯化钙溶液。恰好完全反应,过滤干燥,得到10g沉淀。计算:
(1)纯碱样品中碳酸钠的质量;
(2)所加氯化钙溶液中溶质的质量分数(计算结果保留到0.1%);
(3)反应后所得溶液中溶质的质量分数。
(1)纯碱样品中碳酸钠的质量;
(2)所加氯化钙溶液中溶质的质量分数(计算结果保留到0.1%);
(3)反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某食用碱的主要成分是Na2CO3,其中含有少量的NaCl,小明同学为测定该食用碱中Na2CO3的质量分数,他进行了以下实验,取40 g食用碱,加水配成400g的溶液,把溶液平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
请分析表中数据并计算回答。
(1)m=________ ;
(2)40 g该食用碱配成的溶液与足量CaCl2溶液反应,最多生成沉淀质量为多少;
(3)该食用碱中Na2CO3的质量分数是?(写出计算过程,答案精确到0.1%)
(4)请根据实验四的数据画图并标上合适的坐标。

| 实验一 | 实验二 | 实验三 | 实验四 | |
| 食用碱溶液的质量 | 100g | 100g | 100g | 100g |
| 加入CaCl2溶液的质量 | 20g | 40g | 60g | 80g |
| 生成沉淀的质量 | 2.5g | 5g | m | 8g |
请分析表中数据并计算回答。
(1)m=
(2)40 g该食用碱配成的溶液与足量CaCl2溶液反应,最多生成沉淀质量为多少;
(3)该食用碱中Na2CO3的质量分数是?(写出计算过程,答案精确到0.1%)
(4)请根据实验四的数据画图并标上合适的坐标。

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】小红利用如图所示的实验来验证质量守恒定律,她将反应装置放在天平左盘,使天平横梁水平平衡后,再将碳酸钠粉末倒入锥形瓶中。
(2)反应结束后,气球鼓起,天平向右倾斜。小红按规范操作重新进行实验,得到相同的结果。请你帮她分析原因:_______ 。

(2)反应结束后,气球鼓起,天平向右倾斜。小红按规范操作重新进行实验,得到相同的结果。请你帮她分析原因:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液50g装入烧杯中,每次滴加50g稀盐酸充分反应。测得部分数据及图像如下:

请根据有关信息计算:
(1)a的数值为______ 。
(2)第2次充分反应后,溶液中的溶质为______ 。
(3)计算稀盐酸中溶质质量分数是多少?(写出计算过程)
次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸的质量/g | 50 | 50 | 50 | 50 | 50 |
烧杯中物质的质量/g | 100 | 150 | 197.8 | 245.6 | 295.6 |

请根据有关信息计算:
(1)a的数值为
(2)第2次充分反应后,溶液中的溶质为
(3)计算稀盐酸中溶质质量分数是多少?(写出计算过程)
您最近一年使用:0次



