用化学符号和数字填空:
(1)两个氢氧根离子__________ 。
(2)可用作补钙剂的盐______________ 。
(3)草木灰是农家肥料,它的主要成分是一种含钾的盐。取一些草木灰加入盐酸中,生成的气体可使澄清石灰水变浑浊,由此可推断草木灰的主要成分可能是___________ 。
(1)两个氢氧根离子
(2)可用作补钙剂的盐
(3)草木灰是农家肥料,它的主要成分是一种含钾的盐。取一些草木灰加入盐酸中,生成的气体可使澄清石灰水变浑浊,由此可推断草木灰的主要成分可能是
更新时间:2016-11-28 13:01:27
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】用化学用语(数字与符号)填空:
(1)三个磷原子____________ ;
(2)两个五氧化二氮分子______________ ;
(3)3个氢氧根离子___________________ ;
(4)地壳中含量最多的金属元素________ ;
(5)一种主要空气气体污染物__________ ;
(6)氧化镁中镁元素为+2价___________ .
(1)三个磷原子
(2)两个五氧化二氮分子
(3)3个氢氧根离子
(4)地壳中含量最多的金属元素
(5)一种主要空气气体污染物
(6)氧化镁中镁元素为+2价
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】请用适当的化学用语完成下列各题。
(1)两个氢原子__________ ;
(2)标出氧化镁中镁元素的化合价__________ ;
(3)地壳中含量最多的元素_________ ;
(4)氯化钠中的阳离子_________ 。
(1)两个氢原子
(2)标出氧化镁中镁元素的化合价
(3)地壳中含量最多的元素
(4)氯化钠中的阳离子
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐3】I.现有①氧气 ②氮气 ③二氧化硫 ④二氧化碳 ⑤氢气,请用上述物质的序号填空:
(1)动植物维持生命不可缺少的气体是_____ ,燃料燃烧也离不开它;
(2)_____ 是绿色植物光合作用的原料之一;
(3)_____ 是大气污染物之一,也是形成酸雨的主要原因;
(4)_____ 约占空气体积的78%,是工业上生产硝酸和化肥的重要原料。
(5)______ 可以作高能燃料,且燃烧无污染。
Ⅱ.根据下列要求用化学用语表示:
(6)2个钠原子_____ ;
(7)氦气_____ ;
(8)铵根离子_____ ;
(9)空气中含量最高的元素_____ :
(10)氧化铝中铝元素显+3价_____ 。
(1)动植物维持生命不可缺少的气体是
(2)
(3)
(4)
(5)
Ⅱ.根据下列要求用化学用语表示:
(6)2个钠原子
(7)氦气
(8)铵根离子
(9)空气中含量最高的元素
(10)氧化铝中铝元素显+3价
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
名校
解题方法
【推荐1】用化学用语填空。
(1)氧元素_______ 。
(2)两个氢分子_______ 。
(3)碳酸根离子_______ 。
(4)3个铁原子_______ 。
(5)氯化钾_______ 。
(1)氧元素
(2)两个氢分子
(3)碳酸根离子
(4)3个铁原子
(5)氯化钾
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】请在横线上用恰当的化学用语表示:
(1)3个氧原子__________ ;
(2)氮分子___________ ;
(3)氩原子的结构示意图___________ ;
(4)2个碳酸根离子___________ ;
(5)医用消毒酒精溶液中溶质的化学式是___________ 。
(1)3个氧原子
(2)氮分子
(3)氩原子的结构示意图
(4)2个碳酸根离子
(5)医用消毒酒精溶液中溶质的化学式是
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
解题方法
【推荐1】一种“氢氧化锶-氯化镁法”制备“牙膏用氯化锶(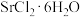 )”的工艺流程如图:
)”的工艺流程如图:
①欧锶的相关化合物(如SrO、SrCO3)的化学性质与相应的钙化合物类似,SrCO4、SrCO3不溶于水。
②SrCl2、MgCl2溶液皆为无色,呈中性。
(1)煅烧工业碳酸锶发生的反应与煅烧石灰石类似,则此过程的化学方程式为___________ 。
(2)“重结晶”是将蒸发结晶得到的无水氢氧化锶粗品溶于适量热水,趁热滤去未溶解的固体后,冷却结晶得到Sr(OH)2•8H2O。为探究蒸馏水用量对Sr(OH)2•8H2O纯度及产率的影响,设计一系列探究实验,结果如表所示。分析表格数据可知,最合适的实验条件为___________ (填序号),当蒸馏水用量大于该条件时,Sr(OH)2•8H2O产率减小,试推测其原因___________ 。
(3)步骤④中,为了保证氯化锶产出量,MgCl2溶液必须足量,判断MgCl2已经加足的方法是:取反应后的上层清液,___________ 。
(4)步骤⑤降温结晶制备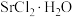 ,需要40%的SrCl2溶液100g,该溶液可由10%的SrCl2溶液蒸发
,需要40%的SrCl2溶液100g,该溶液可由10%的SrCl2溶液蒸发___________ g水获得。
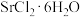 )”的工艺流程如图:
)”的工艺流程如图: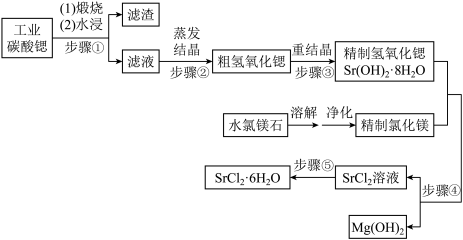
①欧锶的相关化合物(如SrO、SrCO3)的化学性质与相应的钙化合物类似,SrCO4、SrCO3不溶于水。
②SrCl2、MgCl2溶液皆为无色,呈中性。
(1)煅烧工业碳酸锶发生的反应与煅烧石灰石类似,则此过程的化学方程式为
(2)“重结晶”是将蒸发结晶得到的无水氢氧化锶粗品溶于适量热水,趁热滤去未溶解的固体后,冷却结晶得到Sr(OH)2•8H2O。为探究蒸馏水用量对Sr(OH)2•8H2O纯度及产率的影响,设计一系列探究实验,结果如表所示。分析表格数据可知,最合适的实验条件为
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 无水Sr(OH)2粗品质量/g | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 |
| 蒸馏水质量/g | 40.0 | 50.0 | 60.0 | 70.0 | 80.0 | 90.0 | 100 |
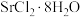 纯度/% 纯度/% | 98.6 | 98.6 | 98.6 | 98.6 | 98.6 | 98.6 | 98.6 |
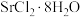 产率% 产率% | 17.91 | 53.36 | 63.50 | 72.66 | 92.17 | 89.65 | 88.93 |
(3)步骤④中,为了保证氯化锶产出量,MgCl2溶液必须足量,判断MgCl2已经加足的方法是:取反应后的上层清液,
(4)步骤⑤降温结晶制备
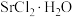 ,需要40%的SrCl2溶液100g,该溶液可由10%的SrCl2溶液蒸发
,需要40%的SrCl2溶液100g,该溶液可由10%的SrCl2溶液蒸发
您最近一年使用:0次
填空与简答-推断题
|
较易
(0.85)
解题方法
【推荐2】A~F均为初中化学常见的物质,他们之间的关系如图所示(“→”表示转化关系,所涉及反应均为初中常见的化学反应),其中A俗称生石灰,C是最常用的溶剂,C与F元素组成相同。
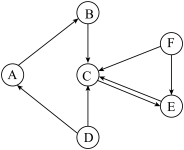
(1)C的化学式是_____ 。
(2)D→A反应的基本类型是_____ 。
(3)F→E反应的化学方程式为_____ 。

(1)C的化学式是
(2)D→A反应的基本类型是
(3)F→E反应的化学方程式为
您最近一年使用:0次
填空与简答-简答题
|
较易
(0.85)
真题
【推荐1】某小组同学外出野炊,所带的部分物品如表所示:
(1)从合理膳食,均衡饮食的角度分析,他们带的食物中还缺少_____ 。
(2)到了目的地,他们发现装食盐和苏打的瓶子忘记了做标记,可用所带物品_____ 来鉴别。
(3)做饭过程中,小红把炉灶里的树枝架空,使其燃烧更旺,原理是_____ 。
(4)味精是烹调中常用的鲜味调味品,它的主要成分是谷氨酸钠。谷氨酸钠低温时不易溶解,在温度T≥100℃时,长时间加热会转变成人体有害物质,根据以上信息,请写出一条食用味精时的注意事项_____ 。
(5)野炊结束后应及时把火熄灭,写出一种可采用的灭火方法_____ 。
| 食物 | 馕、羊肉、鲫鱼、豆腐 |
| 调料 | 食盐、苏打、砂糖、食醋、味精、酱油、食用油 |
(1)从合理膳食,均衡饮食的角度分析,他们带的食物中还缺少
(2)到了目的地,他们发现装食盐和苏打的瓶子忘记了做标记,可用所带物品
(3)做饭过程中,小红把炉灶里的树枝架空,使其燃烧更旺,原理是
(4)味精是烹调中常用的鲜味调味品,它的主要成分是谷氨酸钠。谷氨酸钠低温时不易溶解,在温度T≥100℃时,长时间加热会转变成人体有害物质,根据以上信息,请写出一条食用味精时的注意事项
(5)野炊结束后应及时把火熄灭,写出一种可采用的灭火方法
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
【推荐2】科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环.
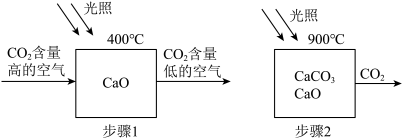
(1)步骤1的化学方程式为___ ;
(2)为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量___ 溶液,若观察到试管内___ ,则分解不完全.
(3)上述设想的优点有___ (填字母序号).
a.原料易得且可循环利用 b.充分利用太阳能 c.可全地域全天候使用
(4)CO2是宝贵的碳氧资源.CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为___ .
(5)若要检验1%甲酸水溶液是否显酸性,能选用的有___ (填字母序号).
a.无色酚酞溶液 b.紫色石蕊溶液 c.pH试纸
(6)请列举CO2的另两种用途___ ,___ .

(1)步骤1的化学方程式为
(2)为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量
(3)上述设想的优点有
a.原料易得且可循环利用 b.充分利用太阳能 c.可全地域全天候使用
(4)CO2是宝贵的碳氧资源.CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为
(5)若要检验1%甲酸水溶液是否显酸性,能选用的有
a.无色酚酞溶液 b.紫色石蕊溶液 c.pH试纸
(6)请列举CO2的另两种用途
您最近一年使用:0次
填空与简答-推断题
|
较易
(0.85)
【推荐3】某兴趣小组的同学在实验室用含有少量CaCl2的NaCl固体配制一定质量分数的NaCl溶液。实验步骤如下图所示:
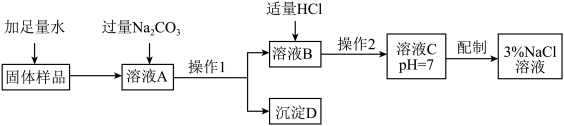
请回答下列问题:
(1)沉淀D的化学式为_____
(2)加入“过量Na2CO3”所发生反应的化学方程式为_____
(3)在“操作1”用的实验方法是_____
(4)加入“适量HCl”的目的是_____
(5)“操作2”的目的是测定溶液为中性,测定溶液pH的方法是_____
(6)经测定“溶液C”的质量为50g,质量分数为6%的氯化钠溶液(密度为1.04g/cm3)。现要用该溶液配制50g质量分数为3%的氯化钠溶液,所需6%的氯化钠溶液和水的体积分别为_____ ml和 _____ ml。(水密度为1.0g/cm3)。

请回答下列问题:
(1)沉淀D的化学式为
(2)加入“过量Na2CO3”所发生反应的化学方程式为
(3)在“操作1”用的实验方法是
(4)加入“适量HCl”的目的是
(5)“操作2”的目的是测定溶液为中性,测定溶液pH的方法是
(6)经测定“溶液C”的质量为50g,质量分数为6%的氯化钠溶液(密度为1.04g/cm3)。现要用该溶液配制50g质量分数为3%的氯化钠溶液,所需6%的氯化钠溶液和水的体积分别为
您最近一年使用:0次



