下图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答。

(1)蒸发前原溶液是 (填“饱和”或“不饱和”)溶液。n的数值是 。
(2)依据上述实验,你认为甲的溶解度随温度变化的趋势是 (填字母)的。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断

(1)蒸发前原溶液是 (填“饱和”或“不饱和”)溶液。n的数值是 。
(2)依据上述实验,你认为甲的溶解度随温度变化的趋势是 (填字母)的。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
2015·陕西·中考真题 查看更多[12]
第九单元 课题2 溶解度-【勤径千里马】2023-2024学年九年级下册化学随堂小练10分钟(人教版)(已下线)【万唯原创】2016年山西省中考化学试题研究卷模块一第6讲(已下线)2015年陕西省初中毕业学业考试(已下线)【万唯原创】2016年安徽省中考化学面对面卷九年级练习册第九单元(已下线)【万唯原创】2017年安徽省中考化学面对面卷九年级练习册第九单元(已下线)【万唯原创】2016年河南省中考化学面对面卷练习册九年级第九单元陕西省咸阳市秦都区百灵中学2019-2020学年九年级下学期第一次月考化学试题2016年福建省厦门市集美区中考模拟化学试题山东省德州市宁津县育新中学2019届九年级上学期12月月考化学试题北京市海淀区普通中学2018届九年级中考化学专题复习:溶解度2016届广东省潮州市高级实验学校九年级第一次模拟考试化学试卷2015年初中毕业升学考试(陕西卷)化学
更新时间:2016-11-28 13:06:42
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】自然界存在着“碳循环”。人类社会生产和生活发展导致大气中CO2含量增多,产生了全球气候变化等环境问题。我国在第七十五届联合国大会上承诺2060年前实现“碳中和”,体现了大国担当。下图表示与碳中和相关的过程。
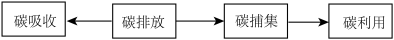
(1)碳排放。除生物体呼吸作用外,碳排放的主要途径有_________ 。
(2)碳吸收。除光合作用外,水吸收CO2是碳吸收的主要途径之一。一同学进行了下列实验:向充满CO2的塑料瓶中加入一定的水,迅速紧瓶盖振荡,塑料瓶变瘪。产生上述实验现象的原因是_________ 。
(3)碳捕集。其中,一种碳捕集的原理如图-1所示
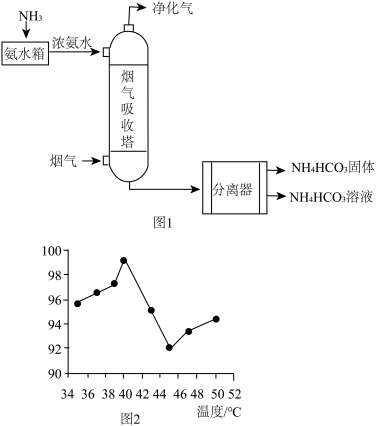
①吸收塔中,浓氨水(NH3·H2O)从上方喷洒,气体从下方通入,目的是________ ,烟气吸收塔中的化学反应方程式为______ 。
②分离器的作用相当于基本实验操作中的_______ ,经分离器得到的NH4HCO3溶液为该温度下的_____ 溶液(填“饱和”或“不饱和”)。
③净化气中CO2的含量________ 烟气中CO2的含量(填“大于”、“小于”或“等于”)。
④由图-2可以看出,温度对于本次实验的影响较大。当温度超过40℃之后,随着温度的上升,CO2脱除率下降,其主要原因是______ 。
(4)碳利用。我国科学家研制了一种高效催化剂,能催化CO2、H2合成CH3OH和H2O的反应。该反应中参加反应的CO2和H2的质量比为________ 。
(5)实现“碳中和”需要每一个人的努力,生活中的许多做法能减少大气中CO2的含量。请列举出一个能减少大气中CO2的含量的做法______ 。

(1)碳排放。除生物体呼吸作用外,碳排放的主要途径有
(2)碳吸收。除光合作用外,水吸收CO2是碳吸收的主要途径之一。一同学进行了下列实验:向充满CO2的塑料瓶中加入一定的水,迅速紧瓶盖振荡,塑料瓶变瘪。产生上述实验现象的原因是
(3)碳捕集。其中,一种碳捕集的原理如图-1所示

①吸收塔中,浓氨水(NH3·H2O)从上方喷洒,气体从下方通入,目的是
②分离器的作用相当于基本实验操作中的
③净化气中CO2的含量
④由图-2可以看出,温度对于本次实验的影响较大。当温度超过40℃之后,随着温度的上升,CO2脱除率下降,其主要原因是
(4)碳利用。我国科学家研制了一种高效催化剂,能催化CO2、H2合成CH3OH和H2O的反应。该反应中参加反应的CO2和H2的质量比为
(5)实现“碳中和”需要每一个人的努力,生活中的许多做法能减少大气中CO2的含量。请列举出一个能减少大气中CO2的含量的做法
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐2】生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水,水是最常用的溶剂。
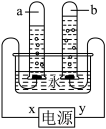
(1)电解水实验如右图所示。x是电源的_____ 极(填“正”或“负”),检验b试管中所得气体的方法是_____ 。
(2)A、B两种物质的溶解度曲线如图1所示;20℃时,将A、B两种固体各50g,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图2所示;升温到50℃时,A、B两种固体在水中的溶解情况如图3所示。(A、B两物质均不含结晶水)
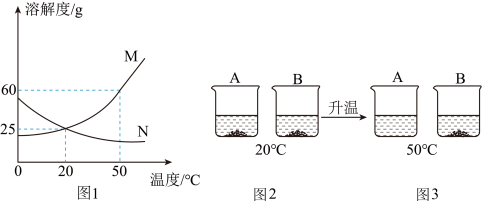
请回答下列问题:
①从20℃到50℃的变化过程中,一直处于饱和状态的是______ (填“A”或“B”)的溶液。
②图1中能表示A物质溶解度随温度变化的曲线是_______ (填“甲”或“乙”)。
③图1中P点的含义_________ 。
④图3中A溶液的溶质质量分数__________ 。(精确到0.1%)
(1)电解水实验如右图所示。x是电源的

(2)A、B两种物质的溶解度曲线如图1所示;20℃时,将A、B两种固体各50g,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图2所示;升温到50℃时,A、B两种固体在水中的溶解情况如图3所示。(A、B两物质均不含结晶水)

请回答下列问题:
①从20℃到50℃的变化过程中,一直处于饱和状态的是
②图1中能表示A物质溶解度随温度变化的曲线是
③图1中P点的含义
④图3中A溶液的溶质质量分数
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐3】工业上将氯化钠转化为氯酸钾(KClO3)晶体的简易流程如图所示:

⑴ 步骤I反应的化学方程式为______________________ 。
⑵ 步骤II析出晶体后的溶液是KClO3的______ (填“饱和溶液”或“不饱和溶液”)。
⑶ 下图分别为固体氯化钠和氯化钾的溶解度曲线。

①医用生理盐水为0.9%的氯化钠溶液,该溶液可为人体补充的营养素有________ 。
②60℃时,10 g水中最多溶解氯化钾的质量为_____ g。氯化钠和氯化钾在某一温度时,具有相同的溶解度,据图11所示,则该温度(t)的范围是_________ 。
③ 若采用某氯化钠溶液来选种,氯化钠与水的质量比为9︰41。将配制好的溶液装入试剂瓶,贴上标签,在下图中注明标签上的内容。

________________

⑴ 步骤I反应的化学方程式为
⑵ 步骤II析出晶体后的溶液是KClO3的
⑶ 下图分别为固体氯化钠和氯化钾的溶解度曲线。

①医用生理盐水为0.9%的氯化钠溶液,该溶液可为人体补充的营养素有
②60℃时,10 g水中最多溶解氯化钾的质量为
③ 若采用某氯化钠溶液来选种,氯化钠与水的质量比为9︰41。将配制好的溶液装入试剂瓶,贴上标签,在下图中注明标签上的内容。

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知蔗糖在水中溶解的质量随温度升高而变大。现在20℃下用蔗糖进行如下图所示的实验,该蔗糖溶液_____ (填“一定”或“不一定”)是饱和溶液,其溶质是_____ ,若要让试管中的蔗糖固体全部溶解,下列办法可行的是_____ (填字母序号)。

①试管内加入适量水
②烧杯内加入适量食盐
③烧杯内加入适量氢氧化钠固体
④烧杯内加入适量硝酸铵固体
A ①② B ①③ C ②③ D ②④

①试管内加入适量水
②烧杯内加入适量食盐
③烧杯内加入适量氢氧化钠固体
④烧杯内加入适量硝酸铵固体
A ①② B ①③ C ②③ D ②④
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】分析处理信息是学习的一种重要方法,下表是氯化钠与硝酸钾在不同温度下的溶解度。这两种固体物质在水中的溶解度曲线如图所示:

请仔细阅读图标后回答下列问题:
(1)A曲线表示的是________ 的溶解度曲线(选填“NaCl”或“KNO3”)。
(2)20 ℃时,100 g水中最多可溶解NaCl______________ g。
(3)溶解度曲线中的t1对应的温度范围是_______________ ℃。
(4)向烧杯中加入100 g水和90 g硝酸钾配成60 ℃的溶液,再冷却到20 ℃,烧杯中析出固体为________ g。

| 温度/℃ | 20 | 40 | 60 | 80 | |
| 温度/g | NaCl | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 31.6 | 63.9 | 110 | 169 | |
(1)A曲线表示的是
(2)20 ℃时,100 g水中最多可溶解NaCl
(3)溶解度曲线中的t1对应的温度范围是
(4)向烧杯中加入100 g水和90 g硝酸钾配成60 ℃的溶液,再冷却到20 ℃,烧杯中析出固体为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】图1是固体甲的溶解度曲线。图2是取等质量甲和乙两种物质(均不含结晶水)进行实验,最终烧杯中析出固体的质量乙大于甲。


(1)固体甲的溶解度随温度升高而_________________ 。
(2)60℃时,甲物质的饱和溶液中溶质与溶剂的质量比为_________________ 。
(3)由图2实验可推测出,40℃时,甲的溶解度____________ (填“>”、“=”或“<”)乙的溶解度。
(4)根据本实验结果,能否判断40℃~80℃,甲、乙哪种物质的溶解度变化受温度的影响更大?_________ (填“能”或“不能”)。


(1)固体甲的溶解度随温度升高而
(2)60℃时,甲物质的饱和溶液中溶质与溶剂的质量比为
(3)由图2实验可推测出,40℃时,甲的溶解度
(4)根据本实验结果,能否判断40℃~80℃,甲、乙哪种物质的溶解度变化受温度的影响更大?
您最近一年使用:0次
【推荐1】如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:

(1)P点含义是_____________ 。
(2)t2℃时,将8gA物质放入20g水中,充分溶解后,形成溶液的质量为________ 。
(3)若B物质中含有少量的A,提纯B物质的方法是________ 。
(4)t2℃时,A、B、C三种物质各10g,分别加水至恰好溶解,所得饱和溶液质量最大的是________ 。
(5)将A、B、C三种物质的饱和溶液从t3℃降温到t1℃时,溶质的质量分数由小到大的顺序为_____________ 。

(1)P点含义是
(2)t2℃时,将8gA物质放入20g水中,充分溶解后,形成溶液的质量为
(3)若B物质中含有少量的A,提纯B物质的方法是
(4)t2℃时,A、B、C三种物质各10g,分别加水至恰好溶解,所得饱和溶液质量最大的是
(5)将A、B、C三种物质的饱和溶液从t3℃降温到t1℃时,溶质的质量分数由小到大的顺序为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】下表是NaCl和KNO3物质在不同温度下的部分溶解度数据(单位:g),请回答问题:
(1)20℃时,NaCl的溶解度是___________ g;
(2)以上两种物质溶解度变化受温度影响较小的是___________ (选填“NaCl”或“KNO3”);
(3)20℃时,将20gNaCl固体加入50g水中,充分搅拌,形成的溶液质量为___________ g;
(4)当KNO3中混有少量的NaCl时,可以用___________ 方法提纯KNO3。
| 温度(℃) | 10 | 20 | 30 | 40 | 60 | |
| 溶解度(g) | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 110 | |
(2)以上两种物质溶解度变化受温度影响较小的是
(3)20℃时,将20gNaCl固体加入50g水中,充分搅拌,形成的溶液质量为
(4)当KNO3中混有少量的NaCl时,可以用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是X、Y、Z三种物质的溶解度曲线图,认真阅读完成下列各小题
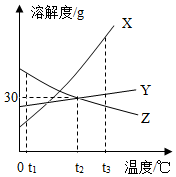
(1)在_____ ℃时,Y、Z两物质溶解度相等。
(2)t2℃时,将20gZ放入装有50g水的烧杯中,充分搅拌可能得到_______ gZ的饱和溶液。
(3)在t1℃时把质量均为mg的X、Y、Z三种固体溶于水中形成饱和溶液,需水质量最多的是_ 。
(4)下列说法正确的有_______ (只需填正确的选项序号)。
①Z物质有可能是气体
②若X中含有少量的Y,可用蒸发结晶提纯X
③将t3℃时等质量的X、Y饱和溶液同时降温到t1℃,析出晶体的质量是X>Y
④要将t1℃时接近饱和的X溶液变成饱和溶液,如不改变该溶液的组成,可选择降低温度的方法
⑤将t3℃时Z的饱和溶液降温至t2℃后,溶液的溶质质量分数会变大
(5)t2℃时,将X、Y、Z三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序是_______ 。

(1)在
(2)t2℃时,将20gZ放入装有50g水的烧杯中,充分搅拌可能得到
(3)在t1℃时把质量均为mg的X、Y、Z三种固体溶于水中形成饱和溶液,需水质量最多的是
(4)下列说法正确的有
①Z物质有可能是气体
②若X中含有少量的Y,可用蒸发结晶提纯X
③将t3℃时等质量的X、Y饱和溶液同时降温到t1℃,析出晶体的质量是X>Y
④要将t1℃时接近饱和的X溶液变成饱和溶液,如不改变该溶液的组成,可选择降低温度的方法
⑤将t3℃时Z的饱和溶液降温至t2℃后,溶液的溶质质量分数会变大
(5)t2℃时,将X、Y、Z三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序是
您最近一年使用:0次



