a g Zn、Mg、Al的混合物与一定浓度的H2SO4 m g恰好完全反应把溶液蒸干得不含结晶水固体质量为b g,则产生H2的质量为__________ g,H2SO4的质量分数为_________ 。
更新时间:2016-11-28 13:39:07
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】铝箔是厚度小于0.20mm、横断面呈矩形且均一的压延铝制品。因其优良的特性,广泛用于食品、饮料、香烟、药品、照相底板、家庭日用品等;铝箔是柔软的金属薄膜,不仅具有防潮、气密、遮光、耐磨蚀、保香、无毒无味等优点,而且还因为其有优雅的银白色光泽,易于加工出各种色彩的美丽图案和花纹,因而更容易受到人们的青睐。特别是铝箔与塑料和纸复合之后,把铝箔的屏蔽性与纸的强度、塑料的热密封性融为一体,进一步提高了作为包装材料所必需的对水汽、空气、紫外线和细菌等的屏蔽性能,大大拓宽了铝箔的应用市场。现对使用后的牛奶包装盒(铝箔与塑料和纸的复合材料)中铝箔的进行回收利用,流程如下:

查阅资料:I.氢氧化铝可以溶于强碱,如氢氧化钠,其反应为:Al(OH)3+NaOH=NaAlO2+2H2O
II.氨水是一种弱碱。
(1)铝箔作为牛奶包装盒材料,主要是因为铝箔__________ ;
(2)操作1可以达到的目的是____________ ;
(3)滤液1中的离子有__________ ,向滤液1中选择通入足量的氨气却没有选择氢氧化钠的原因是__________ ,通入氨气后可以观察到的现象是________________ 。
(4)根据以上提供的信息,Al(OH)3具有的性质是__________ (任写一条),写出反应③的化学方程式_________ ,忽略流程中铝的损失,牛奶包装盒中铝元素的含量是__________ 。

查阅资料:I.氢氧化铝可以溶于强碱,如氢氧化钠,其反应为:Al(OH)3+NaOH=NaAlO2+2H2O
II.氨水是一种弱碱。
(1)铝箔作为牛奶包装盒材料,主要是因为铝箔
(2)操作1可以达到的目的是
(3)滤液1中的离子有
(4)根据以上提供的信息,Al(OH)3具有的性质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体,另一种是参与光合作用的气体,请写出该反应的化学方程式___________ 。
(2)现将20gA和足量B在一定条件下充分反应,生成16gC和11gD,则参加反应的A和B 的质量比是___________
A 20:11 B 20:7 C 5:4 D 16:11
(3)某化合物是由氮、氧两种元素组成,其中相对分子质量为44,氮、氧元素的质量比为7:4,则它的化学式为___________
(2)现将20gA和足量B在一定条件下充分反应,生成16gC和11gD,则参加反应的A和B 的质量比是
A 20:11 B 20:7 C 5:4 D 16:11
(3)某化合物是由氮、氧两种元素组成,其中相对分子质量为44,氮、氧元素的质量比为7:4,则它的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】我国科学家屠呦呦发现并提纯抗疟疾药物青蒿素( C15H22O5),并荣获2015年诺贝尔奖。请计算:
①青蒿素的相对分子质量;_____
②青蒿素中碳、氢、氧元素的质量比;_____
③青蒿素中碳元素的质量分数(精确到0.1%)。_____
①青蒿素的相对分子质量;
②青蒿素中碳、氢、氧元素的质量比;
③青蒿素中碳元素的质量分数(精确到0.1%)。
您最近一年使用:0次
【推荐2】填充气体、放置干燥剂、添加防腐剂是食品防腐保鲜常用的方法。
(1)选用氮气作为填充的气体,其原因是_________________ 。
(2)生石灰可用作干燥剂的原因是_________________ 。(用化学方程式回答)
(3)丙酸钠是一种常用的防腐剂,其化学式为C3H5O2Na。它由___________ 种元素组成, 碳元素和氧元素的质量比为__________ 。
(1)选用氮气作为填充的气体,其原因是
(2)生石灰可用作干燥剂的原因是
(3)丙酸钠是一种常用的防腐剂,其化学式为C3H5O2Na。它由
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】填空。
(1)按要求从氢氧化镁、氧气、氧化钙、碳酸钙、碳酸中选取合适的物质,将其化学式填写在下列横线上。
①一种助燃性气体单质_________ ;
②一种可做干燥剂的金属氧化物_________ ;
③一种易分解的酸_________ ;
④一种难溶性的碱_________ 。
(2)坚持绿色发展,保护生态环境,是落实“人与自然和谐共生”发展观念的重要措施。试回答下列问题:
①水的天然循环给陆地带来淡水;在水中氢元素与氧元素的质量之比为_________ (填最简整数比)。液态水变成水蒸气的过程中,水分子运动速率_________ (填“增大”“减小”“不变”之一)。
②积极应对气候变化,二氧化碳是实现“碳达峰”和“碳中和”目标的指标性物质。山东“十四五”规划提出二氧化碳每年控制在1134万吨,若二氧化碳年排放1100万吨,则其中含碳元素的质量为_________ 万吨(结果精确至0.1万吨)。“碳中和”的有效方式之一就是植树造林,增大绿化面积。植物在光合作用时会吸收二氧化碳,生成的葡萄糖C6H12O6属于_________ (填“单质”“氧化物”“有机物”)。
③生活垃圾实现分类回收,既可以保护环境又能节约资源、能源。生活垃圾分为可回收物、有害垃圾、厨余垃圾和其他垃圾四类。下列各项中,属于有害垃圾的是_______ (填选项序号之一)。
A.废纸旧报 B.废旧灯管 C.瓜皮果核 D.废旧钢材
④开发和利用新能源,有利于生态环境保护。氢氧燃料电池已得到广泛应用,在这种电池中,氢气和氧气通过化学反应生成水。下列有关说法中,合理的是_______ (填选项序号之一)。

A.氢气和氧气发生了化合反应 B.该电池反应生成的水不污染环境
C.该电池的使用过程中化学能转化为电能 D.用电解水的方法制备所需氢气成本很低
(1)按要求从氢氧化镁、氧气、氧化钙、碳酸钙、碳酸中选取合适的物质,将其化学式填写在下列横线上。
①一种助燃性气体单质
②一种可做干燥剂的金属氧化物
③一种易分解的酸
④一种难溶性的碱
(2)坚持绿色发展,保护生态环境,是落实“人与自然和谐共生”发展观念的重要措施。试回答下列问题:
①水的天然循环给陆地带来淡水;在水中氢元素与氧元素的质量之比为
②积极应对气候变化,二氧化碳是实现“碳达峰”和“碳中和”目标的指标性物质。山东“十四五”规划提出二氧化碳每年控制在1134万吨,若二氧化碳年排放1100万吨,则其中含碳元素的质量为
③生活垃圾实现分类回收,既可以保护环境又能节约资源、能源。生活垃圾分为可回收物、有害垃圾、厨余垃圾和其他垃圾四类。下列各项中,属于有害垃圾的是

A.废纸旧报 B.废旧灯管 C.瓜皮果核 D.废旧钢材
④开发和利用新能源,有利于生态环境保护。氢氧燃料电池已得到广泛应用,在这种电池中,氢气和氧气通过化学反应生成水。下列有关说法中,合理的是

A.氢气和氧气发生了化合反应 B.该电池反应生成的水不污染环境
C.该电池的使用过程中化学能转化为电能 D.用电解水的方法制备所需氢气成本很低
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】我国每年报废的手机超过2亿部。废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。化学兴趣小组为回收其中的铜,设计并进行了如图实验。
【资料卡片】Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。_______ 。
(2)步骤①所得滤液中的溶质除硫酸外,还有______ 。
(3)步骤②中的实验现象是:固体部分溶解,______ 。
(4)步骤③中反应的化学方程式是______ 。该步骤所得滤渣的成分有______ 。
【资料卡片】Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。

(2)步骤①所得滤液中的溶质除硫酸外,还有
(3)步骤②中的实验现象是:固体部分溶解,
(4)步骤③中反应的化学方程式是
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】阅读下面科普短文。
我们的胃液呈酸性,是因为胃腺壁细胞能分泌出盐酸。胃酸在人体的消化吸收中发挥着重要作用,比如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维。使其易于被消化吸收。
你知道吗?深受人们喜爱的早餐食品燕麦中常添加颗粒极小的铁粉,它既可以作为双吸剂(起到干燥和减缓食品变质的作用),还可以作为补铁剂。要把铁粉变为人体需要的、能吸收的营养元素,就离不开胃酸的帮助。
健康人胃液的pH在0.9~1.5,胃液的pH不仅影响人的消化吸收功能,还对伴随食物进入人胃内的各类病菌的繁殖有影响。某医院对99位胃溃疡和十二指肠溃疡等患者胃液的pH及胃液中病菌进行了检测,结果如下表所示。
表-人体胃液PH情况分析
胃酸过多会对胃黏膜产生侵蚀作用,并使人感觉反酸或胃灼热。治疗胃酸过多的药主要有两大类:一是抑酸药,能抑制胃酸分泌,但本身不能和胃酸反应;二是抗酸药,能直接与胃酸反应。常服用的抗酸药的药物有碳酸氢钠、氢氧化铝、氧化镁、氢氧化镁和碳酸钙等胃溃疡患者若服用不合适的抗酸药,会因胃内气体压力增大而引起胃穿孔。患者如长期使用抗酸药,很可能刺激胃酸分泌过多。因此,应遵医嘱合理使用抗酸类和抑酸类药物。
依据文章内容,回答下列问题。
(1)在常用的抗酸药物碳酸氢钠(NaHCO3)、氢氧化铝[Al(OH)3]、氧化镁(MgO)、氢氧化镁Mg(OH)2和碳酸钙(CaCO3)中属于氧化物的是________ 。
(2)胃液的pH在0.9~1.5,胃液显________ (填“酸性、碱性、中性”)。
(3)燕麦中的铁粉遇到胃酸发生的化学反应,化学方程式是________ 。
(4)分析表格数据,可以得出胃液pH越________ (填“大”或“小”)越有利于病菌生存。
(5)下列说法正确的是________ (填字母序号)。
A 治疗胃酸过多的药物都能与盐酸反应
B 部分燕麦片中含有极少量的铁单质
C 氢氧化铝、氢氧化镁可以治疗各种胃酸过多
D 选用碳酸钙治疗胃酸过多,同时还可以补钙
我们的胃液呈酸性,是因为胃腺壁细胞能分泌出盐酸。胃酸在人体的消化吸收中发挥着重要作用,比如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维。使其易于被消化吸收。
你知道吗?深受人们喜爱的早餐食品燕麦中常添加颗粒极小的铁粉,它既可以作为双吸剂(起到干燥和减缓食品变质的作用),还可以作为补铁剂。要把铁粉变为人体需要的、能吸收的营养元素,就离不开胃酸的帮助。
健康人胃液的pH在0.9~1.5,胃液的pH不仅影响人的消化吸收功能,还对伴随食物进入人胃内的各类病菌的繁殖有影响。某医院对99位胃溃疡和十二指肠溃疡等患者胃液的pH及胃液中病菌进行了检测,结果如下表所示。
表-人体胃液PH情况分析
| 分组 | 胃液的 pH | 受检患者人数 | 胃液中检出病菌的人数及比列 |
| A | ≤2.0 | 7 | 0(0.0%) |
| B | 2.0-4.0 | 13 | 3(23.1%) |
| C | 4.0-6.0 | 26 | 17(65.4%) |
| D | ﹥6.0 | 53 | 45(84.9%) |
依据文章内容,回答下列问题。
(1)在常用的抗酸药物碳酸氢钠(NaHCO3)、氢氧化铝[Al(OH)3]、氧化镁(MgO)、氢氧化镁Mg(OH)2和碳酸钙(CaCO3)中属于氧化物的是
(2)胃液的pH在0.9~1.5,胃液显
(3)燕麦中的铁粉遇到胃酸发生的化学反应,化学方程式是
(4)分析表格数据,可以得出胃液pH越
(5)下列说法正确的是
A 治疗胃酸过多的药物都能与盐酸反应
B 部分燕麦片中含有极少量的铁单质
C 氢氧化铝、氢氧化镁可以治疗各种胃酸过多
D 选用碳酸钙治疗胃酸过多,同时还可以补钙
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】硫酸亚铁是一种重要的补铁剂。实验室以废铁屑(含少量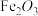 )为原料制备硫酸亚铁晶体的流程如下图所示。已知:铁与硫酸铁反应的化学方程式为:
)为原料制备硫酸亚铁晶体的流程如下图所示。已知:铁与硫酸铁反应的化学方程式为: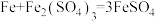 。
。

请据图回答下列问题。
(1)“碱洗”是为了洗去铁屑表面的油污。具体操作:先用热的碳酸钠溶液浸泡,过滤再用蒸馏水洗涤2~3次。取最后一次洗涤液,测其pH,若pH=______ ,说明洗涤液中无碳酸钠。
(2)“酸溶”是向“碱洗”过的铁屑中加入过量稀硫酸。
①写出铁与稀硫酸反应的化学方程式______ 。
②实验时,废铁屑中的少量Fe2O3不需要进行除杂处理,原因是______ 。
(3)“结晶”的相关操作依次为蒸发浓缩、降温结晶。蒸发浓缩的目的是______ ,便于结晶。
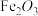 )为原料制备硫酸亚铁晶体的流程如下图所示。已知:铁与硫酸铁反应的化学方程式为:
)为原料制备硫酸亚铁晶体的流程如下图所示。已知:铁与硫酸铁反应的化学方程式为: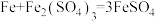 。
。
请据图回答下列问题。
(1)“碱洗”是为了洗去铁屑表面的油污。具体操作:先用热的碳酸钠溶液浸泡,过滤再用蒸馏水洗涤2~3次。取最后一次洗涤液,测其pH,若pH=
(2)“酸溶”是向“碱洗”过的铁屑中加入过量稀硫酸。
①写出铁与稀硫酸反应的化学方程式
②实验时,废铁屑中的少量Fe2O3不需要进行除杂处理,原因是
(3)“结晶”的相关操作依次为蒸发浓缩、降温结晶。蒸发浓缩的目的是
您最近一年使用:0次



