用如图微型仪器来完成制取并检验二氧化碳的实验只消耗了0.55g 10%的盐酸(密度为1.1g/mL)。通过计算回答:
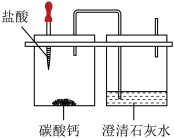
(1)产生二氧化碳的质量是多少?
(2)如果用锥形瓶来完成这个实验约需10%的盐酸5mL,这是微型实验所用药品量的多少倍?

(1)产生二氧化碳的质量是多少?
(2)如果用锥形瓶来完成这个实验约需10%的盐酸5mL,这是微型实验所用药品量的多少倍?
更新时间:2016-11-28 13:40:08
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某化学小组为了测定学校附近某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中的杂质不与稀盐酸反应也不溶于水)。有关实验数据如表所示:
可能用到的相对原子质量 :Ca-40 C-12 O-16 H-1 Cl-35.5
(1)根据质量守恒定律,反应中生成二氧化碳的质量为_______g。
(2)求该石灰石样品中碳酸钙的质量是多少?
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物质量 |
| 150g | 24g | 165.2g | |
可能用到的相对原子质量 :Ca-40 C-12 O-16 H-1 Cl-35.5
(1)根据质量守恒定律,反应中生成二氧化碳的质量为_______g。
(2)求该石灰石样品中碳酸钙的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】向盛有13.5 g石灰石的烧杯中,加入50 g一定质量分数的稀盐酸(杂质不溶于水也不与盐酸反应)恰好完全反应后烧杯中物质总质量为59.1 g,试计算:
(1)碳酸钙中钙元素的质量分数。
(2)所取的石灰石中碳酸钙的质量是多少?
(1)碳酸钙中钙元素的质量分数。
(2)所取的石灰石中碳酸钙的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某化学小组为了测定学校附近某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中的杂质不与稀盐酸反应也不溶于水)。有关实验数据如表所示:
(1)根据质量守恒定律,反应中生成二氧化碳的质量为___________  。
。
(2)求该石灰石样品中碳酸钙的质量是多少?
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物质量 |
| 150g | 24g | 165.2g | |
 。
。(2)求该石灰石样品中碳酸钙的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组测定某硫酸铜溶液中溶质的质量分数。向盛有40g硫酸铜溶液的烧杯中加入50g质量分数为20.8%的氯化钡溶液,恰好完全反应。
(1)氯化钡溶液中溶质的质量为_______ g。
(2)求硫酸铜溶液中溶质的质量分数_____ 。
[温馨提示:CuSO4+BaCl2=BaSO4↓+CuCl2]
(1)氯化钡溶液中溶质的质量为
(2)求硫酸铜溶液中溶质的质量分数
[温馨提示:CuSO4+BaCl2=BaSO4↓+CuCl2]
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】根据如图所示的信息计算:
(1)加入的稀硫酸质量为________ g。
(2)反应后所得溶液中溶质的质量分数。

(1)加入的稀硫酸质量为
(2)反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】某种铁合金中含有不溶于酸的杂质。取该合金样品粉末11.4g,分四次向其中加入稀盐酸共100g。反应过程的有关数据记录如下表。
(1)a= 。
(2)计算稀盐酸中溶质的质量分数(请写出计算过程)。
| 次序 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
| 剩余固体的质量/g | 8.6 | a | 3 | 0.2 |
(1)a= 。
(2)计算稀盐酸中溶质的质量分数(请写出计算过程)。
您最近一年使用:0次



