工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,称为氯碱工业。在工业上,制取氯气和烧碱的主要工艺流程如下:

环节Ⅰ:利用海水提取粗盐的过程(如图)。

(1)图中①是_____ (填“蒸发”或“冷却”)池。
(2)母液为氯化钠的_____ (填“饱和”或“不饱和”)溶液。
环节Ⅱ:利用工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质)精制氯化钠(工艺流程如图)。

(1)X中含有的阳离子是_____ ;
(2)写出生成沉淀D的一个化学方程式_____ ;
(3)溶液E中加过量稀盐酸的作用是_____ ;
(4)实验所得精盐的质量大于粗盐中NaCl的质量,原因是_____ 。
环节Ⅲ:电解饱和食盐水生产氯气和烧碱并测定烧碱的纯度。
(1)请写出环节Ⅲ生产中发生反应的化学方程式_____ ;
(2)工业烧碱常常含有一定的氯化钠和碳酸钠杂质。为了测定烧碱的含量,小婉同学设计探究方案后进行实验并测得数据如图:

请你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程)_____ ;
(3)小强同学认为小婉同学设计的探究方案不够严密,其理由是:
①探究方案中没考虑氢氧化钠的吸水性;
②探究方案中因缺少_____ (填操作名称),导致测得的氢氧化钠的质量分数偏小。
环节Ⅳ:应用举例
氯气与氢氧化钠溶液反应的化学方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,工业上用氯气与石灰乳[Ca(OH)2]反应来制取漂白粉,有关反应的化学方程式是_____ 。

环节Ⅰ:利用海水提取粗盐的过程(如图)。

(1)图中①是
(2)母液为氯化钠的
环节Ⅱ:利用工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质)精制氯化钠(工艺流程如图)。

(1)X中含有的阳离子是
(2)写出生成沉淀D的一个化学方程式
(3)溶液E中加过量稀盐酸的作用是
(4)实验所得精盐的质量大于粗盐中NaCl的质量,原因是
环节Ⅲ:电解饱和食盐水生产氯气和烧碱并测定烧碱的纯度。
(1)请写出环节Ⅲ生产中发生反应的化学方程式
(2)工业烧碱常常含有一定的氯化钠和碳酸钠杂质。为了测定烧碱的含量,小婉同学设计探究方案后进行实验并测得数据如图:

请你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程)
(3)小强同学认为小婉同学设计的探究方案不够严密,其理由是:
①探究方案中没考虑氢氧化钠的吸水性;
②探究方案中因缺少
环节Ⅳ:应用举例
氯气与氢氧化钠溶液反应的化学方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,工业上用氯气与石灰乳[Ca(OH)2]反应来制取漂白粉,有关反应的化学方程式是
更新时间:2016-11-28 13:53:37
|
相似题推荐
综合应用题
|
困难
(0.15)
【推荐1】过氧化钙(CaO2)是用途广泛的优良供氧剂。以电石渣[主要成分为 Ca(OH)2,含少量 CaCO3] 为原料制备 CaO2 的一种工艺流程如图甲所示:

【查阅资料】Ⅰ.Ca(OH)2+2NH4Cl=CaCl2+2NH3•H2O
Ⅱ.CaCl2+2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4Cl
Ⅲ.CaO2•8H2O在水中不太稳定,会缓慢分解
(1)CaO2 与 CO2 反应除了生成氧气外、还生成一种常见的盐,写出反应的化学方程式___________ 。
(2)“提取 Ca(OH)2”时反应的基本类型是________ ;Ca(OH)2 的俗名为________ ;“过滤 1”所得滤渣的主要成分是______________ 。
(3)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“一贴”指的是滤纸紧贴漏斗壁, 原因是________ 。实验室粗略测定溶液的酸碱度,常使用(填名称)_________________ 。
(4)在其他条件不变的情况下,制备 CaO2·8H2O 的反应时间(t)对其产率(ω )的影响如图乙所示。

①平均反应速率最快的时间段为___________ 。
②30min 后,ω 开始下降的主要原因是_________________ 。
(5)为了测定加入的 NH4Cl 溶液中溶质的质量分数,取 107.0gNH4Cl 溶液于烧杯中,加入稍过量的 AgNO3 溶液,完全反应后过滤、洗涤、干燥、称量, 得到14.35 g 白色固体。通过计算确定该溶液中NH4Cl 的质量分数为________ 。(精确到 0.1%)

【查阅资料】Ⅰ.Ca(OH)2+2NH4Cl=CaCl2+2NH3•H2O
Ⅱ.CaCl2+2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4Cl
Ⅲ.CaO2•8H2O在水中不太稳定,会缓慢分解
(1)CaO2 与 CO2 反应除了生成氧气外、还生成一种常见的盐,写出反应的化学方程式
(2)“提取 Ca(OH)2”时反应的基本类型是
(3)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“一贴”指的是滤纸紧贴漏斗壁, 原因是
(4)在其他条件不变的情况下,制备 CaO2·8H2O 的反应时间(t)对其产率(ω )的影响如图乙所示。

①平均反应速率最快的时间段为
②30min 后,ω 开始下降的主要原因是
(5)为了测定加入的 NH4Cl 溶液中溶质的质量分数,取 107.0gNH4Cl 溶液于烧杯中,加入稍过量的 AgNO3 溶液,完全反应后过滤、洗涤、干燥、称量, 得到14.35 g 白色固体。通过计算确定该溶液中NH4Cl 的质量分数为
您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
【推荐2】海水是巨大的资源宝库,利用海水为原料获得许多化工产品的流程如下图:

(1)实验室去除粗盐中难溶性杂质的一般步骤是:溶解、过滤、______ 、计算产率;
(2)步骤①中选用蒸发结晶而不用降温结晶的理由是_________________________ 。
(3)由上述流程图看出碳酸氢钠的热稳定性_________ (填“大于、小于或等于)纯碱的热稳定性。
(4)步骤②发生的反应属于_________ 反应(填一种基本反应类型)。用镁制造的一种镁铝合金常用作生产飞机外壳的材料,该材料具有的优良性能有________ (任答一点)。
(5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),
反应后溴元素的化合价比反应前_______ (填“升高”或“降低”或“不变”)。
(6)通过海水为原料制取纯碱中会含有杂质氯化钠,为了测定纯碱中杂质氯化钠的质量分数,小阳同学进行了三次实验,实验数据如下表:
完成下列计算:
①固体样品中氯化钠的质量分数是______ ;
②第 2 次反应结束后溶液中溶质质量分数是多少______ ?(写出必要的计算题过程)

(1)实验室去除粗盐中难溶性杂质的一般步骤是:溶解、过滤、
(2)步骤①中选用蒸发结晶而不用降温结晶的理由是
(3)由上述流程图看出碳酸氢钠的热稳定性
(4)步骤②发生的反应属于
(5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),
反应后溴元素的化合价比反应前
(6)通过海水为原料制取纯碱中会含有杂质氯化钠,为了测定纯碱中杂质氯化钠的质量分数,小阳同学进行了三次实验,实验数据如下表:
| 编 号 | 第 1 次 | 第 2次 | 第 3次 |
| 所取固体样品的质量/g | 13 | 10 | 10 |
| 样品用98g水溶解后,加入CaCl2溶液的质量/g | 100 | 100 | 125 |
| 反应后生成沉淀的质量/g | 8 | 8 | 8 |
①固体样品中氯化钠的质量分数是
②第 2 次反应结束后溶液中溶质质量分数是多少
您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
【推荐3】金属材料在人类的生产、生活中有着十分重要的作用。
(1)很多种金属可以压成薄片、拉成细丝,说明金属具有______ 性。
(2)每年因金属腐蚀造成的损失都很巨大。下列对金属的防护措施不合理的是______(填序号)。
(3)为探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案:
结论:金属活动性Al>Fe>Cu
①将铝丝插入前应进行的操作是______ ;
②小明同学认为在小刚的实验中只需调整一下插入金属的顺序,就可得出Al>Fe>H>Cu的结论。你认为调整后插入金属的顺序是______ 。
(4)在钢铁厂的实验室,同学们采集了用某种分析仪记录的CO与Fe2O3进行反应时的有关数据,并得到固体质量与反应温度的关系曲线。根据图像分析写出P点时固体成分的化学式______ ;固体质量由48.0g变为46.4g的过程中发生反应的化学方程式______ 。

(5)6.5g某粗锌(杂质不反应)与58.4g稀盐酸恰好完全反应,共产生氢气0.16g。试计算粗锌中锌的质量分数。
(1)很多种金属可以压成薄片、拉成细丝,说明金属具有
(2)每年因金属腐蚀造成的损失都很巨大。下列对金属的防护措施不合理的是______(填序号)。
| A.铁制护栏刷油漆 | B.将钢材深埋保存 |
| C.将钢刀浸泡在盐水中 | D.将铁制成不锈钢 |
(3)为探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案:
| 实验步骤 | 观察到的现象 |
| Ⅰ、在试管中取少量盐酸,插入铁丝,充分作用 | |
| Ⅱ、在I所得的溶液中,插入铜丝,充分作用无明显现象 | 无明显现象 |
| Ⅲ、在Ⅱ所得的溶液中,插入铝丝,充分作用 |
①将铝丝插入前应进行的操作是
②小明同学认为在小刚的实验中只需调整一下插入金属的顺序,就可得出Al>Fe>H>Cu的结论。你认为调整后插入金属的顺序是
(4)在钢铁厂的实验室,同学们采集了用某种分析仪记录的CO与Fe2O3进行反应时的有关数据,并得到固体质量与反应温度的关系曲线。根据图像分析写出P点时固体成分的化学式

(5)6.5g某粗锌(杂质不反应)与58.4g稀盐酸恰好完全反应,共产生氢气0.16g。试计算粗锌中锌的质量分数。
您最近一年使用:0次
【推荐1】(1)实验室制取气体时需要的部分装置如图所示,请回答下列问题。

①实验室中可用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为______ ,应选用的发生装置是______ (选填装置字母序号)。
②实验室中用石灰石和稀盐酸制取一瓶干燥、纯净的二氧化碳气体,所选装置的连接顺序为:气体发生装置→______ →______ →D(选填装置字母序号)。
【信息】二氧化碳不易溶于饱和碳酸氢钠溶液。
③确定实验室制取气体的反应原理时,下列因素中不需要考虑的是______ (选填字母序号)
A.药品容易获得,能生成所要制取的气体
B.反应条件易于控制,反应速率适中
C.操作简便易行,安全可靠,节能环保
D.所要制取气体的颜色和气味
④制取气体的过程包括;a.选择制取装置;b.验证所得气体;c.明确反应原理。据此总结出实验室里制取气体的一般思路为______ (填字母)。
(2)某化学兴趣小组为验证酸的通性,做了以下5组实验,请分析并回答问题:
【演示实验】

【提出质疑】实验③没有明显现象,甲同学对该实验是否发生化学反应提出质疑,并设计了以下实验进行验证。
【实验探究】
【评价交流】①乙同学认为甲同学的验证实验中方案二不可行,理由是______ ,
②请再设计一个实验证明氢氧化钠溶液与稀盐酸发生了反应______ 。
【拓展延伸】演示实验中有一组没有验证酸的通性,该组是______ (填序号)。请你补充一个演示实验(不改变反应物的类别)完整验证酸的通性,该实验的化学方程式为______ 。

①实验室中可用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为
②实验室中用石灰石和稀盐酸制取一瓶干燥、纯净的二氧化碳气体,所选装置的连接顺序为:气体发生装置→
【信息】二氧化碳不易溶于饱和碳酸氢钠溶液。
③确定实验室制取气体的反应原理时,下列因素中不需要考虑的是
A.药品容易获得,能生成所要制取的气体
B.反应条件易于控制,反应速率适中
C.操作简便易行,安全可靠,节能环保
D.所要制取气体的颜色和气味
④制取气体的过程包括;a.选择制取装置;b.验证所得气体;c.明确反应原理。据此总结出实验室里制取气体的一般思路为
(2)某化学兴趣小组为验证酸的通性,做了以下5组实验,请分析并回答问题:
【演示实验】

【提出质疑】实验③没有明显现象,甲同学对该实验是否发生化学反应提出质疑,并设计了以下实验进行验证。
【实验探究】
| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
| 一 | 测定氧氧化钠溶液的pH=a,滴加稀盐酸后测得溶液pH=b(忽略体积的变化) | a | 发生了反应 |
| 二 | 向实验③所得混合溶液中加入硝酸银溶液 | 有白色沉淀产生 | 发生了反应 |
②请再设计一个实验证明氢氧化钠溶液与稀盐酸发生了反应
【拓展延伸】演示实验中有一组没有验证酸的通性,该组是
您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
【推荐2】探究碱的化学性质时,设计图1所示的两个实验,然后将反应废液倒入同一废液缸中,发现混合后废液浑浊并变红色。

(1)A实验中滴有酚酞的目的是______ ,判断A实验中恰好实验反应的现象是______ 。
(2)B实验中发生反应的化学方程式为______ 。
(3)取一定量的废液过滤,向滤液逐滴加入稀盐酸,根据反应现象得到图2所示图像,则混合废液中存在的溶质除了氯化钠外还含有______ ,其理由是______ ,写出加入稀盐酸没有气体生成的化学方程式______ 。
(4)取一定量的混合后的废液过滤,向滤液中逐滴加入氯化钙溶液得到图3所示图像,则废液中一定含有的物质为______ 。
(5)现有50g氯化钙溶液与100g碳酸钠溶液恰好完全反应,将反应后的混合物过滤后得到溶液的质量为140g,求碳酸钠溶液中溶质的质量分数是多少?

(1)A实验中滴有酚酞的目的是
(2)B实验中发生反应的化学方程式为
(3)取一定量的废液过滤,向滤液逐滴加入稀盐酸,根据反应现象得到图2所示图像,则混合废液中存在的溶质除了氯化钠外还含有
(4)取一定量的混合后的废液过滤,向滤液中逐滴加入氯化钙溶液得到图3所示图像,则废液中一定含有的物质为
(5)现有50g氯化钙溶液与100g碳酸钠溶液恰好完全反应,将反应后的混合物过滤后得到溶液的质量为140g,求碳酸钠溶液中溶质的质量分数是多少?
您最近一年使用:0次
综合应用题
|
困难
(0.15)
【推荐3】铁和铁的化合物在工农业生产中有广泛的应用。
I.铁的冶炼和探究
已知B装置中的液体为过量的氢氧化钠与氢氧化钙混合溶液。请回答下列问题:
(1)实验过程中A处对应的化学方程式为_____________ 。
(2)实验装置按如图连接,请将以下四步按正确操作步骤排序:________ (填字母)。

a.点燃A处酒精喷灯 b.通入 CO
c.停止通入 CO d.熄灭酒精喷灯
(3)实验装置图中虚线框内装置起到的作用有_____________ (填字母)。
a.收集一氧化碳 b.吸收二氧化碳 c.检验二氧化碳
II.铁的腐蚀与防护
(4)为防止铁生锈,可对铁制品进行“发蓝”处理,使其表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为_________ 。
III.已知:难溶性的碱受热分解生成对应的金属氧化物。
以FeSO4为原料制备铁黑颜料Fe3O4(其中Fe既有+2价,也有+3价)的过程如下:

资料:分解过程中的反应为
(5)“沉淀”时的反应化学方程式为________ 。实验室进行过滤时需要的玻璃仪器有烧杯、玻璃棒和___________ ,玻璃棒的作用是_____________ 。
(6)检验沉淀是否洗涤干净应选用的试剂是_____________ (填化学式)。
(7)“转化”过程的反应为: 。若原料中含FeSO49.12 t,理论上最终可以获得 Fe3O4的质量为
。若原料中含FeSO49.12 t,理论上最终可以获得 Fe3O4的质量为______ t。
(8)若“转化”过程参与反应的O2过量,则最终所得固体的质量_____________ (填“偏大”,“偏小”或“不变”)。
(9)FeSO4高温下分解,产物是一种红棕色固体 A 和两种硫的氧化物气体且相对分子质量相差16,则该反应的化学方程式___________ 。
I.铁的冶炼和探究
已知B装置中的液体为过量的氢氧化钠与氢氧化钙混合溶液。请回答下列问题:
(1)实验过程中A处对应的化学方程式为
(2)实验装置按如图连接,请将以下四步按正确操作步骤排序:

a.点燃A处酒精喷灯 b.通入 CO
c.停止通入 CO d.熄灭酒精喷灯
(3)实验装置图中虚线框内装置起到的作用有
a.收集一氧化碳 b.吸收二氧化碳 c.检验二氧化碳
II.铁的腐蚀与防护
(4)为防止铁生锈,可对铁制品进行“发蓝”处理,使其表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为
III.已知:难溶性的碱受热分解生成对应的金属氧化物。
以FeSO4为原料制备铁黑颜料Fe3O4(其中Fe既有+2价,也有+3价)的过程如下:

资料:分解过程中的反应为

(5)“沉淀”时的反应化学方程式为
(6)检验沉淀是否洗涤干净应选用的试剂是
(7)“转化”过程的反应为:
 。若原料中含FeSO49.12 t,理论上最终可以获得 Fe3O4的质量为
。若原料中含FeSO49.12 t,理论上最终可以获得 Fe3O4的质量为(8)若“转化”过程参与反应的O2过量,则最终所得固体的质量
(9)FeSO4高温下分解,产物是一种红棕色固体 A 和两种硫的氧化物气体且相对分子质量相差16,则该反应的化学方程式
您最近一年使用:0次
综合应用题
|
困难
(0.15)
名校
解题方法
【推荐1】浩瀚的大海里蕴藏着丰富的资源,开发海水资源前景广阔。
(1)工业上利用太阳能进行海水晒盐。已知海水蒸发浓缩过程中析出盐的种类和质量如下表:(表中数据为每升海水在浓缩过程中析出各种盐的质量,单位为g)
①海水从密度为1.21g/mL浓缩到1.22g/mL时,下列说法正确的是___________ 。
A.各种盐的溶解度增大B.海水中NaBr的质量分数不变
C.析出粗盐中NaCl的质量分数增大D.海水中水的质量分数不变
②海水在浓缩过程中,最先析出的盐是___________ 。
(2)工业上利用粗盐水(含有少量CaCl2、MgCl2)生产纯碱,工艺流程如图:

已知:ⅰ、常温下,NH3极易溶于水,CO2能溶于水;
ⅱ、NaHCO3加热易分解,Na2CO3加热不易分解。
完成下列填空:
①粗盐水加入沉淀剂NaOH,Na2CO3分别除去MgCl2、CaCl2,固体C为___________ 。
②流程中,先“氨化”后“碳酸化”的目的是___________ 。
③“碳酸化”后过滤获得的NH4Cl可用作___________ 肥,也可先___________ (填“加热”或“冷却”)NH4Cl溶液,再加入石灰水以循环使用的物质是___________ 。
④“煅烧”时,NaHCO3分解生成的气体D是___________ ,若将气体D直接排入空气不合理的理由是___________ 。
(3)以含有CaCl2、MgCl2的卤水和贝壳(主要成分为CaCO3)为主要原料在实验室制备无水CaCl2,流程如图1。

请回答下列问题:
①操作Ⅰ的名称是___________ 。
②以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式___________ 。
③操作Ⅱ酸化时应选择的酸是___________ (填化学式)。
④回收的CO2在紫外线照射和催化剂作用下能与水蒸气反应,生成甲烷和氧气,该反应的化学方程式为___________ 。紫外线照射时,在不同催化剂(①、②、③)的作用下,甲烷产量随光照时间的变化如图2所示,在第10小时时,甲烷产量最高是___________ (填写“①”“②”或“③”)。

(1)工业上利用太阳能进行海水晒盐。已知海水蒸发浓缩过程中析出盐的种类和质量如下表:(表中数据为每升海水在浓缩过程中析出各种盐的质量,单位为g)
| 海水密度 | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
| 1.13 | 0.56 | ||||
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
①海水从密度为1.21g/mL浓缩到1.22g/mL时,下列说法正确的是
A.各种盐的溶解度增大B.海水中NaBr的质量分数不变
C.析出粗盐中NaCl的质量分数增大D.海水中水的质量分数不变
②海水在浓缩过程中,最先析出的盐是
(2)工业上利用粗盐水(含有少量CaCl2、MgCl2)生产纯碱,工艺流程如图:

已知:ⅰ、常温下,NH3极易溶于水,CO2能溶于水;
ⅱ、NaHCO3加热易分解,Na2CO3加热不易分解。
完成下列填空:
①粗盐水加入沉淀剂NaOH,Na2CO3分别除去MgCl2、CaCl2,固体C为
②流程中,先“氨化”后“碳酸化”的目的是
③“碳酸化”后过滤获得的NH4Cl可用作
④“煅烧”时,NaHCO3分解生成的气体D是
(3)以含有CaCl2、MgCl2的卤水和贝壳(主要成分为CaCO3)为主要原料在实验室制备无水CaCl2,流程如图1。

请回答下列问题:
①操作Ⅰ的名称是
②以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式
③操作Ⅱ酸化时应选择的酸是
④回收的CO2在紫外线照射和催化剂作用下能与水蒸气反应,生成甲烷和氧气,该反应的化学方程式为

您最近一年使用:0次
综合应用题
|
困难
(0.15)
真题
解题方法
【推荐1】盐城濒临黄海,海盐文化全国知名.某兴趣小组同学去盐场参观,带回了部分粗盐样品,并对其进行了如下探究:

(1)操作①中必须用到的一种仪器是_______ (填序号)
A 研钵 B 量筒 C 烧杯 D 试管
(2)操作③的名称是_____ ,操作④中用到玻璃棒,作用为 _____ 。
(3)用提纯得到的“精盐”配制100g 7.5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有_____ (填序号)
①氯化钠固体不纯
②称量时精盐与砝码放反了
③量取水时俯视读数
④装瓶时,有少量溶液洒出
(4)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgCl2一种),为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如下处理:

①白色沉淀的化学式为_____ .
②在得到的滤液中加入足量的稀盐酸的目的是_____ .
③若实验过程中不考虑损耗,最终到的NaCl固体的质量将_____ (填“大于”、“小于”或“等于”)原精盐中NaCl的质量.

(1)操作①中必须用到的一种仪器是
A 研钵 B 量筒 C 烧杯 D 试管
(2)操作③的名称是
(3)用提纯得到的“精盐”配制100g 7.5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有
①氯化钠固体不纯
②称量时精盐与砝码放反了
③量取水时俯视读数
④装瓶时,有少量溶液洒出
(4)查阅资料得知:粗盐中除含少量泥沙等不溶性杂质外,还含有少量的可溶性杂质(假定可溶性杂质只有MgCl2一种),为了得到较纯净的氯化钠,小组同学将所得的“精盐”又作了如下处理:

①白色沉淀的化学式为
②在得到的滤液中加入足量的稀盐酸的目的是
③若实验过程中不考虑损耗,最终到的NaCl固体的质量将
您最近一年使用:0次
综合应用题
|
困难
(0.15)
名校
解题方法
【推荐2】食盐、碳酸钠和碳酸氢钠是生活中常见的钠盐。请回答下列问题。
(1)碳酸氢钠的水溶液显_______ 性(填“酸”、“碱”或“中”)。碳酸氢钙受热易分解,碳酸氢钠性质与其相似。除去碳酸钠固体中混有的少量碳酸氢钠,反应的化学方程式为_______ ;
(2)等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应时生成的CO2质量,前者_______ 后者(填“>”、“<”或“=”);
(3)粗盐含有少量杂质(主要为CaCl2、MgCl2、Na2SO4等)。用粗盐制取“化学纯”级的NaCl,步骤为溶解、加过量a、加过量NaOH、加过量b、过滤、加适量盐酸,蒸发结晶得到“化学纯”级的NaCl固体。
①试剂a、b分别是_______ (填序号)
A.Na2CO3、BaCl2 B.BaCl2、Na2CO3 C.BaCl2、Na2SO4
②加过量NaOH的目的是_______ ;
③加适量盐酸的目的是_______ ;
④蒸发结晶时,玻璃棒的作用是_______ 。
(4)工业上用电解饱和食盐水的方法生产氯气和烧碱。
资料一:Cl2+H2O=HCl+HClO
资料二:初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-=H2O。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)
第一步:写出Na2SO4与BaCl2反应的化学方程式;
第二步:把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述化学方程式可改写成:2Na++ +Ba2++2Cl-=BaSO4↓+2Na++2Cl-;
+Ba2++2Cl-=BaSO4↓+2Na++2Cl-;
第三步:删去方程式两边不参加反应的离子:Ba2++ =BaSO4↓;
=BaSO4↓;
第四步:检查方程式两边各元素的原子个数和电荷总数是否相等。
①写出Na2CO3与稀盐酸反应的离子方程式:_______ ;
②某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理_______ (用离子方程式表示);
资料三:化学反应类型有不同的分法,其中反应前后,有元素化合价变化的化学反应是氧化还原反应。氧化还原反应中有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂,化合价没有变化的反应物既不是氧化剂也不是还原剂。
③工业上可用氨检验输送氯气的管道是否漏气。反应化学方程式如下:8NH3+3C12=6NH4Cl+N2。该反应_______ (填“是”或“不是”)氧化还原反应,其中氧化剂和还原剂的质量比为_______ (若是氧化还原反应,此空作答,反之,不作答)。
(1)碳酸氢钠的水溶液显
(2)等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应时生成的CO2质量,前者
(3)粗盐含有少量杂质(主要为CaCl2、MgCl2、Na2SO4等)。用粗盐制取“化学纯”级的NaCl,步骤为溶解、加过量a、加过量NaOH、加过量b、过滤、加适量盐酸,蒸发结晶得到“化学纯”级的NaCl固体。
①试剂a、b分别是
A.Na2CO3、BaCl2 B.BaCl2、Na2CO3 C.BaCl2、Na2SO4
②加过量NaOH的目的是
③加适量盐酸的目的是
④蒸发结晶时,玻璃棒的作用是
(4)工业上用电解饱和食盐水的方法生产氯气和烧碱。
资料一:Cl2+H2O=HCl+HClO
资料二:初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-=H2O。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式。离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)
第一步:写出Na2SO4与BaCl2反应的化学方程式;
第二步:把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述化学方程式可改写成:2Na++
 +Ba2++2Cl-=BaSO4↓+2Na++2Cl-;
+Ba2++2Cl-=BaSO4↓+2Na++2Cl-;第三步:删去方程式两边不参加反应的离子:Ba2++
 =BaSO4↓;
=BaSO4↓;第四步:检查方程式两边各元素的原子个数和电荷总数是否相等。
①写出Na2CO3与稀盐酸反应的离子方程式:
②某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理
资料三:化学反应类型有不同的分法,其中反应前后,有元素化合价变化的化学反应是氧化还原反应。氧化还原反应中有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂,化合价没有变化的反应物既不是氧化剂也不是还原剂。
③工业上可用氨检验输送氯气的管道是否漏气。反应化学方程式如下:8NH3+3C12=6NH4Cl+N2。该反应
您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
【推荐3】纯碱是重要的化工原料
(一)制备探究:如图是工业生产纯碱的主要流程示意图。
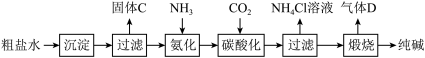
[查阅资料]
①粗盐水中含有杂质MgCl2、CaCl2;
②常温下,NH3极易溶于水,CO2能溶于水,
③NaHCO3加热易分解,Na2CO3加热不易分解。
(1)写出除去粗盐水中MgCl2的化学方程式:_____________________________ 。
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是______________ ,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式______________________________ 。
(3)“碳酸化”后过滤获得的NH4Cl可用作氮肥,也可先加热NH4Cl溶液,再加入熟石灰获得循环使用的物质是___________________ ;
(4)煅烧制得纯碱的化学方程式是________________________________ 。
(二)成分探究
[提出问题]纯碱样品中含有哪些杂质?
[猜想]
猜想一:可能含有NaHCO3; 猜想二:可能含有NaCl;猜想三:NaHCO3和NaCl
[实验探究]确定纯碱中是否含NaHCO3。实验装置和主要实验步骤如下:
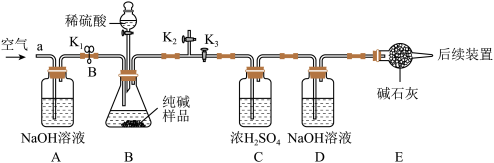
①称量D、E装置总质量为200.0g,检查装置的气密性,将10.6 g纯碱试样放入锥形瓶中,按上图组装仪器,进行如下操作 ,后缓缓鼓入一段时间空气;
②按一定要求正确操作后,加入足量稀硫酸,待锥形瓶中不再产生气泡时,再次打开止水夹K1,从导管a处再次缓缓鼓入空气;
③一段时间后再次称量装置D、E的总质量为204.84g。
[实验讨论]
(5)步骤①中“如下操作”是指______________________________________ ;
(6)装置B中一定发生的化学反应方程式为:________________________ ;
(7)装置B中生成CO2的质量为4.84g,通过计算说明纯碱中__________ 含NaHCO3(填字母)。_______ (写出计算过程)
A. 一定 B. 一定不 C. 可能 D. 无法确定
(8)另取10.6 g样品,加入a g 14.6%的盐酸恰好完全反应,再将所得溶液蒸干后得到固体的质量为W,当W的值满足_____________________ 条件时,样品中含有NaCl。
(一)制备探究:如图是工业生产纯碱的主要流程示意图。

[查阅资料]
①粗盐水中含有杂质MgCl2、CaCl2;
②常温下,NH3极易溶于水,CO2能溶于水,
③NaHCO3加热易分解,Na2CO3加热不易分解。
(1)写出除去粗盐水中MgCl2的化学方程式:
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是
(3)“碳酸化”后过滤获得的NH4Cl可用作氮肥,也可先加热NH4Cl溶液,再加入熟石灰获得循环使用的物质是
(4)煅烧制得纯碱的化学方程式是
(二)成分探究
[提出问题]纯碱样品中含有哪些杂质?
[猜想]
猜想一:可能含有NaHCO3; 猜想二:可能含有NaCl;猜想三:NaHCO3和NaCl
[实验探究]确定纯碱中是否含NaHCO3。实验装置和主要实验步骤如下:

①称量D、E装置总质量为200.0g,检查装置的气密性,将10.6 g纯碱试样放入锥形瓶中,按上图组装仪器,进行如下操作 ,后缓缓鼓入一段时间空气;
②按一定要求正确操作后,加入足量稀硫酸,待锥形瓶中不再产生气泡时,再次打开止水夹K1,从导管a处再次缓缓鼓入空气;
③一段时间后再次称量装置D、E的总质量为204.84g。
[实验讨论]
(5)步骤①中“如下操作”是指
(6)装置B中一定发生的化学反应方程式为:
(7)装置B中生成CO2的质量为4.84g,通过计算说明纯碱中
A. 一定 B. 一定不 C. 可能 D. 无法确定
(8)另取10.6 g样品,加入a g 14.6%的盐酸恰好完全反应,再将所得溶液蒸干后得到固体的质量为W,当W的值满足
您最近一年使用:0次



