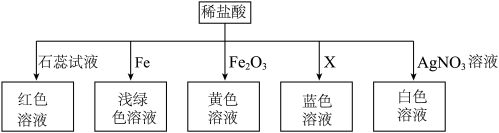
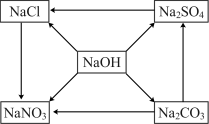
有五种化合物,它们两两之间发生的某些转化关系如下图箭头所示。请回答:__________ (填基本反应类型);这一类型反应能发生必须具备的条件之一是__________ (填一种)。
(2)写出下列转化的化学方程式:
NaOH→Na2SO4________________________________
NaCl→NaNO3________________________________ 。
(2)写出下列转化的化学方程式:
NaOH→Na2SO4
NaCl→NaNO3
更新时间:2016-11-28 13:55:42
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E是初中化学常见的物质,A是大理石的主要成分,D广泛用于玻璃、造纸、纺织和洗涤剂的生产,C转化为E的反应类型为化合反应。各物质之间的相互关系如图所示(“—”表示相邻的两种物质间能发生反应;“→表示两种物质间的转化关系;部分反应物、生成物已略去)。请回答下列问题:

(1)A的化学式为______ ,D的俗名叫______ 。
(2)C的用途为______ 。
(3)B→D发生的反应的方程式为______ ,这个反应______ (填“属于”或“不属于”)复分解反应。
(4)D和E反应的化学方程式为______ 。

(1)A的化学式为
(2)C的用途为
(3)B→D发生的反应的方程式为
(4)D和E反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列小题
(1)用相关化学用语表示:碘酒中的溶剂_____ ;侯氏制碱法中的“碱”是指_____ ;3个锰酸根离子_____ ;可用作干燥剂的氧化物是_____ 。
(2)有复合肥生成的中和反应(方程式表示)_____ 。
(3)除去氯化钠中少量的硫酸钠杂质_____ 。
(4)铝碳酸镁咀嚼片的主要成分是 ,可治疗胃酸过多症,写出其发生反应的化学方程式
,可治疗胃酸过多症,写出其发生反应的化学方程式_____ 。
(5)在四种基本反应类型中,能生成水的反应类型有(填数字)_____ 种。
(1)用相关化学用语表示:碘酒中的溶剂
(2)有复合肥生成的中和反应(方程式表示)
(3)除去氯化钠中少量的硫酸钠杂质
(4)铝碳酸镁咀嚼片的主要成分是
 ,可治疗胃酸过多症,写出其发生反应的化学方程式
,可治疗胃酸过多症,写出其发生反应的化学方程式(5)在四种基本反应类型中,能生成水的反应类型有(填数字)
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】有一包粉末,已知由BaSO4、Cu(NO3)2、BaCl2、Na2SO4、NaOH、NaCl中的几种组成。为了确定其成分,现进行以下实验:
(1)取一定量粉末,加足量水搅拌后过滤,得有色沉淀甲和无色溶液A,原粉末中一定含_____ ;
(2)向甲中加足量稀盐酸,固体全部消失并得到蓝色溶液,原粉末中一定不含_______ ;
(3)向A中加入过量BaCl2溶液,出现白色沉淀,过滤,取滤液少量滴加酚酞试液,试液变红。原粉末中一定还不含_______ ,无色溶液A至少含______ 种溶质(填数字);
(4)另取步骤③滤液加入过量稀硝酸和硝酸银,出现白色沉淀,则原粉末中_______ (选填“一定”或“可能”)含有NaCl。
(1)取一定量粉末,加足量水搅拌后过滤,得有色沉淀甲和无色溶液A,原粉末中一定含
(2)向甲中加足量稀盐酸,固体全部消失并得到蓝色溶液,原粉末中一定不含
(3)向A中加入过量BaCl2溶液,出现白色沉淀,过滤,取滤液少量滴加酚酞试液,试液变红。原粉末中一定还不含
(4)另取步骤③滤液加入过量稀硝酸和硝酸银,出现白色沉淀,则原粉末中
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化,再从剩余的浓海水中通过一系列工艺流程提取其他产品。回答下列问题:
(1)海水提取镁的一段工艺流程如下图:

浓海水的主要成分如下:
该工艺流程中需要对海水进行脱硫,原理是用钙离子沉淀硫酸根离子,产品1为______ ,过滤后干燥的产品2为氢氧化镁,该反应方程式为______ ;1L浓海水最多可得到产品2的质量为______ g。
(2)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为______ ;电解时,若有少量水存在会造成产品镁与水在高温下反应生成碱与氢气,该反应的化学方程式______ 。
(3)如下图所示:海水经过晒盐后得到粗盐和苦卤,粗盐中还含有Ca2+、Mg2+、 等可溶性杂质,以下是某化工厂进行粗盐提纯的示意图:
等可溶性杂质,以下是某化工厂进行粗盐提纯的示意图:

过量试剂①②③的顺序也可调整为______ ,过滤后可得到四种沉淀的化学式为______ ;在利用粗盐制备精盐过程中,加入适量盐酸的目的是除去溶液中含有的______ (填物质的化学式)。
(4)利用井盐和合成氨生产的氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德傍先生发明的,其氯化钠的利用率高达96%。其原理流程如下图所示:

①氨极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为氨盐水),氨盐水比食盐水更容易吸收二氧化碳,其原因是______ ;
②写出氯化铵溶液与熟石灰反应的化学方程式______ 。
(1)海水提取镁的一段工艺流程如下图:

浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- |  |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(2)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为
(3)如下图所示:海水经过晒盐后得到粗盐和苦卤,粗盐中还含有Ca2+、Mg2+、
 等可溶性杂质,以下是某化工厂进行粗盐提纯的示意图:
等可溶性杂质,以下是某化工厂进行粗盐提纯的示意图:
过量试剂①②③的顺序也可调整为
(4)利用井盐和合成氨生产的氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德傍先生发明的,其氯化钠的利用率高达96%。其原理流程如下图所示:

①氨极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为氨盐水),氨盐水比食盐水更容易吸收二氧化碳,其原因是
②写出氯化铵溶液与熟石灰反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐3】根据表中信息,请回答下列问题:
部分碱、酸、盐的溶解性表(20℃)
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“—”表示那种物质不存在或遇到水就分解了。
(1)CaCO3属于______ (填“可溶物”、”微溶物”或“不溶物”)。
(2)表中可溶于水的硫酸盐有__ 种。
(3)在溶液中,磷酸钠与氯化钙能否发生复分解反应。若能,写出化学方程式;若不能,说明理由。______
(4)某同学将盐酸倒入Ba(OH)2溶液中,得到溶液甲。

① 溶液甲中溶质的组成情况可能有______ 种。
② 实验设计:探究溶液甲中可能含有的溶质
a.探究溶液甲中是否含盐酸
b.探究溶液甲中是否含Ba(OH)2
上述三个方案中有一个不合理,请指出不合理的方案编号并说明理由:__________ 。
③ 欲从溶液甲中获得纯净的BaCl2固体,应采取的简单操作是_________ 。
部分碱、酸、盐的溶解性表(20℃)
| 阴离子 阳离子 | OH- | NO3- | Cl- | SO42- | CO32- | PO43- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | 溶 | |
| K+ | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 | 不 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 不 | 不 |
| Cu2+ | 不 | 溶 | 溶 | 溶 | — | 不 |
(1)CaCO3属于
(2)表中可溶于水的硫酸盐有
(3)在溶液中,磷酸钠与氯化钙能否发生复分解反应。若能,写出化学方程式;若不能,说明理由。
(4)某同学将盐酸倒入Ba(OH)2溶液中,得到溶液甲。

① 溶液甲中溶质的组成情况可能有
② 实验设计:探究溶液甲中可能含有的溶质
a.探究溶液甲中是否含盐酸
| 方案编号 | 实验操作 | 实验现象 |
| 1 | 取少量溶液甲于试管中,加入铁粉 | 是否 |
| 方案编号 | 实验操作 | 实验现象 |
| 2 | 取少量溶液甲于试管中,加入 | 是否产生蓝色沉淀 |
| 3 | 取少量溶液甲于试管中,加入Na2SO4溶液 | 是否产生白色沉淀 |
③ 欲从溶液甲中获得纯净的BaCl2固体,应采取的简单操作是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A~F是初中常见的化合物,有如图转化关系(部分生成物已省略)。其中A是大 理石的主要成分,C可用于灭火,F俗名纯碱。 请回答下列问题:

(1)B的化学式为__________ ,D的化学式为__________ 。
(2)E的俗名为_______ ,E与盐酸反应的化学方程式为_______ ,该反应是______ 反应(填基本反应类型)。

(1)B的化学式为
(2)E的俗名为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】已知奥运五环中A、B、C、D、E为稀硫酸、氢氧化钠溶液、二氧化碳、氧化铜、水中的一种,
且相连环内的两种物质能发生化学反应,E是常见的溶剂。请回答:

(1)B的化学式是___________ 。
(2)写出C与D反应的化学方程式___________ 。
(3)写出A与B反应的实验现象___________ 。
且相连环内的两种物质能发生化学反应,E是常见的溶剂。请回答:

(1)B的化学式是
(2)写出C与D反应的化学方程式
(3)写出A与B反应的实验现象
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】一包固体粉末,可能含有BaCl2、Na2SO4、NH4NO3、CuCl2、Ba(OH)2中的两种或多种。按照下图进行实验,出现的现象如图中所述(假设过程中所有发生的反应都恰好完全反应):

(1)气体B的化学式为______ ,该气体能使湿润的红色石蕊试纸变______ 色。
(2)写出①中生成沉淀C的一个化学方程式______ 。
(3)原固体混合物A中一定不含______ (写化学式);无色溶液D中一定存在的酸根阴离子是______ 。
(4)通过上述实验现象还不能确定混合物A中存在的物质是______ ,若想进一步判断该物质是否存在,可用溶液D再进行实验,请你设计实验方案,简述操作步骤、实验现象及结论:______ 。

(1)气体B的化学式为
(2)写出①中生成沉淀C的一个化学方程式
(3)原固体混合物A中一定不含
(4)通过上述实验现象还不能确定混合物A中存在的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】溶液是生产生活中常见的物质,依据相关信息回答问题:
(1)在抗击新冠肺炎战“疫"中,使用的75%酒精溶液的溶质是__________ 。
(2)资料:硝酸钾的溶解度数据(部分数据已做取整数处理)见下表。
A、B、C、D四个烧杯中分别盛有100 g水,在40℃时,向四个烧杯中分别加入110 g、86 g、64 g、32 g硝酸钾,充分溶解。

①烧杯________ (选填字母序号)中一定是饱和溶液。
②若使B烧杯的溶液升温至50℃时,溶液的质量为____________ g。
③若采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是________ (填字母序号)。
a 溶剂质量可能都相等
b 溶质质量都不相等
c 溶质的溶解度可能都相等
d 烧杯A中溶质的质量分数可能最大
(3)为测定某工业废水中硫酸铜的含量进行如图所示的实验。

①生成沉淀的质量是_____________ g。
②计算原废水中硫酸铜的质量分数为_______ 。
(1)在抗击新冠肺炎战“疫"中,使用的75%酒精溶液的溶质是
(2)资料:硝酸钾的溶解度数据(部分数据已做取整数处理)见下表。
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
A、B、C、D四个烧杯中分别盛有100 g水,在40℃时,向四个烧杯中分别加入110 g、86 g、64 g、32 g硝酸钾,充分溶解。

①烧杯
②若使B烧杯的溶液升温至50℃时,溶液的质量为
③若采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是
a 溶剂质量可能都相等
b 溶质质量都不相等
c 溶质的溶解度可能都相等
d 烧杯A中溶质的质量分数可能最大
(3)为测定某工业废水中硫酸铜的含量进行如图所示的实验。

①生成沉淀的质量是
②计算原废水中硫酸铜的质量分数为
您最近一年使用:0次