“五一”假期,某化学兴趣小组对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】A.可能与硫酸的质量分数有关;B.可能与锌的颗粒大小有关
【设计并实验】用不同质量分数的硫酸和不同颗粒大小的锌进行如下实验。
(1)写出稀硫酸与锌反应的化学方程式___________________________________ 。
(2)【收集证据】要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是_________ 。
(3)【得出结论】完成①②③三组实验后得出的结论是___________ 。
(4)【评价与反思】下表是第①组实验的详细数据。
从上述表格可知,从第3 分钟开始反应的速度减慢,其原因是___________________ 。
(5)由于没有及时记录数据,导致第④组实验数据丢失,经同组同学回忆,得到以下数据,你认为可能的是______。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】A.可能与硫酸的质量分数有关;B.可能与锌的颗粒大小有关
【设计并实验】用不同质量分数的硫酸和不同颗粒大小的锌进行如下实验。
| 实验编号 | 硫酸的质量分数 (均取20mL) | 锌的颗粒大小 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌粒 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌粉 |
(2)【收集证据】要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是
(3)【得出结论】完成①②③三组实验后得出的结论是
(4)【评价与反思】下表是第①组实验的详细数据。
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| 氢气的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
(5)由于没有及时记录数据,导致第④组实验数据丢失,经同组同学回忆,得到以下数据,你认为可能的是______。
| A.45.7 | B.54.7 | C.75.4 |
更新时间:2016-11-28 14:03:02
|
相似题推荐
【推荐1】酸碱盐在学习、生活中发挥着重要作用。
(1)现有一根铝丝和一根银丝,用下列哪种试剂可以鉴别________ 。
①氯化钠 ②硫酸铜 ③硝酸镁
(2)已知金属铝可以和氢氧化钠、水反应生成偏铝酸钠(NaAlO2)和氢气,试写出该反应的化学方程式________ 。铝粉和氢氧化钠混合物常用于疏通管道,一方面是因为氢氧化钠可以腐蚀油脂及毛发而不腐蚀管道,另一个原因是________ 。
(3)某小组测定实验室里一瓶久置的氢氧化钠固体是否变质,进行了如下实验探究:
【提出问题】
猜想Ⅰ:没变质;
猜想Ⅱ:完全变质,全部是碳酸钠;
猜想Ⅲ:部分变质,既含有氢氧化钠又含有碳酸钠。
【设计方案并进行实验】
【实验结论】通过实验,说明上述猜想_______ 是正确的。
【反思】久置氢氧化钠变质的原因是_______ (用化学方程式表示)。
(4)根据步骤①中数据,计算出NaOH的质量为______ g。
(1)现有一根铝丝和一根银丝,用下列哪种试剂可以鉴别
①氯化钠 ②硫酸铜 ③硝酸镁
(2)已知金属铝可以和氢氧化钠、水反应生成偏铝酸钠(NaAlO2)和氢气,试写出该反应的化学方程式
(3)某小组测定实验室里一瓶久置的氢氧化钠固体是否变质,进行了如下实验探究:
【提出问题】
猜想Ⅰ:没变质;
猜想Ⅱ:完全变质,全部是碳酸钠;
猜想Ⅲ:部分变质,既含有氢氧化钠又含有碳酸钠。
【设计方案并进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品7.3g溶于水配成溶液,向溶液中滴加中性氯化钡溶液至过量,充分反应,静置 | 产生白色沉淀9.85g | |
| ②取反应后的溶液少量于试管中,滴加几滴酚酞 | 溶液变红 |
【实验结论】通过实验,说明上述猜想
【反思】久置氢氧化钠变质的原因是
(4)根据步骤①中数据,计算出NaOH的质量为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】我县某学校化学兴趣小组在学习金属的化学性质实验操作时,发现几支试管中产生气泡有快有慢,于是该兴趣小组的同学们一起合作进行了如下探究。
【提出问题】金属与酸反应的快慢受哪些因素影响?
【猜想与假设】猜想1:可能与酸的浓度有关;
猜想2:可能与金属的种类有关;
猜想3:可能与金属的形状有关。
【设计并实验】为了验证猜想,同学们设计了如图1所示的装置进行如下实验:
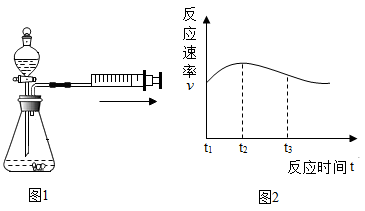
(1)同学们检查图1装置气密性的方法是关闭分液漏斗活塞,用力将注射器活塞外拉(右移)一段距离,停止用力后松手,若观察到活塞缓慢回到原位置,则气密性______ (填“好”或“差”);
(2)实验时需将镁片和铁片进行打磨,其目的是_________ ;
(3)写出铁与稀硫酸反应的化学方程式:________ ;
【收集证据】
(4)要比较金属的形状对反应快慢的影响,应选择的实验编号是_______ ;
【得出结论】
(5)从上述实验数据可得出的结论是________ ;(任写一条即可)
【评价与反思】
(6)测得实验①反应中产生气体的速率(v)与时间(t)的关系如图2所示,你认为在t1-t2时间段内反应速率逐渐加快的原因是__________ ,t2-t3时间段内反应速率逐渐减慢的主要原因是_________ ;
【拓展与应用】
(7)铁与硫酸反应的快慢还受到温度的影响,请你设计实验验证:___________ 。
【提出问题】金属与酸反应的快慢受哪些因素影响?
【猜想与假设】猜想1:可能与酸的浓度有关;
猜想2:可能与金属的种类有关;
猜想3:可能与金属的形状有关。
【设计并实验】为了验证猜想,同学们设计了如图1所示的装置进行如下实验:

| 实验编号 | 硫酸的浓度 (均取20ml) | 金属 (均取2g) | 金属的形状 | 收集50mL H2 所需时间/s |
| ① | 10% | 镁 | 粉末 | 60 |
| ② | 10% | 铁 | 片状 | 120 |
| ③ | 10% | 镁 | 片状 | 102 |
| ④ | 20% | 铁 | 片状 | 110 |
(1)同学们检查图1装置气密性的方法是关闭分液漏斗活塞,用力将注射器活塞外拉(右移)一段距离,停止用力后松手,若观察到活塞缓慢回到原位置,则气密性
(2)实验时需将镁片和铁片进行打磨,其目的是
(3)写出铁与稀硫酸反应的化学方程式:
【收集证据】
(4)要比较金属的形状对反应快慢的影响,应选择的实验编号是
【得出结论】
(5)从上述实验数据可得出的结论是
【评价与反思】
(6)测得实验①反应中产生气体的速率(v)与时间(t)的关系如图2所示,你认为在t1-t2时间段内反应速率逐渐加快的原因是
【拓展与应用】
(7)铁与硫酸反应的快慢还受到温度的影响,请你设计实验验证:
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】同学们对CO2是否支持常见金属的燃烧进行了如下探究活动:
【活动一】探究CO2是否支持实验室常见金属镁的燃烧
实验①:将燃着的镁条插入充满CO2的集气瓶中,发现镁条仍在燃烧。生成一种金属氧化物和一种非金属单质。
(1)镁在CO2中反应的化学方程式为______________________________________
(2)实验①的结论是____________________________________
由该结论可知__________ (填“能”或“不能”)用CO2灭火器扑灭金属镁的火灾。
(3)通过实验①,你对燃烧条件的新认识是_____________________________
【活动二】探究CO2是否支持实验室常见金属铁的燃烧
实验②:将弯成螺旋状的细铁丝系上一支火柴,点燃火柴后立即将铁丝插入装有CO2的集气瓶中,发现铁丝未燃烧。
(1)将细铁丝弯成螺旋状的目的是______________________________________
(2)小刚同学提出:如果实验②中细铁丝未得到充分加热,将对判断“CO2是否支持铁的燃烧”造成干扰。他依据什么认为实验②中细铁丝未得到充分加热?____________________________
请你帮助他设计对比试验,排除干扰因素,证明CO2是否支持铁的燃烧。
【活动一】探究CO2是否支持实验室常见金属镁的燃烧
实验①:将燃着的镁条插入充满CO2的集气瓶中,发现镁条仍在燃烧。生成一种金属氧化物和一种非金属单质。
(1)镁在CO2中反应的化学方程式为
(2)实验①的结论是
由该结论可知
(3)通过实验①,你对燃烧条件的新认识是
【活动二】探究CO2是否支持实验室常见金属铁的燃烧
实验②:将弯成螺旋状的细铁丝系上一支火柴,点燃火柴后立即将铁丝插入装有CO2的集气瓶中,发现铁丝未燃烧。
(1)将细铁丝弯成螺旋状的目的是
(2)小刚同学提出:如果实验②中细铁丝未得到充分加热,将对判断“CO2是否支持铁的燃烧”造成干扰。他依据什么认为实验②中细铁丝未得到充分加热?
请你帮助他设计对比试验,排除干扰因素,证明CO2是否支持铁的燃烧。
| 实验方法 | 可能观察到的现象和结论 |
| 如果铁丝在装有O2和CO2的集气瓶中都燃烧,证明CO2支持铁的燃烧 | |
| 如果铁丝在装有O2的集气瓶中燃烧,在装CO2的集气瓶中逐渐冷却,证明CO2不支持铁的燃烧 |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】为探究锌、铜、镍三种金属的性质,某兴趣小组进行如下实验
【实验一】取粗细、长短相同的锌丝、铜丝、镍丝均与50mL稀盐酸反应,实验记录如下:
(1)经查阅资料得知镍与稀盐酸反应生成氯化镍(NiC12)和氢气,则镍与稀盐酸反应的化学方程式是______ ,并根据已学的知识分析得出铜不能与稀盐酸发生化学反应的原因是______ 。
(2)要判断三种金属的活动性强弱,另取一根粗细、长短相同的锌丝放入50mL质量分数为____ 的稀盐酸中,观察放出气泡的快慢。小组最后得出锌的活动性最强。
(3)实验时,有同学建议先用砂纸将三种金属丝表面进行打磨,目的是_______ 。
【实验二】
(4)同学又设计了表格中的实验,成功的验证了三种金属的活动性强弱。填写表中空白:
【拓展延伸】
(5)为了回收利用金属,同学们将实验一反应后的溶液倒入同一容器中,向其中加入少量的铝粉,充分反应后过滤,则滤渣中一定含有的金属为______ 。(填名称)
【实验一】取粗细、长短相同的锌丝、铜丝、镍丝均与50mL稀盐酸反应,实验记录如下:
| 锌 | 铜 | 镍 | 铜 | |
| 稀盐酸的质量分数 | 3% | 3% | 15% | 15% |
| 反应现象 | 少量气泡 | 无现象 | 许多气泡 | 无现象 |
(2)要判断三种金属的活动性强弱,另取一根粗细、长短相同的锌丝放入50mL质量分数为
(3)实验时,有同学建议先用砂纸将三种金属丝表面进行打磨,目的是
【实验二】
(4)同学又设计了表格中的实验,成功的验证了三种金属的活动性强弱。填写表中空白:
| 实验步骤 | 实验现象 |
| 把镍浸入到 | 表面有红色固体出现 |
| 把镍浸入到硫酸锌溶液中 |
【拓展延伸】
(5)为了回收利用金属,同学们将实验一反应后的溶液倒入同一容器中,向其中加入少量的铝粉,充分反应后过滤,则滤渣中一定含有的金属为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】铁锈蚀会造成资源浪费,但生活中人们却能善于利用铁锈蚀的原理,将“害”转化为“利”,研制出好产品,如用于食品保鲜的双吸剂、冬天取暖使用的“暖宝宝”等。某化学兴趣小组对铁锈蚀的原理及应用进行了探究。
【查阅资料】
①某品牌双吸剂的成分为:还原铁粉(有疏松多孔的结构)。
②某品牌暖宝宝的成分为:铁粉(主要成分)、活性炭、蛭石、吸水性树脂、食盐。
③蛭石:一种天然矿物,加工后具有极强的保温隔热性能。吸水性树脂:一种新型高分子材料,吸水能力强,可反复吸收水、释放水。
[实验 1]
图 1 是教材中铁的锈蚀实验装置图,实验一段时间后观察到导管内有一段液柱上升。同学们在第二课堂活动中,用等量还原铁粉代替细铁丝,按图 1 所示装置进行实验,在较短时间内就观察到烧杯中的溶液倒吸入锥形中。
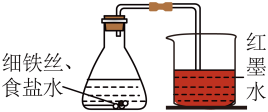
(1)实验中,铁钉生锈的其中一步反应是铁与氧气、水共同作用生成氢氧化亚铁[ Fe(OH)2 ], 该反应的化学方程式为____ 。
(2)用还原铁粉代替细铁丝进行实验,造成水倒吸速度变快的原因是____ 。该实验____ (填“能”或“不能”)用于测定空气中氧气的体积分数。
[实验 2]
化学小组设计如图 2 所示的实验装置,三颈烧瓶内装入少量水和某品牌暖宝宝 5g,测量时间为 1100s。用温度传感器(图 3)、氧气浓度传感器(图 4)和湿度传感器(图 5)采集的数据如下:
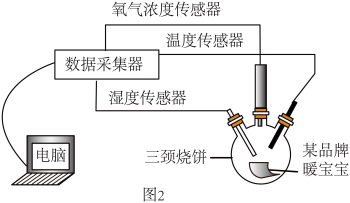


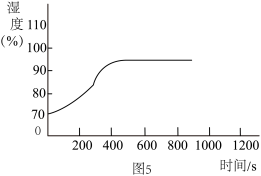
(3)结合图 4 分析,实验 1 中(图 1)导管内水柱上升的原因是____ 。
(4)结合图 5 分析,造成湿度逐渐增大的原因可能与____ 有关。
[实验 3]
化学小组继续探究“暖宝宝”能较快且持续放热的原因。
(5)对比实验①和实验②:暖宝宝成分中的____ 显著加快了铁粉锈蚀的速率。
(6)暖宝宝成分中蛭石的作用是____ 。
【交流反思】
(7)请你设计一个实验方案,验证使用后的“暖宝宝”是否还含有铁粉(写出实验步骤和预期的现象)____ 。
【查阅资料】
①某品牌双吸剂的成分为:还原铁粉(有疏松多孔的结构)。
②某品牌暖宝宝的成分为:铁粉(主要成分)、活性炭、蛭石、吸水性树脂、食盐。
③蛭石:一种天然矿物,加工后具有极强的保温隔热性能。吸水性树脂:一种新型高分子材料,吸水能力强,可反复吸收水、释放水。
[实验 1]
图 1 是教材中铁的锈蚀实验装置图,实验一段时间后观察到导管内有一段液柱上升。同学们在第二课堂活动中,用等量还原铁粉代替细铁丝,按图 1 所示装置进行实验,在较短时间内就观察到烧杯中的溶液倒吸入锥形中。

(1)实验中,铁钉生锈的其中一步反应是铁与氧气、水共同作用生成氢氧化亚铁[ Fe(OH)2 ], 该反应的化学方程式为
(2)用还原铁粉代替细铁丝进行实验,造成水倒吸速度变快的原因是
[实验 2]
化学小组设计如图 2 所示的实验装置,三颈烧瓶内装入少量水和某品牌暖宝宝 5g,测量时间为 1100s。用温度传感器(图 3)、氧气浓度传感器(图 4)和湿度传感器(图 5)采集的数据如下:




(3)结合图 4 分析,实验 1 中(图 1)导管内水柱上升的原因是
(4)结合图 5 分析,造成湿度逐渐增大的原因可能与
[实验 3]
化学小组继续探究“暖宝宝”能较快且持续放热的原因。
| 实验 | 药品 | 现象 |
| ① | 铁粉(12g)、空气、10%NaCl 溶液 | 200s 时,温度升高到 35.9℃,但不能保持 |
| ② | 铁粉(12g)、空气、10%NaCl 溶液、活性炭(8g) | 200s 时,温度升高到 46.4℃,但不能保持 |
| ③ | 暖宝宝成分(12g) | 200s 时,温度升高到 60℃,并长时间保持 |
(6)暖宝宝成分中蛭石的作用是
【交流反思】
(7)请你设计一个实验方案,验证使用后的“暖宝宝”是否还含有铁粉(写出实验步骤和预期的现象)
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】某化学兴趣小组在实验室里探究某些酸碱盐的化学性质,分别做了如下实验:
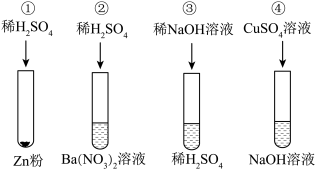
(1)实验①的反应现象是___________ 。
(2)实验④反应的化学方程式为___________ 。
(3)向试管③中滴加了过量的氢氧化钠溶液仍无明显现象,要证明二者已经发生反应,可选用___________(填字母)继续进行实验,以达到实验目的。
(4)小组同学将实验②③④三支试管反应后的物质倒入同一洁净的烧杯中,充分反应后过滤,分别得到沉淀A和无色滤液B。
I.沉淀A的成分是___________ 。(填化学式)
Ⅱ.同学们对无色滤液B继续进行实验,取滤液B于试管,加入足量Ba(NO3)2溶液,无明显现象,由此现象说明滤液B中一定没有的离子是___________ (填离子符号)。同学们经过讨论认为无色滤液B中离子的种类可能有多种情况,你认为溶液中最多含有的离子有___________ (填离子符号)。

(1)实验①的反应现象是
(2)实验④反应的化学方程式为
(3)向试管③中滴加了过量的氢氧化钠溶液仍无明显现象,要证明二者已经发生反应,可选用___________(填字母)继续进行实验,以达到实验目的。
| A.酚酞 | B.氯化钡溶液 | C.pH试纸 | D.碳酸钾溶液 |
I.沉淀A的成分是
Ⅱ.同学们对无色滤液B继续进行实验,取滤液B于试管,加入足量Ba(NO3)2溶液,无明显现象,由此现象说明滤液B中一定没有的离子是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】把足量锌粒加入装有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应过程中,溶液的温度也先随之升高,最后下降到室温。于是,同学们设计实验来探究“一定质量的锌粒和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
一定质量的锌粒与同体积盐酸溶液反应实验数据表
(1)锌粒和盐酸反应的化学化学方程式为_______________________ 。
(2)分析实验数据得出:一定质量的锌粒和同体积盐酸反应,影响锌和酸反应快慢的主要因素有_________ 、_________ 。
(3)可以通过比较________ 实验数据来确定锌和酸反应的快慢。
(4)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快原因_____________ 。
一定质量的锌粒与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10 mL | 60 mL |
| 10% | 20℃ | 19 mL | 118 mL |
| 15% | 20℃ | 28 mL | 175 mL |
| 5% | 35℃ | 28 mL | 60 mL |
| 10% | 35℃ | 72 mL | 118 mL |
| 15% | 35℃ | 103 mL | 175 mL |
(1)锌粒和盐酸反应的化学化学方程式为
(2)分析实验数据得出:一定质量的锌粒和同体积盐酸反应,影响锌和酸反应快慢的主要因素有
(3)可以通过比较
(4)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快原因
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐2】鱼浮灵【主要成分是过碳酸钠(2Na2CO3·3H2O2)】是水产养殖中常见的增氧剂,溶于水后生成Na2CO3和H2O2,能迅速增加水体溶氧量,某课外小组用如图装置探究促进H2O2分解的因素。
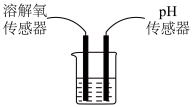
【查阅资料】H2O2常温下分解很慢。
NaCl溶于水解离出Na+和Cl-。
Na2CO3溶于水解离出Na+和CO32-,CO32-与水作用使溶液呈碱性。
【猜想与假设】①.Na+促进H2O2分解。②.溶液的碱性促进H2O2分解。
【进行实验】
探究一:分别进行下列3个实验(80mL蒸馏水中加入6.7g“鱼浮灵”,所得溶液中H2O2的浓度约为4%)。
【解释与结论】
(1)根据实验1的实验结果,加入“鱼浮灵”后,液体的变化是______ 。
(2)通过实验______ ,证明猜想1不成立。
(3)证明猜想2成立的依据是______ 。
探究二:向5个烧杯中分别加入80mL4%的H2O2溶液,再分别滴加NaOH溶液,测得不同pH下的溶解氧情况如下表所示。
(4)探究二得出的结论是______ 。
【反思与评价】
(5)下列物质能加快H2O2分解的是_______ 。
A MnO2 B NaCl C NaOH D Na2CO3
(6)探究一中,实验2-①与实验1-①对比,溶解氧增大的原因是______ 。

【查阅资料】H2O2常温下分解很慢。
NaCl溶于水解离出Na+和Cl-。
Na2CO3溶于水解离出Na+和CO32-,CO32-与水作用使溶液呈碱性。
【猜想与假设】①.Na+促进H2O2分解。②.溶液的碱性促进H2O2分解。
【进行实验】
探究一:分别进行下列3个实验(80mL蒸馏水中加入6.7g“鱼浮灵”,所得溶液中H2O2的浓度约为4%)。
| 实验 | 实验内容 | 实验结果 | |
| pH | 溶解氧(mg/L) | ||
| 1 | ① 80 mL蒸馏水 | 6.96 | 5.68 |
| ② 加“鱼浮灵”6.7g | 9.89 | 7.97 | |
| 2 | ① 80 mL 4%的H2O2溶液 | 6.01 | 6.44 |
| ② 加少量NaCl | 6.00 | 6.46 | |
| ③ 再加少量Na2CO3 | 8.14 | 9.11 | |
| 3 | 80 mL 4%的H2O2溶液中加少量NaOH溶液 | 9.26 | 10.97 |
【解释与结论】
(1)根据实验1的实验结果,加入“鱼浮灵”后,液体的变化是
(2)通过实验
(3)证明猜想2成立的依据是
探究二:向5个烧杯中分别加入80mL4%的H2O2溶液,再分别滴加NaOH溶液,测得不同pH下的溶解氧情况如下表所示。
| 烧杯 | 1 | 2 | 3 | 4 | 5 |
| pH | 8.00 | 8.59 | 9.29 | 10.43 | 11.47 |
| 溶解氧(mg/L) | 6.88 | 9.30 | 13.82 | 17.57 | 13.15 |
(4)探究二得出的结论是
【反思与评价】
(5)下列物质能加快H2O2分解的是
A MnO2 B NaCl C NaOH D Na2CO3
(6)探究一中,实验2-①与实验1-①对比,溶解氧增大的原因是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】同学们在实验室用高锰酸钾制取氧气。实验后,同学们发现沾有高锰酸钾的白抹布洗完晾干后变为棕褐色。
【查阅资料】草酸溶液能将棕褐色物质除去。
【提出问题】哪些因素能加快草酸除去棕褐色物质的速率?
【进行实验】将均匀染有棕褐色的抹布剪成大小相同的小布条进行实验
【解释与结论】
(1)配制200g溶质质量分数为0.5%的草酸溶液,需要草酸的质量为______ 。
(2)实验1的目的是______ 。
(3)证明升高温度能加快草酸除去棕褐色物质的速率,需要对比______ (填实验序号)。
(4)由实验2、3、4可以得出的结论是______ 。
【反思与评价】
(5)实验后,同学们查资料得知抹布上的棕褐色物质为二氧化锰,请你设计实验方案进行验证。
_____________________________ 。
【查阅资料】草酸溶液能将棕褐色物质除去。
| 实验编号 | 实验1 20℃ 水  | 实验2 20℃ 0.5%草酸溶液  | 实验3 20℃ 0.25%草酸溶液  | 实验4 20℃ 0.125%草酸溶液  | 实验5 30℃ 0.25%草酸溶液  | 实验6 40℃ 0.25%草酸溶液  |
| 现象 | 颜色没有褪去 | 70秒后颜色褪去 | 98秒后颜色褪去 | 150秒后颜色褪去 | 51秒后颜色褪去 | 40秒后颜色褪去 |
【提出问题】哪些因素能加快草酸除去棕褐色物质的速率?
【进行实验】将均匀染有棕褐色的抹布剪成大小相同的小布条进行实验
【解释与结论】
(1)配制200g溶质质量分数为0.5%的草酸溶液,需要草酸的质量为
(2)实验1的目的是
(3)证明升高温度能加快草酸除去棕褐色物质的速率,需要对比
(4)由实验2、3、4可以得出的结论是
【反思与评价】
(5)实验后,同学们查资料得知抹布上的棕褐色物质为二氧化锰,请你设计实验方案进行验证。
您最近一年使用:0次



