绍兴市获得2015年度全省“五水共治”工作优秀市并被授予大禹鼎,“五水共治”是指治污水、防洪水、排涝水、保供水、抓节水,还社会一个蓝天碧水,为百姓创造美好的生活环境。
某化工厂流程会产生澄清废水,其中可能含有的离子是Ag+、Cu2+、Cl﹣、NO3﹣,已知:白色的沉淀Fe(OH)2在空气中会迅速转化为红褐色的Fe(OH)3。
(1)取少量废水,加入过量稀盐酸,产生白色沉淀;再加入过量氢氧化钠溶液,产生蓝色沉淀。该废水中含有的金属离子是_____________ 。
(2)兴趣小组设计了一个除去该废水中原有金属离子的实验方案,部分流程如图所示。

操作I的名称是_______ ,单质A是_______ 。
某化工厂流程会产生澄清废水,其中可能含有的离子是Ag+、Cu2+、Cl﹣、NO3﹣,已知:白色的沉淀Fe(OH)2在空气中会迅速转化为红褐色的Fe(OH)3。
(1)取少量废水,加入过量稀盐酸,产生白色沉淀;再加入过量氢氧化钠溶液,产生蓝色沉淀。该废水中含有的金属离子是
(2)兴趣小组设计了一个除去该废水中原有金属离子的实验方案,部分流程如图所示。

操作I的名称是
2016九年级·浙江绍兴·学业考试 查看更多[3]
更新时间:2016-11-28 14:05:23
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】氧化锌是一种常用的化工原料,俗称“锌白”。工业级粗氧化锌(含有FeO、MnO、NiO等杂质)提纯为“锌白”的流程如图所示(已知:步骤①中,金属氧化物与硫酸反应生成盐和水)。请回答下列问题。

(1)步骤①中,ZnO与稀硫酸反应的化学方程式为______ ;步骤②中元素的化合价发生变化的是______ 、______ (填元素符号)。
(2)步骤③中除去杂质的化学方程式为______ ,该反应类型为______ 反应。
(3)从流程分析Zn2(OH)2CO3在水中的溶解性属于______ (选填“易溶”“可溶”或“难溶”)。
(4)反应⑤的化学方程式为: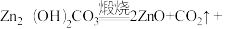
______ ;从“碳达峰”和“碳中和”角度考虑,处理二氧化碳最好的措施是______ 。

(1)步骤①中,ZnO与稀硫酸反应的化学方程式为
(2)步骤③中除去杂质的化学方程式为
(3)从流程分析Zn2(OH)2CO3在水中的溶解性属于
(4)反应⑤的化学方程式为:
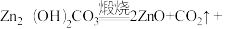
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】从铜、氧化铜的混合粉末中回收铜的具体流程如下:

回答下列问题:
(1)混合粉末加入过量稀硫酸反应的化学方程式为_________ 。
(2)操作Ⅰ用到的玻璃仪器有烧杯、玻璃棒和________ 。
(3)滤渣Ⅱ中除了含铜还含有_______ ,试剂A为稀硫酸,其作用是________ 。

回答下列问题:
(1)混合粉末加入过量稀硫酸反应的化学方程式为
(2)操作Ⅰ用到的玻璃仪器有烧杯、玻璃棒和
(3)滤渣Ⅱ中除了含铜还含有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】普通立德粉(BaSO4·ZnS)广泛用于工业生产中,以粗氧化锌(含Zn、CuO、FeO等杂质)和BaS为原料制备立德粉的流程如下:
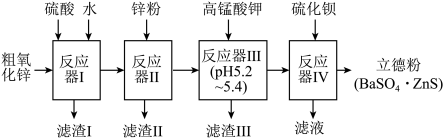
(1)生产ZnSO4的过程中,反应器Ⅰ要保持强制通风,原因是_______ 。
(2)滤渣Ⅱ可回收的金属主要为_______ 。
(3)配平反应器Ⅲ中反应的化学方程式______________ 。
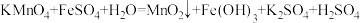
(4)普通立德粉(BaSO4·ZnS)中ZnS含量为29.4%,高品质银印级立德粉中ZnS含量为62.5%。(已知BaSO4、ZnS的相对分子质量分别为233、97)
①银印级立德粉的化学式为_______ 。
②从ZnSO4、Na2SO4、BaS和Na2S中选取三种物质,经过一步反应制备银印级立德粉,反应的化学方程式为_______ 。

(1)生产ZnSO4的过程中,反应器Ⅰ要保持强制通风,原因是
(2)滤渣Ⅱ可回收的金属主要为
(3)配平反应器Ⅲ中反应的化学方程式
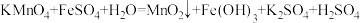
(4)普通立德粉(BaSO4·ZnS)中ZnS含量为29.4%,高品质银印级立德粉中ZnS含量为62.5%。(已知BaSO4、ZnS的相对分子质量分别为233、97)
①银印级立德粉的化学式为
②从ZnSO4、Na2SO4、BaS和Na2S中选取三种物质,经过一步反应制备银印级立德粉,反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】合理处理和利用工厂的“三废”是环境治理的重要举措。某化工厂用废硫酸制备K2SO4的流程如下:

(1)生产上将CaCO3研成粉末的目的是______ 。
(2)上述流程中,除可综合利用CO2外,还可循环使用的物质是______ (填写化学式)。
(3)洗涤反应③所得晶体,不用水而用饱和K2SO4溶液的目的是______ ;检验此晶体是否洗涤干净的方法是______ 。

(1)生产上将CaCO3研成粉末的目的是
(2)上述流程中,除可综合利用CO2外,还可循环使用的物质是
(3)洗涤反应③所得晶体,不用水而用饱和K2SO4溶液的目的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某学校研究小组从废干电池筒内的物质(含有C、MnO2、ZnCl2、NH4Cl等)进行回收MnO2实验,过程如下:
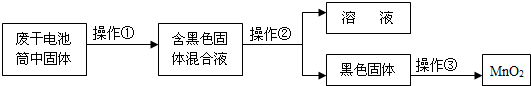
(1)操作①、②、③依次为下图中的____________ 。(填字母)
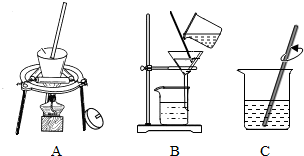
(2)操作②后要进行洗涤,判断洗净的方法是:取最后6次洗涤液,加入________ 溶液,如果不生成白色沉淀,则说明已洗净。操作③中发生反应的化学方程式为________ 。
(3)为检验获得的MnO2,可在试管中加入获得的MnO2和适量的过氧化氢溶液混合,反应化学方程式为__________ ,在试管口用________ 检验生成的气体。

(1)操作①、②、③依次为下图中的

(2)操作②后要进行洗涤,判断洗净的方法是:取最后6次洗涤液,加入
(3)为检验获得的MnO2,可在试管中加入获得的MnO2和适量的过氧化氢溶液混合,反应化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有一包白色粉末,其中含有CuSO4、BaCl2、NaOH、Na2CO3中的一种或几种。某化学小组为确定白色粉末的成分,进行了如下实验:(Ⅰ)取一定量白色粉末,加入足量水,振荡,得到无色透明溶液;(Ⅱ)取少量(Ⅰ)的溶液,加入足量盐酸,有气泡产生。(提示:BaCO3难溶于水;Na2CO3的水溶液呈碱性)
(1)该白色粉末中肯定含有什么物质?可能含有什么物质?
(2)为确定可能含有的物质是否存在,还需做什么实验?请写出简要的实验步骤。
(1)该白色粉末中肯定含有什么物质?可能含有什么物质?
(2)为确定可能含有的物质是否存在,还需做什么实验?请写出简要的实验步骤。
您最近一年使用:0次



