重质碳酸钙粉体产业为我市一大支柱产业,产品远销全国各地。某化学兴趣小组对粉体中碳酸钙含量进行了探究,小组成员从一包粉体产品中取出样品5.10g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不参与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如表所示。
(1)碳酸钙的相对分子质量为____;
(2)表中m=_____;
(3)求样品中碳酸钙的质量分数(结果保留两位小数)?
| 稀盐酸的总质量(g) | 10.00 | 20.00 | 30.00 | 40.00 | 50.00 | 60.00 | 70.00 |
| 烧杯中物质总质量(g) | 14.66 | 24.22 | m | 43.34 | 52.90 | 62.90 | 72.90 |
(1)碳酸钙的相对分子质量为____;
(2)表中m=_____;
(3)求样品中碳酸钙的质量分数(结果保留两位小数)?
2016·广西贺州·中考真题 查看更多[6]
2016年初中毕业升学考试(广西贺州卷)化学2017年秋人教版九年级上册化学:第六单元 碳和碳的氧化物-单元清检测广东省揭阳市揭西县第三华侨中学2019届九年级上学期期中考试化学试题(已下线)第6单元 碳和碳的氧化物(检测卷)-2020-2021学年九年级化学上册同步课堂课件精讲及好题精练(人教版)2017年湖北省黄石市大冶市鹏程中学中考三模化学试题2022年广西贺州市富川瑶族自治县第三中学中考模拟化学试题
更新时间:2016-11-28 06:11:45
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】小明用含有铜粉和氧化铜粉末的样品进行了如图所示的实验。
(1)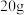 样品中氧化铜的质量为
样品中氧化铜的质量为_______ g。
(2)求稀硫酸中溶质质量分数。

(1)
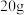 样品中氧化铜的质量为
样品中氧化铜的质量为(2)求稀硫酸中溶质质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。根据以下信息计算:

(1)生成二氧化碳的质量为_____ g:
(2)样品中碳酸钙的质量分数是多少?
(3)C烧杯中溶液的溶质的质量分数是多少?

(1)生成二氧化碳的质量为
(2)样品中碳酸钙的质量分数是多少?
(3)C烧杯中溶液的溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
解题方法
【推荐3】将34.6g氯酸钾和氯化钾的混合物充分加热至质量不变,收集到9.6g氧气。
(1)求上述混合物中氯酸钾的质量。
(2)将反应后的固体溶于一定量水,配成100g溶液,求该溶液的溶质质量分数。
(3)将(2)的溶液降温至20℃,通过计算判断有无晶体析出(20℃时,氯化钾的溶解度为34g)。
(1)求上述混合物中氯酸钾的质量。
(2)将反应后的固体溶于一定量水,配成100g溶液,求该溶液的溶质质量分数。
(3)将(2)的溶液降温至20℃,通过计算判断有无晶体析出(20℃时,氯化钾的溶解度为34g)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】某混合物中含有碳酸钙和氯化钙,取该混合物6g,向其中加入61.7g稀盐酸,恰好完全反应,产生2.2g气体(假设气体全部逸出)。计算:
(1)该混合物中碳酸钙的质量为___________ ;
(2)反应后所得到的不饱和溶液中溶质的质量分数。
(1)该混合物中碳酸钙的质量为
(2)反应后所得到的不饱和溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】实验室高温煅烧125g含CaCO380%的石灰石(杂质不分解也不与酸反应),一段时间后,停止实验,冷却后用剩余的固体处理废盐酸。问能否处理含70gHCl的废盐酸,请写出计算过程。__________________
已知:CaCO3 CaO+ CO2↑
CaO+ CO2↑
CaO+2HCl=CaCl2+H2O
Ca(OH)2+2HCl=CaCl2+2H2O
已知:CaCO3
 CaO+ CO2↑
CaO+ CO2↑CaO+2HCl=CaCl2+H2O
Ca(OH)2+2HCl=CaCl2+2H2O
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某项目学习小组对实验室制取二氧化碳后过滤所得的废液进行探究。取100g该废液,逐滴加入碳酸钠溶液,测得产生沉淀的质量如图所示,请回答:

(1)由图可知,废液呈___________ 性,可用___________ 测定其pH.
(2)充分反应后生成碳酸钙的质量为___________ g。
(3)计算该废液中氯化钙的质量分数。(写出计算过程)
(4)用氧化钙、氢氧化钙和碳酸钙都可将该废液中的盐酸除去,获得氯化钙溶液,比较处理等质量的该废液,需这三种物质的质量由小到大的顺序为___________ (用物质名称填空)。

(1)由图可知,废液呈
(2)充分反应后生成碳酸钙的质量为
(3)计算该废液中氯化钙的质量分数。(写出计算过程)
(4)用氧化钙、氢氧化钙和碳酸钙都可将该废液中的盐酸除去,获得氯化钙溶液,比较处理等质量的该废液,需这三种物质的质量由小到大的顺序为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】下图是某品牌补铁片标签上的部分文字说明,该补铁片的主要成分是硫酸亚铁,其它成分不含铁元素。计算:

(1)硫酸亚铁的相对分子质量(列式计算)。
(2)硫酸亚铁中铁、硫、氧三种元素质量比 (列式计算,化成最简整数比)。
(3)硫酸亚铁中铁元素质量分数列式计算,保留0.1%)。
(4)该补铁片中铁元素的质量分数(保留0.1%)(写出计算过程,下同)。
(5)按照说明书服用补铁片,成人每天补充铁元素质量(保留整数)。

(1)硫酸亚铁的相对分子质量(列式计算)。
(2)硫酸亚铁中铁、硫、氧三种元素质量比 (列式计算,化成最简整数比)。
(3)硫酸亚铁中铁元素质量分数列式计算,保留0.1%)。
(4)该补铁片中铁元素的质量分数(保留0.1%)(写出计算过程,下同)。
(5)按照说明书服用补铁片,成人每天补充铁元素质量(保留整数)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】尿素[CO(NH2)2]是农村常用的化肥,请按要求进行计算。
(1)尿素的相对分子质量为__________。
(2)尿素中碳、氮元素的质量比为__________。
(3)尿素中氮元素的质量分数为__________。(计算结果保留至 )
)
(4)现有尿素和硝酸铵的混合物,已知其中氮元素的质量分数为 。则混合物中尿素与硝酸铵的质量比为__________,混合物中氢元素的质量分数为_________。
。则混合物中尿素与硝酸铵的质量比为__________,混合物中氢元素的质量分数为_________。
(1)尿素的相对分子质量为__________。
(2)尿素中碳、氮元素的质量比为__________。
(3)尿素中氮元素的质量分数为__________。(计算结果保留至
 )
)(4)现有尿素和硝酸铵的混合物,已知其中氮元素的质量分数为
 。则混合物中尿素与硝酸铵的质量比为__________,混合物中氢元素的质量分数为_________。
。则混合物中尿素与硝酸铵的质量比为__________,混合物中氢元素的质量分数为_________。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】某化学兴趣小组通过二氧化碳的质量,计算石灰石中碳酸钙的含量,将30g石灰石样品放入大烧杯,称得大烧杯和石灰石样品的总质量为100g,再把300g稀盐酸平分五份,依次加入大烧杯,每次反应后,记录数据如下
(1)其中a的值是___________ 。
(2)计算石灰石样品中碳酸钙的质量分数(有计算过程)
(3)计算稀盐酸的溶质的质量分数
(4)画出在30g样品中加入稀盐酸的质量与生成气体的质量变化关系示意图
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 入稀盐酸的质量 | 60 | 60 | 60 | 60 | 60 |
| 大烧杯所盛物质的的总质量 | 155.6 | 211.2 | 269 | 329 | a |
(2)计算石灰石样品中碳酸钙的质量分数(有计算过程)
(3)计算稀盐酸的溶质的质量分数
(4)画出在30g样品中加入稀盐酸的质量与生成气体的质量变化关系示意图
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】实验小组购得用于食用菌种植的轻质碳酸钙,标签如图1.为测定碳酸钙的质量分数,小组进行了如下实验:
①称取一定量样品放入一烧杯中;
②再往上述烧杯中加入50g的盐酸充分反应;
③绘制放出气体与烧杯中物质质量的关系图(图2),(温馨提示:图中58g为反应开始时烧杯中物质的质量.)

请计算,并回答下列有关问题:
(1)反应过程中产生的气体质量是______ g。
(2)若反应中消耗的盐酸质量为50g,则样品中碳酸钙的质量分数是多少?(写出计算过程,结果保留小数点后2位)
(3)请你画出消耗固体样品质量与生成气体质量变化关系图。
(4)如果上述轻质碳酸钙样品中所含杂质不含钙元素,请你通过计算回答标签标示的含钙量______ (填正确或不正确)。
①称取一定量样品放入一烧杯中;
②再往上述烧杯中加入50g的盐酸充分反应;
③绘制放出气体与烧杯中物质质量的关系图(图2),(温馨提示:图中58g为反应开始时烧杯中物质的质量.)

请计算,并回答下列有关问题:
(1)反应过程中产生的气体质量是
(2)若反应中消耗的盐酸质量为50g,则样品中碳酸钙的质量分数是多少?(写出计算过程,结果保留小数点后2位)
(3)请你画出消耗固体样品质量与生成气体质量变化关系图。
(4)如果上述轻质碳酸钙样品中所含杂质不含钙元素,请你通过计算回答标签标示的含钙量
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】下图为某钙片的商品标签,为测定钙片中钙元素的质量分数(假设钙片中的辅助原料不含钙元素,也不参与反应),某化学兴趣小组取10片钙片研碎,放入烧杯中,进行如下实验。

(1)过程中化学反应化学方程式为_______ ,产生的CO2质量为_______ 。
(2)计算此钙片中含碳酸钙的质量分数_______ 。(最后结果精确至0.1%)。
| XXX钙咀嚼片 【主要原料】碳酸钙、辅助原料等 【适宜人群】需要补充钙的中老年人 【食用方法】每日2次,每次1片,嚼食 【产品规格】1.2g/片 |

(1)过程中化学反应化学方程式为
(2)计算此钙片中含碳酸钙的质量分数
您最近一年使用:0次

 ]
]

