[提出问题]这包已完全变质的干燥剂成分是什么?
[猜想]猜想I:Ca(OH)2 猜想II:Ca(OH)2和CaCO3 猜想III:CaCO3
[实验探究]
(1)取少量样品于试管中,向其中滴加少量稀盐酸,无气泡产生.于是小莉认为没有CaCO3,小晶却不同意小莉的结论,理由是
(2)为进一步确定其成分,小组同学共同设计了如表方案,请你完成实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加适量水溶解,向试管中滴加几滴酚酞溶液。 | 猜想II成立 | |
| ②另取少量样品于试管中,加适量水溶 解,加入 |
[实验反思](1)步骤②中有关反应的化学方程式为
(2)生石灰变质过程可简述为:生石灰吸收
相似题推荐
【猜想与假设】
猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:
【实验与探究】
(1)设计如下实验:
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸。 | 若实验过程中始终没有气泡产生。 | 则证明猜想 |
| 步骤二:取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氢氧化钙溶液。 | 若实验过程中产生 | 则证明猜想Ⅱ或Ⅲ成立,此过程中发生反应的化学方程式为 |
(2)为了进一步验证猜想结果,小明同学提出了如下实验方案:在完成步骤二的实验后,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立。小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道:氯化钙溶液呈中性。因此氯化钙溶液不能使无色酚酞试液变红,但碳酸钠溶液呈
(3)实验小组的同学展开讨论,又提出了一个定量实验方案,通过测定产生沉淀的质量来证明猜想Ⅱ或Ⅲ成立。实验如下:准确称量m克固体样品于试管中,加入蒸馏水完全溶解,然后滴加足量氯化钙溶液,充分反应后过滤、洗涤、干燥称得沉淀的质量为n克,若猜想Ⅱ成立,则m与n的关系式为(用含m和n的等式或不等式表示,下同)
【推荐2】兴趣小组想探究家中厨房用某种洗涤剂粉末的成分,在老师指导下,进行了大胆的猜想与实验:
【提出问题】洗涤剂粉末中主要含有哪些物质?
【作出猜想】根据所学酸碱盐知识做出以下猜想。
猜想一:可能含有 ;
;
猜想二:可能含有
猜想三:可能含有 和
和 。
。
【实验探究】
Ⅰ.取少量粉末,加水溶解得到无色溶液,小组同学测得溶液液的 大于7,证明洗涤剂的溶液显碱性,用
大于7,证明洗涤剂的溶液显碱性,用 试纸测定溶液
试纸测定溶液 的方法:
的方法:
Ⅱ.取洗涤剂粉末,滴加少量的稀盐酸,未观察到有气泡产生。证明猜想一正确,小组同学对此结论产生了疑问,原因是
Ⅲ.探究该洗涤剂中是否含有 、
、 .
.
取少量粉末,加水配成溶液,加入稍过量 溶液,观察到
溶液,观察到 .静置,取上层清液于试管中,再滴几滴
.静置,取上层清液于试管中,再滴几滴 。
。
【分析讨论】
(1)实验Ⅲ中发生反应的化学方程式为
(2)实验Ⅲ中加入稍过量的 溶液的目的是
溶液的目的是
【实验结论】该洗涤剂中含有 和
和 。
。
小刚认为氢氧化钙可能变质所依据的化学原理是(用化学方程式表示):
[猜想]①该固体未变质;②该固体部分变质;③该固体完全变质。
[设计实验]
操作步骤 | 现象 | 结论 |
(1) | 证明该固体已经发生变质 | |
(2)另取少量瓶中的白色粉末加入水中后,再取少许上层清液加入无色酚酞试液 | 证明该固体未完全变质 |
[结论]通过现象分析,小刚确定猜想②成立。
[反思]我对该固体有一个想继续探究的问题:
【学习交流】碱石灰不能干燥二氧化碳气体的原因分析
原因一:氢氧化钠与二氧化碳反应生成碳酸钠;
原因二:
实验室有一瓶因敞口久置后变质的碱石灰,某化学兴趣小组对其成分展开讨论与探究:
【提出猜想】变质的碱石灰除含水以外,可能还含有哪些成分?
猜想一:NaOH Ca(OH)2
猜想二:NaOH Ca(OH)2 CaCO3
猜想三:NaOH CaCO3
猜想四:Na2CO3 Ca(OH)2
猜想五:Na2CO3 CaCO3
【提出质疑】
兴趣小组部分同学认为猜想
【查阅资料】兴趣小组为了更好地进行实验探究,将常见盐的水溶液的酸碱性整理如下:
| 氯化钠 | 硝酸钠 | 碳酸钠 | 氯化钙 | 硝酸钙 | 氯化钡 | 硝酸钡 | 硫酸铜 |
| 中性 | 中性 | 碱性 | 中性 | 中性 | 中性 | 中性 | 酸性 |
取少量碱石灰样品于试管中,加入足量蒸馏水。
(1)若发现样品完全溶解,则证明猜想
(2)若发现样品未完全溶解,过滤后得到滤渣M和溶液N,进行相关实验。
实验一:向溶液N中先滴加几滴酚酞溶液,可观察到溶液
实验二:向滤渣M中加入适量盐酸,可看到有气泡产生,反应方程式为
【拓展延伸】干燥剂的选择要视被干燥气体的性质而定,碱性干燥剂不能干燥酸性气体,同理,酸性干燥剂不能干燥碱性气体。总之,干燥剂不能与被干燥气体发生化学反应。

(1)同学们看到干燥剂袋上的文字马上明白了干燥原理。其原理是
(2)小明同学用一支试管进行实验就证明了这包干燥剂仍然有效,其实验方法是
(3)成分研究:这包干燥剂是否含碳酸钙?小亮和小芳分别进行如下实验探究:
| 实验操作 | 实验现象 | 实验结论 | |
| 小亮 | 取少量干燥剂于试管中加水溶解、过滤 | 滤纸上留有白色固体 | 含有碳酸钙 |
| 小芳 | 取少量干燥剂于试管中滴加盐酸 | 无气泡产生 | 不含有碳酸钙 |
 某同学对一瓶久置的“碱石灰”作了如下探究:(已知:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH)
某同学对一瓶久置的“碱石灰”作了如下探究:(已知:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH)(1)猜想:
猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3.
则CaO与水反应的反应方程式为
(2)实验:如图所示:
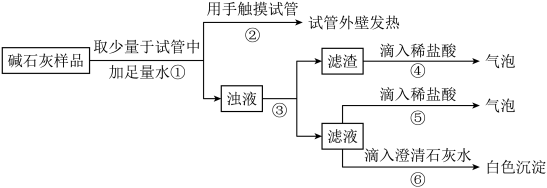
(3)判断:
a若Ca(OH)₂、CaCO3和Na2CO3投入到水中不会放热,则由操作②现象判断:猜想Ⅱ
b NaOH暴露在空气中变质的化学方程式为
c综合a和b的结论,判断该样品变质情况为
(4)拓展:由上述实验说明,实验室中“碱石灰”应
【提出问题】刺激性气味的气体是什么?
【猜想与假设】猜想1:可能是SO2猜想2:可能是HCl猜想3:可能是NH3
大家讨论后认为猜想3不合理,依据是
【查阅资料】
(1)二氧化硫和氯化氢溶于水后溶液均呈酸性;
(2)SO2和CO2的化学性质相似,都能使澄清石灰水变浑浊,且原理相同。写出二氧化硫和氢氧化钙反应的化学方程式
【实验探究】
小诚将产生的气体通入紫色石蕊溶液中,观察到
【评价与改进】小煜认为小诚的结论不科学,原因
| 实验操作 | 实验现象 |
| 将产生的气体 | 无明显现象。 |
【拓展应用】实验室可用氯化钠和硫酸反应制取氯化氢气体,已知氯化氢气体极易溶于水。
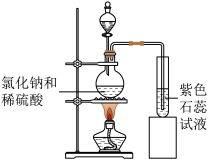
请推测实验室制取氯化氢气体最适宜的方法为
A.加热氯化氢溶液和稀硫酸的混合物
B.加热氯化钠固体和稀硫酸的混合物
C.加热氯化钠固体和浓硫酸的混合物
【建立猜想】①氢氧化钡过量 ②盐酸过量 ③
【进行实验】取少量反应后的溶液于试管中,滴入几滴无色酚酞溶液,溶液不变色。
【得出结论】猜想①错误。
【继续实验】小敏为了验证剩余猜想,设计了如下实验方案:
实验方案I:重新取样,滴加少量AgNO3溶液,若产生白色沉淀,证明猜想②正确。有同学认为方案Ⅰ的结论不合理,其原因是
实验方案Ⅱ:重新取样,逐滴滴加足量Na2CO3溶液,若出现
小敏同学通过实验方案Ⅱ得出了正确结论。
【表达交流】为确定猜想②是否正确,还可以选择的试剂有
A.紫色石蕊溶液 B.铜片 C.铁锈

【提出问题】滤液Y中的溶质成分是什么?
【做出猜想】猜想一:溶质是NaOH;
猜想二;溶质是
猜想三:溶质是NaOH和Na2CO3。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量滤液Y于试管中,滴加 | 无明显现象 | 猜想二不成立 |
| ②另取少量滤液Y于试管中,加入适量BaCl2溶液 | 猜想三成立 |
小林同学:滤渣X为CaCO3;
小华同学:滤渣为XCaCO3和Ca(OH)2。
你认为
【反思交流】通过本次实验,同学们认为,反应后物质的成分,既要考虑反应的生成物,还要考虑
【实验一】自制酸碱指示剂
(1)取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色。分别装好待用。
(2)取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图。

记录如下:
| NaOH溶液 | 稀盐酸 | |
| 紫包菜汁液 | ①绿色 | ②红色 |
| 白菜汁液 | ③无色 | ④淡黄色 |
你认为两种汁液中,更适合做酸碱指示剂的是
(3)再用苹果汁进行相同实验,紫包菜汁液变红色,白菜汁液变淡黄色。则苹果汁溶液显
【实验二】探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为
【实验三】废液再探究
【实验二】结束后,两组同学将全部的废液集中倒进一个废液缸中。兴趣小组同学对废液进行过滤,得到无色滤液。
【提出问题】
滤液中含有什么溶质?
【做出猜想】
滤液中一定含有
【实验探究】
(1)取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色。
(2)继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有
(3)为最终确定该滤液的组成,还需补充的实验是:
【实验结论】 该无色滤液的组成为
【提出问题】这瓶NaOH溶液一定变质了,其变质的程度如何呢?
【猜想与假设】小红的猜想:NaOH溶液部分变质。
你的不同猜想:NaOH溶液
【收集资料】小红知道,NaOH敞口放置会变质的原因是NaOH与空气中的CO2反应。
【实验探究】小红设计如下实验验证自己的猜想,请根据表中内容填写小红实验时的现象。
| 实验步骤 | 现象 | 结论 |
| 第一步:取少量NaOH溶液于试管中,滴加足量的CaCl2溶液 | ①有白色沉淀产生。 | 该NaOH溶液部分变质。 |
| 第二步:向上述试管中再滴加酚酞溶液 | ② |
假设你的猜想正确,并按小红的实验方案进行实验,则你观察到的“第一步”实验现象有白色沉淀产生,“第二步”实验现象是
【实验反思】保存NaOH溶液的方法是
[提出问题]蚁酸的成分是什么?它有什么性质?
[查阅资料]I.蚁酸的化学名称叫甲酸,化学式为HCOOH
II.蚁酸隔绝空气并加热时会分解生成两种氧化物
[实验探究](1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成
(2)小芳同学根据蚁酸中含有
(3)对它分解生成的另一种氧化物,小敏提出两种猜想:
猜想Ⅰ是CO2;
猜想Ⅱ是
他们按如图所示进行实验:先向装置中通入一会N2,再将蚁酸分解产生的气体通入其中.
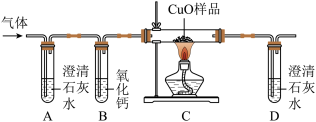
①先通N2的目的是
②若实验过程中看到
③装置B的作用是
④装置C中的现象为
[结论]甲酸受热能分解,反应的化学方程式是
[讨论交流]从环保角度看,该装置存在的明显缺陷是
[拓展延伸]小组同学利用蚁酸分解产生的气体,测定10g氧化铜样品(杂质不参与反应)中氧化铜的质量分数,在不同时刻测定C中固体的质量(如表):
| 反应时间/min | 2 | 4 | 6 | 8 | 10 |
| 固体质量/g | 9.3 | 8.8 | 8.5 | 8.4 | 8.4 |



