人类社会的发展离不开金属,试回答相关问题:
1.“沙里淘金”说明金在自然界中有___________ 形式存在(填“单质”或“化合物”)。
2.金属矿物的储量有限,而且不能再生.保护金属资源的有效途径除防止金属的腐蚀外,还有(写出一条即可)__________ 等。
3.铁在空气中腐蚀,实际上是铁跟___________ 等物质作用,发生一系列复杂的化学反应,转化为铁的化合物的过程;如图所示的某取暖片中发热剂主要成分有铁粉、活性炭、氯化钠、水等,使用过程中是_______ 能转化为热能。

4.铁、铜、铝三种元素在地壳中的含量由多到少顺序为Al>Fe>Cu,三种金属中被人类发现和利用的时间最早的是金属___________ ;铝具有很好的抗腐蚀性能,原因是__________________ 。
5.小王同学想测定某Cu-Zn合金中铜的质量分数,取合金粉末13g,向其中逐滴加入一定浓度的稀硫酸,所加稀硫酸与生成氢气的质量关系如有下图所示。请完成下列分析及计算:

①反应生成氢气的质量为_______ g;
②计算合金中铜的质量分数(写出计算过程)。_______
1.“沙里淘金”说明金在自然界中有
2.金属矿物的储量有限,而且不能再生.保护金属资源的有效途径除防止金属的腐蚀外,还有(写出一条即可)
3.铁在空气中腐蚀,实际上是铁跟

4.铁、铜、铝三种元素在地壳中的含量由多到少顺序为Al>Fe>Cu,三种金属中被人类发现和利用的时间最早的是金属
5.小王同学想测定某Cu-Zn合金中铜的质量分数,取合金粉末13g,向其中逐滴加入一定浓度的稀硫酸,所加稀硫酸与生成氢气的质量关系如有下图所示。请完成下列分析及计算:

①反应生成氢气的质量为
②计算合金中铜的质量分数(写出计算过程)。
更新时间:2017-02-28 15:02:40
|
相似题推荐
综合应用题
|
适中
(0.65)
名校
【推荐1】“化学氧呼吸自救器”是人在缺氧环境或出现高浓度有毒有害气体环境中使用的一种安全防护装置,内部装有颗粒状超氧化钾(KO2)作为“制氧剂”,其反应原理为: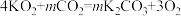 。
。_____________
(2)若要制得96g氧气,则理论上需要含KO2 80%的制氧剂的质量是多少?(请写出计算过程)
(3)小明设计“化学氧呼吸自救器”时,为确定制氧剂的用量,除了查阅人体每分钟呼吸次数外,还需了解与人体呼吸相关的数据是 (填序号)。
(4)吸氧时,供氧装置要与如图装置配套使用,使用时罐中要加入一定量的水,氧气需通过水再被人体吸入,所以吸氧时病人的吸氧管要接在__________ (选填“a”或“b”)端,吸氧时该装置的作用是_________ 。
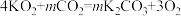 。
。
(2)若要制得96g氧气,则理论上需要含KO2 80%的制氧剂的质量是多少?(请写出计算过程)
(3)小明设计“化学氧呼吸自救器”时,为确定制氧剂的用量,除了查阅人体每分钟呼吸次数外,还需了解与人体呼吸相关的数据是 (填序号)。
| A.每次呼出二氧化碳的量 | B.每次呼吸耗氧量 | C.每次呼出氮气的量 |
(4)吸氧时,供氧装置要与如图装置配套使用,使用时罐中要加入一定量的水,氧气需通过水再被人体吸入,所以吸氧时病人的吸氧管要接在
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组的同学在探究碱溶液的化学性质时,进行了如图所示的实验。

(1)实验A中,推入NaOH溶液后,可观察到的现象是______________ 。
(2)实验B中发生反应的化学方程式为_____________ 。实验结束后,小组的同学对B试管中上层清液的溶质成分产生疑问,作出如下猜想:
猜想一:只含有NaOH;
猜想二:含有NaOH、Na2CO3
猜想三:含有NaOH、Ca(OH)2。
同学们取少量B试管中的上层清液分别置于甲、乙两支试管中,进行探究:
(3)A、B、C、 D四个实验中,能体现碱化学通性的是 ________ (填字母)。小组的同学经过讨论认为四个实验并没有探究出碱所有的化学通性。从这四个实验中选择一个,继续加入相关试剂,能得出碱的其他化学通性。该实验的方案是_________ (写出操作和现象)。
(4)实验C中盛有一定质量5%的氢氧化钠溶液,当加入66.9g硫酸铜溶液,恰好完全反应,得到4.9g蓝色沉淀。试计算:
①所用氢氧化钠溶液的质量__________ 。
②反应后所得溶液的溶质质量分数________ 。解题过程: (计算结果保留一位小数)

(1)实验A中,推入NaOH溶液后,可观察到的现象是
(2)实验B中发生反应的化学方程式为
猜想一:只含有NaOH;
猜想二:含有NaOH、Na2CO3
猜想三:含有NaOH、Ca(OH)2。
同学们取少量B试管中的上层清液分别置于甲、乙两支试管中,进行探究:
| 实验操作 | 实验现象 | 结论 |
| 在试管甲中滴加碳酸钠溶液 | 不产生白色沉淀 | 猜想三错误 |
| 在试管乙中滴加足量稀盐酸 | 猜想二正确 |
(4)实验C中盛有一定质量5%的氢氧化钠溶液,当加入66.9g硫酸铜溶液,恰好完全反应,得到4.9g蓝色沉淀。试计算:
①所用氢氧化钠溶液的质量
②反应后所得溶液的溶质质量分数
您最近一年使用:0次
【推荐3】农业生产的可持续发展是国家重点战略之一.某校化学小组决定围绕秸秆综合利用开展一次主题实践活动.
【查阅资料】目前世界主流的秸秆综合利用方式有:
①粉碎、压缩膨化后作饲料;②粉碎直接还田作肥料;③粉碎、压缩成颗粒后焚烧发电、灰烬作钾肥.
【定性研究】
(1)秸秆粉碎后再燃烧的目的是______ .
(2)小组同学还围绕草木灰(主要成分为碳酸钾和不溶性杂质,其他成分不影响实验,忽略不计),进行如下实验:
①取浸出液少许、测得其pH约为11,溶液是______ (填“酸性”或“碱性”).
②为验证 存在,小组同学另取草木灰浸出液适量,低温浓缩后,部分同学向其中入足量的盐酸,你观察到的现象是
存在,小组同学另取草木灰浸出液适量,低温浓缩后,部分同学向其中入足量的盐酸,你观察到的现象是______ .
③另一部分同学观察到的现象是有白色沉淀生成,他们向浸出液中滴加的试剂可能是______ (填字母序号,名选).
A. 溶液 B.稀硫酸 C.
溶液 B.稀硫酸 C. 溶液 D.
溶液 D. 溶液
溶液
【定量研究】草木灰可作优质钾肥,为进一步分析草木灰中钾元素质量分数,实验小组同学称取草木灰100g,加水充分溶解,经过滤、稀释,制得草木灰浸出液100g,进行定量研究.
(3)小组同学设计了如图装置进行探究(部分夹持装置省略,药品均足量).

①装置E的作用是______ .
②反应结束后,打开弹簧夹,向装置中缓慢通入一会儿氮气,目的是______ .
【数据处理】
(4)打开A装置中分液漏斗活塞,向烧瓶中缓慢滴加溶质质量分数为7.3%的稀盐酸,至溶液中不再产生气泡时,恰好用去稀盐酸100g,同时测得D装置溶液增重4.84g.
①小明同学根据所用盐酸质量计算出草木灰中钾元素的质量分数为______ .
②小亮同学认为也可根据溶液增重来计算草木灰中钾元素质量分数,你同意他的观点吗?请说明理由______ .
【实践拓展】
(5)草木灰做肥料______ (填“适宜”或“不适宜”)与铵态氮肥混合施用.
【查阅资料】目前世界主流的秸秆综合利用方式有:
①粉碎、压缩膨化后作饲料;②粉碎直接还田作肥料;③粉碎、压缩成颗粒后焚烧发电、灰烬作钾肥.
【定性研究】
(1)秸秆粉碎后再燃烧的目的是
(2)小组同学还围绕草木灰(主要成分为碳酸钾和不溶性杂质,其他成分不影响实验,忽略不计),进行如下实验:
①取浸出液少许、测得其pH约为11,溶液是
②为验证
 存在,小组同学另取草木灰浸出液适量,低温浓缩后,部分同学向其中入足量的盐酸,你观察到的现象是
存在,小组同学另取草木灰浸出液适量,低温浓缩后,部分同学向其中入足量的盐酸,你观察到的现象是③另一部分同学观察到的现象是有白色沉淀生成,他们向浸出液中滴加的试剂可能是
A.
 溶液 B.稀硫酸 C.
溶液 B.稀硫酸 C. 溶液 D.
溶液 D. 溶液
溶液【定量研究】草木灰可作优质钾肥,为进一步分析草木灰中钾元素质量分数,实验小组同学称取草木灰100g,加水充分溶解,经过滤、稀释,制得草木灰浸出液100g,进行定量研究.
(3)小组同学设计了如图装置进行探究(部分夹持装置省略,药品均足量).

①装置E的作用是
②反应结束后,打开弹簧夹,向装置中缓慢通入一会儿氮气,目的是
【数据处理】
(4)打开A装置中分液漏斗活塞,向烧瓶中缓慢滴加溶质质量分数为7.3%的稀盐酸,至溶液中不再产生气泡时,恰好用去稀盐酸100g,同时测得D装置溶液增重4.84g.
①小明同学根据所用盐酸质量计算出草木灰中钾元素的质量分数为
②小亮同学认为也可根据溶液增重来计算草木灰中钾元素质量分数,你同意他的观点吗?请说明理由
【实践拓展】
(5)草木灰做肥料
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】I.用符号要求的物质的字母填空.
A.石墨 B.小苏打 C.食盐 D.天然气
(1)常用做调味品的是__ ;(2)常用作电池电极的是__ ;
(3)常用于家庭燃料的是__ ;(4)常用于焙制糕点的是__ .
II.判断下列大小或强弱关系,并用“<”、“>”或“=”填空.
(1)金属活动性:锌__ 铜;(2)受热稳定性:碳酸钙__ 碳酸氢铵;
(3)相同条件下的密度:空气__ 二氧化碳;
(4)相同条件下的挥发性:稀盐酸__ 浓盐酸.
A.石墨 B.小苏打 C.食盐 D.天然气
(1)常用做调味品的是
(3)常用于家庭燃料的是
II.判断下列大小或强弱关系,并用“<”、“>”或“=”填空.
(1)金属活动性:锌
(3)相同条件下的密度:空气
(4)相同条件下的挥发性:稀盐酸
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】金属及金属材料广泛应用于生产、生活及科学实验,其应用推动了社会的发展。
(1)用金属铜制作铜火锅,主要是利用了铜具有良好的延展性和______________ 性。
(2)《天工开物》中记录了黄铜(铜锌合金)的冶炼工业:“赤铜(Cu2O),以炉甘石或倭铅参和,转色为黄铜…”,利用此法炼制得到的黄铜的硬度比纯铜______________ (选填“大”或“小”)。
(3)为了防止铁制品生锈,通常会在铁制品表面刷漆,其原理是______________ 。工人师傅常用稀盐酸去除铁锈,有关反应的化学方程式为______________ 。
(4)从X、银、铜、锌四种金属的混合物中分离某贵重金属。流程如下:

①滤液A中含有______________ 种溶质。
②金属X、银、铜、锌的金属活动性由强到弱的顺序是______________ 。
(1)用金属铜制作铜火锅,主要是利用了铜具有良好的延展性和
(2)《天工开物》中记录了黄铜(铜锌合金)的冶炼工业:“赤铜(Cu2O),以炉甘石或倭铅参和,转色为黄铜…”,利用此法炼制得到的黄铜的硬度比纯铜
(3)为了防止铁制品生锈,通常会在铁制品表面刷漆,其原理是
(4)从X、银、铜、锌四种金属的混合物中分离某贵重金属。流程如下:

①滤液A中含有
②金属X、银、铜、锌的金属活动性由强到弱的顺序是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】认识O2的性质
某同学做氧气的性质实验,如图为木炭在氧气中燃烧的实验示意图。

实验步骤:
①用排水法收集好一瓶氧气
②……
③用坩埚钳夹取一小块木炭,在酒精灯上加热到发红,伸入盛满氧气的集气瓶中,燃烧停止后,取出坩埚钳。
④向集气瓶中加入少量澄清石灰水,振荡。
根据实验操作,通过分析,回答下列问题:
(1)步骤②具体操作为______ 。
(2)步骤③操作中,最好是将烧红的木炭从瓶口由上至下缓慢伸入到盛满氧气的集气瓶中,这一实验操作的主要目的是______ 。
(3)步骤④操作中,可观察到澄清石灰水变浑浊,其发生反应的化学方程式为______ 。
认识金属的性质
(4)下列物质中不属于 合金的是______(填字母标号)。
(5)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,这为发现金属活动性顺序奠定了基础。小嘉选用锡、铜、锌三种金属放入稀盐酸中,会“消失”的金属有______ 。
(6)向硝酸铜和硝酸银的混合溶液中逐渐加入铁粉,溶液质量变化如图所示,则B点时溶液中所含的金属阳离子为______ 。

认识酸、碱、盐的性质
(7)生活中常见的几种物质和Na2CO3的关系如图所示,“—”表示物质之间可以反应,“→”表示物质之间可以转化(部分反应物、生成物及反应条件已略去)。丁物质常用作食品干燥剂,请写出图中序号①所对应反应的化学方程式:______ 。

若不慎将乙物质的浓溶液沾到皮肤上,应先用大量的水冲洗,再涂上______ (填名称)溶液。上述反应及转化关系中共涉及______ 种基本反应类型。
某同学做氧气的性质实验,如图为木炭在氧气中燃烧的实验示意图。

实验步骤:
①用排水法收集好一瓶氧气
②……
③用坩埚钳夹取一小块木炭,在酒精灯上加热到发红,伸入盛满氧气的集气瓶中,燃烧停止后,取出坩埚钳。
④向集气瓶中加入少量澄清石灰水,振荡。
根据实验操作,通过分析,回答下列问题:
(1)步骤②具体操作为
(2)步骤③操作中,最好是将烧红的木炭从瓶口由上至下缓慢伸入到盛满氧气的集气瓶中,这一实验操作的主要目的是
(3)步骤④操作中,可观察到澄清石灰水变浑浊,其发生反应的化学方程式为
认识金属的性质
(4)下列物质中
| A.钢 | B.青铜 | C.焊锡 | D.水银 | E.赤铁矿 |
(5)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,这为发现金属活动性顺序奠定了基础。小嘉选用锡、铜、锌三种金属放入稀盐酸中,会“消失”的金属有
(6)向硝酸铜和硝酸银的混合溶液中逐渐加入铁粉,溶液质量变化如图所示,则B点时溶液中所含的金属阳离子为

认识酸、碱、盐的性质
(7)生活中常见的几种物质和Na2CO3的关系如图所示,“—”表示物质之间可以反应,“→”表示物质之间可以转化(部分反应物、生成物及反应条件已略去)。丁物质常用作食品干燥剂,请写出图中序号①所对应反应的化学方程式:

若不慎将乙物质的浓溶液沾到皮肤上,应先用大量的水冲洗,再涂上
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】人类历史发展的不同阶段曾以不同金属材料的使用作为标志。

(1)金、银在自然界有单质形式存在,说明他们的化学性质都_________ (填“不活泼”或“活泼”)。
(2)工业上常以赤铁矿石(主要成分是氧化铁)为原料炼铁,请写出一氧化碳与氧化铁反应的化学方程式:______________ 。
(3)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其_______________ (填字母序号)非常好。
A可塑性 B机械性能 C抗腐蚀性能
(4)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有________________ (填字母序号)。
A金属原料的成本 B生成过程中的能耗和污染 C金属的回收利用
(5)黄铜是铜和锌的合金。某化学兴趣小组的同学为了测定某黄铜样品中铜的质量分数,取20g该黄铜样品粉末放入烧杯中,向其中加入100g稀硫酸,恰好完全反应。反应后烧杯中剩余物的总质量为119.8g。试求:
①反应产生氢气的质量是___________ g。
②该黄铜样品中铜的质量分数。(写出计算过程)____

(1)金、银在自然界有单质形式存在,说明他们的化学性质都
(2)工业上常以赤铁矿石(主要成分是氧化铁)为原料炼铁,请写出一氧化碳与氧化铁反应的化学方程式:
(3)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其
A可塑性 B机械性能 C抗腐蚀性能
(4)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有
A金属原料的成本 B生成过程中的能耗和污染 C金属的回收利用
(5)黄铜是铜和锌的合金。某化学兴趣小组的同学为了测定某黄铜样品中铜的质量分数,取20g该黄铜样品粉末放入烧杯中,向其中加入100g稀硫酸,恰好完全反应。反应后烧杯中剩余物的总质量为119.8g。试求:
①反应产生氢气的质量是
②该黄铜样品中铜的质量分数。(写出计算过程)
您最近一年使用:0次
【推荐2】金属材料在人类文明的发展中起着重要作用,古代冶金技术彰显了我国劳动人民的智慧。
(1)战国《韩非子·内储说上》提到,早期采金技术均是“沙里淘金”。金在自然界中主要以______ (填“单质”或“化合物”)形式存在。
(2)明代宋应星所著的《天工开物》一书,介绍了“火法炼锌”的方法:把炉甘石( )和煤炭饼装入炼锌罐(加下图所示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。
)和煤炭饼装入炼锌罐(加下图所示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。
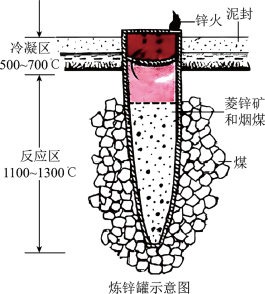
①炉甘石( )加入锌罐之前,先将其粉碎的目的是
)加入锌罐之前,先将其粉碎的目的是______ 。
②反应区中,炉甘石( )在高温下分解生成一种金属氧化物和一种常见的温室气体,写出相应的化学方程式
)在高温下分解生成一种金属氧化物和一种常见的温室气体,写出相应的化学方程式______ 。
③反应区中,煤炭中的碳与氧化锌发生反应: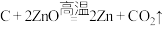 ,该反应中体现了碳的(填“还原性”或“氧化性”)
,该反应中体现了碳的(填“还原性”或“氧化性”)______ ;
④必须“冷定”后才能“毁罐”取锌,请从化学变化的角度解释其原因______ 。
(3)北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”的方法:“熬胆矾铁金,久之亦化为铜”。即在硫酸铜溶液中加入铁,则可得到铜。该反应的化学方程式是______ ,该反应中,化合价发生改变的元素是______ (填元素符号)。
(1)战国《韩非子·内储说上》提到,早期采金技术均是“沙里淘金”。金在自然界中主要以
(2)明代宋应星所著的《天工开物》一书,介绍了“火法炼锌”的方法:把炉甘石(
 )和煤炭饼装入炼锌罐(加下图所示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。
)和煤炭饼装入炼锌罐(加下图所示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。
①炉甘石(
 )加入锌罐之前,先将其粉碎的目的是
)加入锌罐之前,先将其粉碎的目的是②反应区中,炉甘石(
 )在高温下分解生成一种金属氧化物和一种常见的温室气体,写出相应的化学方程式
)在高温下分解生成一种金属氧化物和一种常见的温室气体,写出相应的化学方程式③反应区中,煤炭中的碳与氧化锌发生反应:
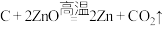 ,该反应中体现了碳的(填“还原性”或“氧化性”)
,该反应中体现了碳的(填“还原性”或“氧化性”)④必须“冷定”后才能“毁罐”取锌,请从化学变化的角度解释其原因
(3)北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”的方法:“熬胆矾铁金,久之亦化为铜”。即在硫酸铜溶液中加入铁,则可得到铜。该反应的化学方程式是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐3】中国古代已掌握了一定的金属冶炼技术,现在的技术依然在不断革新。
Ⅰ、古文记载的冶炼技术
(1)战国《韩非子·内储说上》提到,早期采金技术均是“沙里淘金”。黄金能以单质形式存在于自然界的原因是______ 。
(2)东汉《周易参同契》记载:“胡粉[主要含PbCO3⋅Pb(OH)2],投火中,色坏还为铅(Pb)”。该反应过程主要原理之一: 。下列分析正确的是______。
。下列分析正确的是______。
(3)明代《天工开物》记载:“火法炼锌”过程为“炉甘石(主要含 )装载入泥罐内……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,冷定毁罐取出,取出即倭铅也”。
)装载入泥罐内……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,冷定毁罐取出,取出即倭铅也”。
①文中“倭铅”的主要成分是______ (填标号)。
A.Pb B.Zn C.Zn和Pb混合物
②“其底铺薪”指利用燃烧的“薪”将煤炭饼引燃,从燃烧条件分析燃烧“薪”的作用是______ 。
③火法炼锌时在鼓风炉中控制温度在 至
至 进行,使生成的锌汽化蒸馏出来,蒸馏过程属于
进行,使生成的锌汽化蒸馏出来,蒸馏过程属于______ 变化。
④“冷定”才能“毁罐取出”,从化学变化角度分析原因是______ 。
Ⅱ、现代金属冶炼
(4)①用赤铁矿石冶铁的反应原理是______ 。(用化学方程式表示)。
②某钢铁厂采用赤铁矿(主要成分为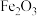 )炼铁,日产含铁
)炼铁,日产含铁 的生铁,至少需要含
的生铁,至少需要含 的赤铁矿的质量是多少?(写出计算过程)
的赤铁矿的质量是多少?(写出计算过程)______
(5)现代湿法冶铜的技术有很大发展,其中一种工艺流程简要概括如下图所示。

①废矿石中的 与稀硫酸溶液在某种细菌催化下与氧气作用生成硫酸铜溶液的化学方程式为
与稀硫酸溶液在某种细菌催化下与氧气作用生成硫酸铜溶液的化学方程式为______ 。
②流程中“系列操作”工艺的目的是______ 。
③上述流程中,可以回收再利用的物质是______ 。
Ⅰ、古文记载的冶炼技术
(1)战国《韩非子·内储说上》提到,早期采金技术均是“沙里淘金”。黄金能以单质形式存在于自然界的原因是
(2)东汉《周易参同契》记载:“胡粉[主要含PbCO3⋅Pb(OH)2],投火中,色坏还为铅(Pb)”。该反应过程主要原理之一:
 。下列分析正确的是______。
。下列分析正确的是______。| A.胡粉属于混合物 | B.冶炼过程中可能生成水 | C.上述反应属于分解反应 |
(3)明代《天工开物》记载:“火法炼锌”过程为“炉甘石(主要含
 )装载入泥罐内……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,冷定毁罐取出,取出即倭铅也”。
)装载入泥罐内……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,冷定毁罐取出,取出即倭铅也”。①文中“倭铅”的主要成分是
A.Pb B.Zn C.Zn和Pb混合物
②“其底铺薪”指利用燃烧的“薪”将煤炭饼引燃,从燃烧条件分析燃烧“薪”的作用是
③火法炼锌时在鼓风炉中控制温度在
 至
至 进行,使生成的锌汽化蒸馏出来,蒸馏过程属于
进行,使生成的锌汽化蒸馏出来,蒸馏过程属于④“冷定”才能“毁罐取出”,从化学变化角度分析原因是
Ⅱ、现代金属冶炼
(4)①用赤铁矿石冶铁的反应原理是
②某钢铁厂采用赤铁矿(主要成分为
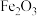 )炼铁,日产含铁
)炼铁,日产含铁 的生铁,至少需要含
的生铁,至少需要含 的赤铁矿的质量是多少?(写出计算过程)
的赤铁矿的质量是多少?(写出计算过程)(5)现代湿法冶铜的技术有很大发展,其中一种工艺流程简要概括如下图所示。

①废矿石中的
 与稀硫酸溶液在某种细菌催化下与氧气作用生成硫酸铜溶液的化学方程式为
与稀硫酸溶液在某种细菌催化下与氧气作用生成硫酸铜溶液的化学方程式为②流程中“系列操作”工艺的目的是
③上述流程中,可以回收再利用的物质是
您最近一年使用:0次



