糕点疏松剂的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究。
【探究实验一】碳酸氢钠溶液的酸碱性:用玻璃棒蘸取碳酸氢钠溶液滴在pH试纸上并与____ 对比,读出其pH约为10。由此得出的结论是:碳酸氢钠溶液呈碱性。
【探究实验二】碳酸氢钠能否与酸反应:取少量固体放入试管中,滴加足量的稀盐酸,现象为___ 。结论:碳酸氢钠能与盐酸反应。
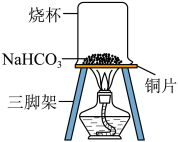
【探究实验三】碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示。
(1)加热一段时间后,观察到烧杯内壁有水珠。
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,
振荡,观察到澄清石灰水变浑浊。
(3)通过进一步实验来确定充分加热后的固体产物的成分。限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管。
(4)请分析上述操作①中不能用澄清石灰水替代氯化钙溶液的理由 _____ 。
(5)根据上述实验结论,写出碳酸氢钠受热分解的化学方程式:____ 。

【探究实验一】碳酸氢钠溶液的酸碱性:用玻璃棒蘸取碳酸氢钠溶液滴在pH试纸上并与
【探究实验二】碳酸氢钠能否与酸反应:取少量固体放入试管中,滴加足量的稀盐酸,现象为
【探究实验三】碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示。
(1)加热一段时间后,观察到烧杯内壁有水珠。
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,
振荡,观察到澄清石灰水变浑浊。
(3)通过进一步实验来确定充分加热后的固体产物的成分。限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管。
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量氯化钙溶液,振荡,静置 | 产生白色沉淀 | 产物含 |
| ② | 取操作①后的上层清液于试管B中,滴加 | 产物不含NaOH |
(5)根据上述实验结论,写出碳酸氢钠受热分解的化学方程式:
2017·广东·一模 查看更多[17]
2017届广东省九年级初中毕业生学业考试模拟化学试卷2广东省佛山市顺德区2018届九年级4月月考化学试题鲁教版九年级下册第八单元第三节 海水“制碱”考点12 盐和化肥2017年江苏省徐州市邳州市中考二模化学试题(已下线)【万唯原创】2017年河北省中考化学面对面卷练习册九年级专题突破专题八类型四(已下线)题型 实验探究题·课后特训1—4(已下线)题型 实验探究题·课后特训2—1(已下线)【万唯原创】2017年安徽省中考化学面对面卷九年级讲解册重点专题突破专题六类型四(已下线)【万唯原创】2017年陕西省中考化学面对面卷(科广版)九年级重难题型突破题型六(已下线)【万唯原创】2017年陕西省中考化学面对面卷(人教版)九年级重难题型突破题型六(已下线)【万唯原创】2017年陕西省中考化学试题研究卷练习册模块一专题七(已下线)【万唯原创】2017年陕西省中考化学面对面卷讲解册(鲁教版)九年级重难题型突破题型六(已下线)【万唯原创】2017年广东省中考化学试题研究卷九年级练习册第15讲人教版 初中化学 考点12 盐和化肥(已下线)7.3溶液的酸碱性基础拔高-2021-2022学年九年级化学鲁教版下册2023-2024九化课后作业与单元测试 鲁教版 第八单元 单元测试C卷
更新时间:2017-05-06 17:06:34
|
相似题推荐
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐1】CO2 的捕集与资源化利用是化学研究的热点。


(1)我国科学家李灿院士团队突破了太阳能电解水制取H2和CO2加氢制甲醇(CH3OH)的关键技术(液态太阳燃料技术),技术路线如图-1所示。
①该路线实现了能量间的相互转化,电解水的过程是由电能转化为______ (填“化学能”或“太阳能”)。
②氢能存储/CO2加氢反应(催化剂:ZnO-ZrO2、压强:5.0 Mpa、温度:315~ 320°C)的化学方程式为______ ,每生成1吨甲醇,理论上可减少排放______ 吨CO2。
③图-1中可循环使用的物质是CO2和______ 。
(2)捕集燃煤电厂烟气(含有CO2、N2、O2及H2O)中的CO2,并将其甲烷(CH4)化的流程如下。
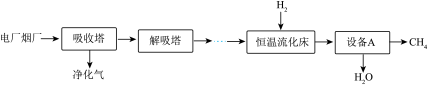
【资料卡片】
a、MEA水溶液低温可吸收CO2,升高温度可解吸CO2。
b、恒温流化床反应器出口温度高。
①“吸收塔”中电厂烟气从塔底通入,MEA水溶液从塔顶喷淋。这样操作的优点是______ ,“解吸塔”实现CO2解吸的操作是______ 。
②“设备A”可实现CH4和H2O气液分离,方法是______ 。
③根据资料卡片信息及流程,说出一种降低工艺成本的措施:______ 。
④CO2甲烷化的反应中, =
=____ 。
⑤不同制氢工艺碳排放量对比图如图-2所示,采用____ (填制氢方式)可以实现碳减排。


(1)我国科学家李灿院士团队突破了太阳能电解水制取H2和CO2加氢制甲醇(CH3OH)的关键技术(液态太阳燃料技术),技术路线如图-1所示。
①该路线实现了能量间的相互转化,电解水的过程是由电能转化为
②氢能存储/CO2加氢反应(催化剂:ZnO-ZrO2、压强:5.0 Mpa、温度:315~ 320°C)的化学方程式为
③图-1中可循环使用的物质是CO2和
(2)捕集燃煤电厂烟气(含有CO2、N2、O2及H2O)中的CO2,并将其甲烷(CH4)化的流程如下。

【资料卡片】
a、MEA水溶液低温可吸收CO2,升高温度可解吸CO2。
b、恒温流化床反应器出口温度高。
①“吸收塔”中电厂烟气从塔底通入,MEA水溶液从塔顶喷淋。这样操作的优点是
②“设备A”可实现CH4和H2O气液分离,方法是
③根据资料卡片信息及流程,说出一种降低工艺成本的措施:
④CO2甲烷化的反应中,
 =
=⑤不同制氢工艺碳排放量对比图如图-2所示,采用
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐2】能源“非石油化”是战略目标,发展以CH4、CO2等为原料的“C1化学”成为当今化工生产的必然趋势。通常天然气中含有H2S等有毒气体,下图为天然气合成氨的工艺流程。

(1)合成氨的原料之一为氮气,该流程中为合成氨提供氮气的物质是__________ 。
(2)①处加入Fe2O3·H2O的目的是_________________ 。
(3)③处一般加入K2CO3溶液以吸收CO2 ,K2CO3溶液与CO2反应生成碳酸氢钾(KHCO3),该反应的化学方程式是_________________ 。
(4)如图是实验室模拟合成氨气的装置

(反应方程式:N2+3H2=2NH3)甲装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是_______________ ,从而提高氮气和氢气的利用率。
(5)该流程中参与循环的物质是_______________ 。

(1)合成氨的原料之一为氮气,该流程中为合成氨提供氮气的物质是
(2)①处加入Fe2O3·H2O的目的是
(3)③处一般加入K2CO3溶液以吸收CO2 ,K2CO3溶液与CO2反应生成碳酸氢钾(KHCO3),该反应的化学方程式是
(4)如图是实验室模拟合成氨气的装置

(反应方程式:N2+3H2=2NH3)甲装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是
(5)该流程中参与循环的物质是
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐1】归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示-——表示物质两两之间能发生化学反应。请根据如图,回答问题。(已知:CaCl2溶液呈中性,CaCl2+Na2CO3═CaCO3↓+2NaCl)

(1)甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈_________________ (填“酸性、碱性或中性”)。
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的现象是________________ ,此时含有的溶质有________ (酸碱指示剂除外)(用化学式填空,下同)。
(3)为验证乙同学所得溶液中含有的溶质,可取少量反应后的溶液滴加过量的____________ 溶液(填一种物质的化学式),产生_______________________________ 现象,则证明存在。

(1)甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的现象是
(3)为验证乙同学所得溶液中含有的溶质,可取少量反应后的溶液滴加过量的
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐2】碱式氯化铝是某种高效净水剂的主要成分。实验室利用铝土矿(主要含Al2O3,还含少量Fe2O3及其他不溶杂质)制取碱式氯化铝的过程如下:

(1)溶解过程中,需要使用质量分数为15%的盐酸,则配制这种盐酸需要________ mL 30%的浓盐酸(密度约为1.15 g/cm3)和115 g蒸馏水。
(2)盐酸溶解铝土矿过程中,发生反应的化学方程式为:____________________________________________ 。
(3)加少量铝粉的主要作用是除去浊液中的________ 。
(4)加CaCO3粉末的作用是调节pH至5。请写出用pH试纸测定溶液pH的操作:在白瓷板或玻璃片上放一小片pH试纸,____________________________________________ ,得出被测液的pH。

(1)溶解过程中,需要使用质量分数为15%的盐酸,则配制这种盐酸需要
(2)盐酸溶解铝土矿过程中,发生反应的化学方程式为:
(3)加少量铝粉的主要作用是除去浊液中的
(4)加CaCO3粉末的作用是调节pH至5。请写出用pH试纸测定溶液pH的操作:在白瓷板或玻璃片上放一小片pH试纸,
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐1】在实验室中找到一包久置的白色粉末,可能有 Ca(OH)2、NaOH、CuSO4、NH4Cl、BaCl2中的一种或几种,但由于时间推移,部分成分可能发生变质。为探究其成分,做如下实验(微溶按可溶处理):

(1)气体 1 的成分为______ ;
(2)烧碱可以干燥的气体有______(填序号);
(3)原样品中,由于物质发生变质,还可能有的物质是______ ;
(4)下列关于溶液和沉淀的设想中,正确的是______。

(1)气体 1 的成分为
(2)烧碱可以干燥的气体有______(填序号);
| A.CO | B.SO2 | C.NH3 | D.H2 |
(4)下列关于溶液和沉淀的设想中,正确的是______。
| A.除去 Ba(NO3)2溶液中的稀HNO3:加入过量的白色沉淀A,过滤 |
| B.鉴别稀盐酸和Ca(OH)2溶液:加入无色溶液a,观察现象 |
| C.除去铁制品表面的铁锈:加入过量无色溶液b,并长期浸泡 |
| D.向红色溶液d 通入少量CO2,液体会变浑浊 |
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
解题方法
【推荐2】周望同学在学完初中化学知识后,把常见八种物质的相互关系连接成如下图所示。已知B、C、F、G 属于四种不同类别的化合物(氧化物、酸、碱、盐),H为生活中最常见的调味品。(“→”表示一种物质可以通过一步反应转化为另一种物质,“—”表示相连的两种物质之间可以发生反应。反应条件、部分反应物和生成物已略去。)

(1)写出 H 物质的化学式___________ 。
(2)请写出 D→E 反应的化学方程___________ 。

(1)写出 H 物质的化学式
(2)请写出 D→E 反应的化学方程
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
【推荐3】下图表示某些物质间的转化关系。F是有机物,H的水溶液呈蓝色,部分反应条件和生成物已略去。

(1)化学式: A____________ ,F_____________ 。
(2)反应①、②的化学方程式:①______________ ② ____________ 。
(3)反应③在医学上可用于_____________ 病的检查。
(4)工业上可用B和G合成乙醇(C2H6O), 反应中B和G的质量比为______ 。

(1)化学式: A
(2)反应①、②的化学方程式:①
(3)反应③在医学上可用于
(4)工业上可用B和G合成乙醇(C2H6O), 反应中B和G的质量比为
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
【推荐1】某校实验室有一无色澄清废液,其中除了硝酸钠以外,可能还含有氢氧化钠、碳酸钠、硫酸钠、硝酸钡中的一种或几种。
实验活动一:探究该废液的组成。
取一定量的无色废液,进行如下图所示实验。

请回答下列问题:
(1)原无色废液呈___________ (填“酸性”“碱性”或“中性”),操作Ⅰ的名称为_____________ 。
(2)生成固体甲的化学方程式为_____________ 。
(3)原无色澄清废液中一定没有___________ (写名称或化学式均可,下同)。
实验活动二:处理废液得到较纯净的硝酸钠溶液。
将溶液A和原无色废液充分混和,无明显现象。接下来进行如下图所示实验。

(4)试剂①是____________ ,试剂②是____________ 。
实验活动一:探究该废液的组成。
取一定量的无色废液,进行如下图所示实验。

请回答下列问题:
(1)原无色废液呈
(2)生成固体甲的化学方程式为
(3)原无色澄清废液中一定没有
实验活动二:处理废液得到较纯净的硝酸钠溶液。
将溶液A和原无色废液充分混和,无明显现象。接下来进行如下图所示实验。

(4)试剂①是
您最近一年使用:0次
填空与简答-推断题
|
困难
(0.15)
解题方法
【推荐2】已知某固体混合物中可能含有(NH4)2SO4、FeCl3、CuSO4、Fe2O3四种物质中的两种或多种。按下图所示进行探究实验,出现的现象如图所述(设过程中所有发生的发应都恰好完全反应)。

试根据实验过程和图示提供的信息,进行分析推理,填写以下空白:
(1)气体 A 的气味是______ ;
(2)黄色溶液 F 的溶质是______ ;
(3)在溶液 E 中,一定大量存在的酸根离子是______ (填写离子符号);
(4)实验过程③中发生反应的化学方程式为______ ;
(5)该固体混合物中,还不能确定存在的是______ 。

试根据实验过程和图示提供的信息,进行分析推理,填写以下空白:
(1)气体 A 的气味是
(2)黄色溶液 F 的溶质是
(3)在溶液 E 中,一定大量存在的酸根离子是
(4)实验过程③中发生反应的化学方程式为
(5)该固体混合物中,还不能确定存在的是
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
【推荐3】蛇纹石矿可以看做 MgO、Fe2O3、Al2O3、SiO2 组成。由蛇纹石制取碱式碳酸镁的实验步骤如图所示:
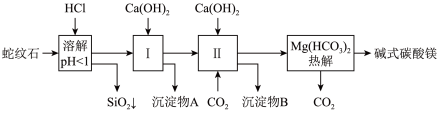
查阅资料:A.几种物质沉淀和溶解时的 pH 如下表
B.难溶性碱加热会生成两种氧化物,各元素化合价都不变。
探究一:制取碱式碳酸镁
(1)在操作Ⅰ中发生的中和反应是________ (用化学方程式表示)。
(2)进行操作Ⅰ时,需控制溶液 pH=6~7,Ca(OH)2 不能过量。若 Ca(OH)2 过量, 可能导致_______ 溶解、________ 沉淀。
(3)从沉淀混合物 A 中提取红色氧化物作颜料,先向沉淀物 A 中加入________ (填物质的化学式),然后_________ 、________ 、灼烧(依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是______ 。
探究二:确定产品碱式碳酸镁(mMgCO3·nMg(OH)2·xH2O)的组成,组装如图 1 仪器:

实验测得:硬质玻璃管中剩余的固体质量为 2.0g,C 处浓 H2SO4 增重 0.9g,D 处碱石灰增 重 1.76g。
(1)在装好试剂后,加热前应进行的操作是_______ ;
(2)A 框中装置的作用是________ ;
(3)通过计算写出碱式碳酸镁的化学式__________ 。(请写出计算过程)
【交流与反思】
(1)若将 E 框中的装置去掉,对实验结果的影响是 m 值________ ,x 值_______ (填“偏 大”、“偏小”或“不变”)
(2)已知碳酸镁和氢氧化镁在不同的温度下受热易分解为氧化物。为精确测定此碱式碳酸镁受热分解过程中时间与剩余固体质量的关系,结合以上数据,作出图 2 坐标系,试回答。

①t4~t5 时间段固体的化学式为__________ ;
②t5~t6 时间段发生反应的方程式为___________ 。

查阅资料:A.几种物质沉淀和溶解时的 pH 如下表
氢氧化物 | 溶液 pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | 沉淀不溶 | 沉淀不溶 |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| Mg(OH)2 | 8.6 | 11.1 | 沉淀不溶 | 沉淀不溶 |
探究一:制取碱式碳酸镁
(1)在操作Ⅰ中发生的中和反应是
(2)进行操作Ⅰ时,需控制溶液 pH=6~7,Ca(OH)2 不能过量。若 Ca(OH)2 过量, 可能导致
(3)从沉淀混合物 A 中提取红色氧化物作颜料,先向沉淀物 A 中加入
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是
探究二:确定产品碱式碳酸镁(mMgCO3·nMg(OH)2·xH2O)的组成,组装如图 1 仪器:

实验测得:硬质玻璃管中剩余的固体质量为 2.0g,C 处浓 H2SO4 增重 0.9g,D 处碱石灰增 重 1.76g。
(1)在装好试剂后,加热前应进行的操作是
(2)A 框中装置的作用是
(3)通过计算写出碱式碳酸镁的化学式
【交流与反思】
(1)若将 E 框中的装置去掉,对实验结果的影响是 m 值
(2)已知碳酸镁和氢氧化镁在不同的温度下受热易分解为氧化物。为精确测定此碱式碳酸镁受热分解过程中时间与剩余固体质量的关系,结合以上数据,作出图 2 坐标系,试回答。

①t4~t5 时间段固体的化学式为
②t5~t6 时间段发生反应的方程式为
您最近一年使用:0次




