实验室有一瓶长期放置的氢氧化钠固体,某兴趣小组同学欲对该固体变质情况进行探究.
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液呈中性
③盐酸加入到氢氧化钠和碳酸钠的混合溶液中,盐酸先和氢氧化钠反应
【提出猜想】猜想Ⅰ:固体未变质
猜想Ⅱ:___________
猜想Ⅲ:固体部分变质
【原因分析】氢氧化钠在空气中变质的原因是_____________________ (用化学方程式表示).
【进行实验】
小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是___________________ ;
小玲同学也取少量样品于烧杯中,用足量水溶解,再向溶液中滴加几滴稀盐酸,未发现有气泡产生。据此现象小玲认为NaOH未变质。你认为该结论是否正确?_____________
请说明理由__________________________________________ 。
为了进一步得出结论,该兴趣小组同学结合所给资料分工合作,集思广益,设计了下列实验进行验证。请将下表补充完整。
【反思评价】
(1)在实验步骤①中为什么要加入过量的CaCl2溶液?_______________________
(2)小玲同学认为在实验步骤①中可以用Ca(OH)2 溶液代替CaCl2证明这一瓶中是否含有NaOH,你认为呢?并说明理由__________________________ 。
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液呈中性
③盐酸加入到氢氧化钠和碳酸钠的混合溶液中,盐酸先和氢氧化钠反应
【提出猜想】猜想Ⅰ:固体未变质
猜想Ⅱ:
猜想Ⅲ:固体部分变质
【原因分析】氢氧化钠在空气中变质的原因是
【进行实验】
小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是
小玲同学也取少量样品于烧杯中,用足量水溶解,再向溶液中滴加几滴稀盐酸,未发现有气泡产生。据此现象小玲认为NaOH未变质。你认为该结论是否正确?
请说明理由_
为了进一步得出结论,该兴趣小组同学结合所给资料分工合作,集思广益,设计了下列实验进行验证。请将下表补充完整。
| 实验步骤 | 反应方程式 | 实验现象 | 结论 |
| ①将该样品配制成溶液,滴加过量CaCl2溶液 | 猜想Ⅲ正确 | ||
| ②对①进行过滤,向滤液中滴加 | 溶液变红 |
【反思评价】
(1)在实验步骤①中为什么要加入过量的CaCl2溶液?
(2)小玲同学认为在实验步骤①中可以用Ca(OH)2 溶液代替CaCl2证明这一瓶中是否含有NaOH,你认为呢?并说明理由
更新时间:2017-04-14 09:56:20
|
【知识点】 强碱露置在空气中的变质解读
相似题推荐
科学探究题
|
较难
(0.4)
解题方法
【推荐1】小明在帮老师整理实验室时,发现一瓶未密封的KOH固体,对其成分提出以下假设,并在老师的指导下进行实验探究。
【查阅资料】①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是_________ 。
②K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性。
【猜想假设】假设Ⅰ:只含KOH;假设Ⅱ:含KOH和K2CO3;假设Ⅲ:只含K2CO3。
【进行实验】
【问题讨论】步骤②中加入过量BaCl2溶液的作用是_________ ,排除对KOH检验的干扰。
【拓展应用】完全变质的KOH也有利用价值,从K2CO3的组成或性质看,这瓶变质的试剂在农业上的用途是________ 。
【查阅资料】①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是
②K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性。
【猜想假设】假设Ⅰ:只含KOH;假设Ⅱ:含KOH和K2CO3;假设Ⅲ:只含K2CO3。
【进行实验】
| 实验操作步骤 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入足量的稀盐酸 | 假设Ⅰ不正确 | |
| ②另取少量样品于试管中,加水溶解,加入过量的BaCl2溶液,振荡,静置 | ||
| ③取②中上层清液,滴加无色酚酞溶液 | 无色酚酞溶液不变色 | 假设Ⅲ正确 |
【问题讨论】步骤②中加入过量BaCl2溶液的作用是
【拓展应用】完全变质的KOH也有利用价值,从K2CO3的组成或性质看,这瓶变质的试剂在农业上的用途是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与NaOH溶液浓度大小有关;
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
(2)乙同学设计如图装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。

请写出CO2与NaOH溶液反应的化学方程式:_____ 。甲同学认为乙同学的实验不够严谨,理由是_____ 。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与NaOH溶液浓度大小有关;
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
| 实验步骤 | 设计这一步骤目的 | 实验现象 | 实验结论 |
| 1.将NaOH溶液加热煮沸 | 溶液变红,过一会儿红色消失 | 甲同学猜想 | |
| 2.向冷却后的溶液中滴入酚酞,并滴一些植物油在其上方 |

请写出CO2与NaOH溶液反应的化学方程式:
您最近一年使用:0次
【推荐3】学习酸碱中和反应时,同学们发现稀盐酸与氢氧化钠溶液混合在一起无明显现象。学习小组的同学们对其产生探究兴趣,于是他们分别从不同的角度探究酸碱中和反应。
(1)利用如图1所示的装置进行实验探究。用pH传感器测得烧杯中溶液的pH随滴加液体体积变化的曲线如图2所示。
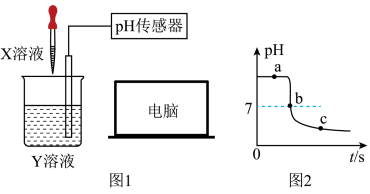
①反应前烧杯中盛放的液体Y是_______ 。(填写物质名称)
②图中a点所示溶液中的溶质是_______ 。(填写化学式)
③写出盐酸和氢氧化钠反应的化学方程式:_______ 。
【探究二】通过能量变化的角度,证明酸碱发生中和反应。
(2)毛毛同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,试管壁发烫,于是他得出酸碱中和反应是放热反应的结论,牛牛同学认为毛毛同学推理不合理,理由是_______ 。
(3)牛牛同学为了验证毛毛同学的结论,将实验加以改进:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出氢氧化钠溶液温度随加入稀硫酸质量的变化。如图①所示:

①由图知,稀硫酸与氢氧化钠溶液发生的反应是_______ (填“放热”或“吸热)反应。
②从A到B过程中,烧杯中溶液pH逐渐_______ (“增大”或“减小”),到达C时溶液中溶质有_______ 。
【探究三】通过溶液酸碱性变化的角度,证明酸碱发生中和反应。
(4)娇娇同学利用如图实验进行反应,证明碱与酸发生反应的现象是_______ 。

(5)明明同学观察到实验过程中有气泡产生,他认为氢氧化钠溶液已经变质,请你分析变质的原因_______ (用化学方程式表示)。
【探究四】
(6)酸碱中和反应的微观实质是_______ 。
(1)利用如图1所示的装置进行实验探究。用pH传感器测得烧杯中溶液的pH随滴加液体体积变化的曲线如图2所示。

①反应前烧杯中盛放的液体Y是
②图中a点所示溶液中的溶质是
③写出盐酸和氢氧化钠反应的化学方程式:
【探究二】通过能量变化的角度,证明酸碱发生中和反应。
(2)毛毛同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,试管壁发烫,于是他得出酸碱中和反应是放热反应的结论,牛牛同学认为毛毛同学推理不合理,理由是
(3)牛牛同学为了验证毛毛同学的结论,将实验加以改进:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出氢氧化钠溶液温度随加入稀硫酸质量的变化。如图①所示:

①由图知,稀硫酸与氢氧化钠溶液发生的反应是
②从A到B过程中,烧杯中溶液pH逐渐
【探究三】通过溶液酸碱性变化的角度,证明酸碱发生中和反应。
(4)娇娇同学利用如图实验进行反应,证明碱与酸发生反应的现象是

(5)明明同学观察到实验过程中有气泡产生,他认为氢氧化钠溶液已经变质,请你分析变质的原因
【探究四】
(6)酸碱中和反应的微观实质是
您最近一年使用:0次



