有一包粉末,可能由KCl、K2SO4、K2CO3、CuCl2、MgCl2中的一种或几种物质组成。现在做如下实验:
(1)根据以下实验操作及现象,请回答:
实验1:取少量粉末,加水溶解,得到无色透明溶液。
实验2:取1所得溶液少许,加入NaOH溶液,看不到明显现象。
实验3:取1所得溶液少许,加入足量硝酸钡溶液,出现白色沉淀。
实验4:将实验3所得混合物过滤后,在沉淀中加入足量稀硝酸,沉淀部分溶解并有气泡生成。原粉末中一定有_______________________ 。实验4中沉淀部分溶解的化学方程式为:____________________________ 。
(2)据上述实验现象,可推知原粉末中可能有______________ ,为了进一步验证原粉末中可能含有的成分是否存在,请你设计实验证明:
(1)根据以下实验操作及现象,请回答:
实验1:取少量粉末,加水溶解,得到无色透明溶液。
实验2:取1所得溶液少许,加入NaOH溶液,看不到明显现象。
实验3:取1所得溶液少许,加入足量硝酸钡溶液,出现白色沉淀。
实验4:将实验3所得混合物过滤后,在沉淀中加入足量稀硝酸,沉淀部分溶解并有气泡生成。原粉末中一定有
(2)据上述实验现象,可推知原粉末中可能有
操作步骤 | 现 象 | 结 论 |
该物质存在 |
更新时间:2017-05-04 20:52:10
|
相似题推荐
【推荐1】氢氧化钴Co(OH)2可作涂料和清漆的干燥剂,其制备方法是:把金属钴与稀盐酸反应制得氯化钴(CoCl2),再将氯化钴溶液与氢氧化钠溶液反应制得氢氧化钴。
查阅资料得知:氯化钴溶液是粉红色,氢氧化钴是难溶于水的粉红色固体。请回答:
(1)从物质分类的角度看,CoCl2属于________ (填选项)。
A化合物 B酸 C碱 D盐
(2)金属钴与稀盐酸反应的化学方程式为_________
(3)在氯化钴溶液中加入足量氢氧化钠溶液,发生了复分解反应其现象是________ ,化学方程式为________
(4)若有18g钴完全反应制备氢氧化钴理论上可以得到氢氧化钴________ g.
(5)下列说法正确的是________ (填字母)。
A钴的金属活动性比铜的强 B氢氧化钴可以干燥氯化氢气体
C氯化钴溶液也能和石灰水反应 D金属钴与盐酸反应后的溶液质量变小
查阅资料得知:氯化钴溶液是粉红色,氢氧化钴是难溶于水的粉红色固体。请回答:
(1)从物质分类的角度看,CoCl2属于
A化合物 B酸 C碱 D盐
(2)金属钴与稀盐酸反应的化学方程式为
(3)在氯化钴溶液中加入足量氢氧化钠溶液,发生了复分解反应其现象是
(4)若有18g钴完全反应制备氢氧化钴理论上可以得到氢氧化钴
(5)下列说法正确的是
A钴的金属活动性比铜的强 B氢氧化钴可以干燥氯化氢气体
C氯化钴溶液也能和石灰水反应 D金属钴与盐酸反应后的溶液质量变小
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】为验证CO2和氢氧化钠确实能发生化学反应,某同学将收集满二氧化碳的两支试管(相同规格)分别倒立在水和氢氧化钠溶液中,轻轻晃动试管,产生了如图所示现象。

(1)写出CO2与氢氧化钠溶液反应的化学方程式______ 。
(2)甲实验的目的是什么?
(3)请设计实验证明实验乙中反应后的溶液中还含有氢氧化钠。(简要写出实验的步骤、现象和结论)。

(1)写出CO2与氢氧化钠溶液反应的化学方程式
(2)甲实验的目的是什么?
(3)请设计实验证明实验乙中反应后的溶液中还含有氢氧化钠。(简要写出实验的步骤、现象和结论)。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】从A~G中选出适当的选项分别用字母代号填写在下面的横线上。
A 熔点 B.沸点 C.酸性 D.碱性 E.颜色 F.溶解性
(1)利用物质的___________ 不同,工业上用液态空气制氧气;
(2)由于固体NaCl和CaCO3的___________ 不同,可用水加以鉴别;
(3)根据___________ 不同,可以最快区别硫酸铜溶液和硝酸钾溶液;
A 熔点 B.沸点 C.酸性 D.碱性 E.颜色 F.溶解性
(1)利用物质的
(2)由于固体NaCl和CaCO3的
(3)根据
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
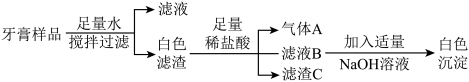
【推荐2】粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2、MgCl2)。现以粗盐为原料制取精盐,生产过程如图。

(1)写出I中发生反应的化学方程式______ 。
(2)操作a的名称是______ 。
(3)加入适量稀盐酸的作用是除去滤液中的______ (填化学式)。

(1)写出I中发生反应的化学方程式
(2)操作a的名称是
(3)加入适量稀盐酸的作用是除去滤液中的
您最近一年使用:0次
【推荐3】一年的化学学习,我们对化学反应有了一定的认识。
(1)判断反应的发生。如氢氧化镁和稀硫酸的反应,可以通过_______ 现象判断反应的发生。
(2)所有化学反应都遵循质量守恒定律。如4g氢气和16g氧气充分反应,生成水的质量为_______ g。
(3)判断金属活动性顺序。如对镁和铜的金属活动性进行探究:
③若实验前加入的镁条质量为ag,反应一段时间后过滤,将所得固体洗涤、干燥,称其质量仍为ag,则生成气体与铜的质量比为_______ 。
(1)判断反应的发生。如氢氧化镁和稀硫酸的反应,可以通过
(2)所有化学反应都遵循质量守恒定律。如4g氢气和16g氧气充分反应,生成水的质量为
(3)判断金属活动性顺序。如对镁和铜的金属活动性进行探究:
| 操作 | 主要现象 | 结论 |
| 镁条表面有红色固体析出;镁条表面有气泡产生 | ①活动性:Mg ②硫酸铜溶液中可能含有 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】有一包固体物质,含有NaCl、MgSO4,某化学兴趣小组为了除去其中的MgSO4,得到纯净的NaCl,设计如图实验方案。
(2)将所得滤渣放入烧杯中,加入足量稀盐酸,有气泡出现,写出有气泡生成的化学方程式。
(3)请设计实验证明所得滤液2中除了NaCl之外,还含有哪些溶质?(简要写出实验步骤、现象和结论)

(2)将所得滤渣放入烧杯中,加入足量稀盐酸,有气泡出现,写出有气泡生成的化学方程式。
(3)请设计实验证明所得滤液2中除了NaCl之外,还含有哪些溶质?(简要写出实验步骤、现象和结论)
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】①将一种白色固体A和一种黑色固体B按一定比例混合后加热,产生一种无色无味的气体C;
②取淡黄色粉末D点燃放入气体C中,会产生蓝紫色火焰,生成一种有刺激性气味的气体E。试回答:
(1)A、B各是什么物质:________ 、________
(2)写出上述反应②的文字表达式:________ 。
②取淡黄色粉末D点燃放入气体C中,会产生蓝紫色火焰,生成一种有刺激性气味的气体E。试回答:
(1)A、B各是什么物质:
(2)写出上述反应②的文字表达式:
您最近一年使用:0次