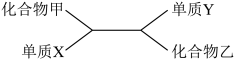
我们常用下列装置进行实验:
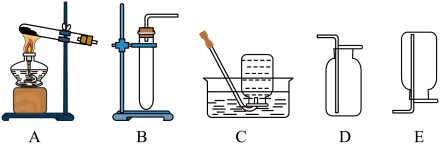
(1)实验室可用B装置制取多种气体,请你写出实验室用B装置制取氢气的化学方程式:______________________________ ,该气体的收集装置 可以是______ (填字母编号,下同)。
(2)实验室常用加热固体甲和固体乙的混合物来制取气体丙,则制取丙选用的发生装置 是______ ;若收集气体丙时只能 用C装置,则可推知丙的性质可能有___________________ (答一条即可)。

(1)实验室可用B装置制取多种气体,请你写出实验室用B装置制取氢气的化学方程式:
(2)实验室常用加热固体甲和固体乙的混合物来制取气体丙,则制取丙选用的
更新时间:2017-05-04 08:21:39
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
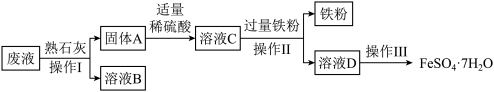
【推荐1】某化学兴趣小组用除铁锈后的废液(主要含FeCl3、FeCl2、HCl〕制备FeSO4﹒7H2O,其流程如下:
【查阅资料】铁能与硫酸铁反应,生成硫酸亚铁。化学方程式: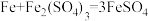 :
:
(1)写出熟石灰与废液中的某物质发生中和反应的化学方程式______________ 。
(2)操作Ⅰ的名称是_____________ ,所得固体A需洗涤,具体的操作是:取最后一次洗涤后的滤液,向其中滴加___________ ,无明显现象,则表示固体已洗净,所得溶液B的溶质一定有___________ (填化学式)。
(3)向洗涤后的固体A中加入稀硫酸,发生的化学反应方程式为___________ (写一个即可)。
(4)操作Ⅱ加入过量铁粉的作用是___________________ 。
(5)已知硫酸亚铁的溶解度和析出晶体的组成如下表:
根据上表,硫酸亚铁晶体(FeSO4﹒7H2O)冷却结晶温度最高不超过_____________ ℃。
(6)得到的FeSO4﹒7H2O晶体应该用________________ 洗涤(填序号)。
a.水b.饱和硫酸亚铁溶液c.稀硫酸

【查阅资料】铁能与硫酸铁反应,生成硫酸亚铁。化学方程式:
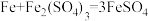 :
:(1)写出熟石灰与废液中的某物质发生中和反应的化学方程式
(2)操作Ⅰ的名称是
(3)向洗涤后的固体A中加入稀硫酸,发生的化学反应方程式为
(4)操作Ⅱ加入过量铁粉的作用是
(5)已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
| 析出晶体 | FeSO4﹒7H2O | FeSO4﹒ 4H2O | FeSO4﹒H2O | |||||||
(6)得到的FeSO4﹒7H2O晶体应该用
a.水b.饱和硫酸亚铁溶液c.稀硫酸
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】五氧化二钒(V2O5)是一种工业催化剂,下图是制取V2O5的工艺流程。

(1)写出反应①的化学方程式____________________________________ ;
(2)操作a的名称是____________ ;实验室进行该操作所需的玻璃仪器有烧杯,玻璃棒和____________ ;
(3)反应②的反应类型是____________ ;物质X一定含有的元素是___________ ;(填元素符号)

(1)写出反应①的化学方程式
(2)操作a的名称是
(3)反应②的反应类型是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】氢气是一种极具发展潜力的新能源,它的开发,储存与利用是目前研究的热点。
I.制氢
(1)工业上以CH4为原料生产H2,制取原理如图15所示:
①“转化炉”中有H2产生,参加反应的CH4与H2O的质量比是_______ 。
②“洗涤塔”中发生反应的化学方程式为_______ ,气体从塔底通入,NaOH溶液从塔顶喷淋。这样操作优点是_______ 。
Ⅱ.储氢
(2)Mg2Cu是一种性价比高、绿色环保的贮氢合金,其贮氢与释氢过程如图16。_______ 。
②释氢过程中,发生反应的化学方程式为_______ 。释氢开始时反应速率较快,然后反应速率迅速减小,最终停止,导致较多量的MgH2剩余。反应速率迅速减小并最终停止的原因是_______ 。
Ⅲ.用氢
(3)①北京冬奥会使用的氢能客车搭载“氢腾”燃料电池系统,“氢腾”燃料电池工作时的能量转化形式为_______ 能转化为电能。
②“绿色化学”的特点之一是“零排放”。一定条件下,二氧化碳和氢气可以按照不同比例、反应,生成下列有机物。其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是_______ (填字母序号,下同)。
A.甲醇(CH4O) B.甲酸(CH2O2) C.乙醇(C2H6O) D.乙酸(C2H4O2)
I.制氢
(1)工业上以CH4为原料生产H2,制取原理如图15所示:
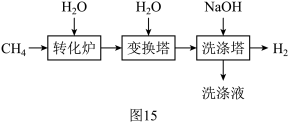

①“转化炉”中有H2产生,参加反应的CH4与H2O的质量比是
②“洗涤塔”中发生反应的化学方程式为
Ⅱ.储氢
(2)Mg2Cu是一种性价比高、绿色环保的贮氢合金,其贮氢与释氢过程如图16。
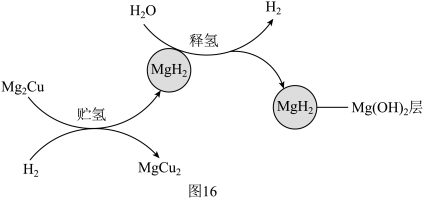
②释氢过程中,发生反应的化学方程式为
Ⅲ.用氢
(3)①北京冬奥会使用的氢能客车搭载“氢腾”燃料电池系统,“氢腾”燃料电池工作时的能量转化形式为
②“绿色化学”的特点之一是“零排放”。一定条件下,二氧化碳和氢气可以按照不同比例、反应,生成下列有机物。其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是
A.甲醇(CH4O) B.甲酸(CH2O2) C.乙醇(C2H6O) D.乙酸(C2H4O2)
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】氢气被看做是理想的“绿色能源”,氢气的制备和储存是目前的研究热点。
(一)甲烷水蒸气催化重整是制高纯氢的方法之一,主要流程如下:
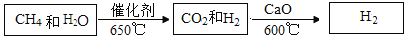
(1)甲烷和水蒸气反应的化学方程式是______ 。
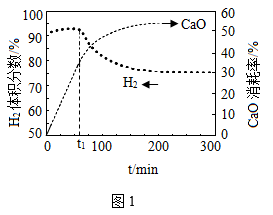
(2)用CaO可以将CO2除去转化为CaCO3,H2体积分数和CaO消耗率随时间变化关系如图1所示。从t1时开始,H2体积分数显著降低,单位时间CaO消耗率______ (填“升高”、“降低”或“不变”)。此时CaO消耗率约为35%,但已失效,结合反应解释原因:______ 。
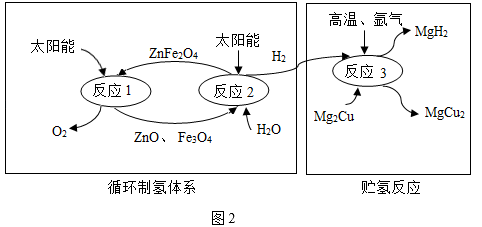
(二)图2是利用贮氢合金通过化学反应贮存氢气的方法。
资料:Mg2Cu是一种贮氢合金,在高温下能与氧气反应。
Mg2Cu吸氢后生成MgH2和MgCu2合金。
MgH2和HCl反应的化学方程式为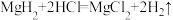 。
。
(3)循环制氢反应中得到的氢气和氧气的质量比为______ ;
(4)贮氢反应中通入氩气的目的是______ ;
(5)反应2产生的氢气质量______ (填“>”、“<”或“=”)反应3所得混合物与足量稀盐酸反应生成的氢气质量。
(一)甲烷水蒸气催化重整是制高纯氢的方法之一,主要流程如下:
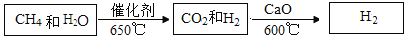
(1)甲烷和水蒸气反应的化学方程式是
(2)用CaO可以将CO2除去转化为CaCO3,H2体积分数和CaO消耗率随时间变化关系如图1所示。从t1时开始,H2体积分数显著降低,单位时间CaO消耗率


(二)图2是利用贮氢合金通过化学反应贮存氢气的方法。
资料:Mg2Cu是一种贮氢合金,在高温下能与氧气反应。
Mg2Cu吸氢后生成MgH2和MgCu2合金。
MgH2和HCl反应的化学方程式为
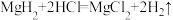 。
。(3)循环制氢反应中得到的氢气和氧气的质量比为
(4)贮氢反应中通入氩气的目的是
(5)反应2产生的氢气质量
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
Ⅰ.制氢。铁酸锌(ZnFe2O4)可用于循环分解水制备氢气,反应原理可表示为:6ZnFe2O4 6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O 3ZnFe2O4+H2↑。
3ZnFe2O4+H2↑。
(1)ZnFe2O4中Fe的化合价是______ 。
(2)该制氢方法中不断消耗的物质是______ ,得到氢气和氧气的质量比是______ 。
(3)该制氢法中所用水不可以是硬水,可以用______ (填写试剂名称)鉴别。
Ⅱ.储氢。传统的储氢方法是将大量气体压缩后储存在钢瓶中,压缩气体可以____ (a.减小气体分子的体积;b.减小气体分子间空隙);合金Mg2Cu是一种优良的储氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔合制得。该合金在一定条件下能吸收氢气生成金属氢化物和另一种合金:2Mg2Cu+3H2  3MgH2+MgCu2。
3MgH2+MgCu2。
注:铜莫氏硬度:3,镁莫氏硬度2.5;已知最软物质滑石莫氏硬度为1,最硬物质金刚石莫氏硬度为10。
(1)制备合金Mg2Cu时用氩气保护,原因是______ 。
A.氩气化学性质稳定 B.氩气密度比空气大 C.氩气燃烧时放出大量的热
(2)写出合金Mg2Cu的莫氏硬度范围______ 。
(3)氢化物MgH2中H的化合价是______ ;MgH2能与水反应生成氢氧化镁,并释出氢气,写出反应的化学方程式_______ 。
Ⅰ.制氢。铁酸锌(ZnFe2O4)可用于循环分解水制备氢气,反应原理可表示为:6ZnFe2O4
 6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O 3ZnFe2O4+H2↑。
3ZnFe2O4+H2↑。(1)ZnFe2O4中Fe的化合价是
(2)该制氢方法中不断消耗的物质是
(3)该制氢法中所用水不可以是硬水,可以用
Ⅱ.储氢。传统的储氢方法是将大量气体压缩后储存在钢瓶中,压缩气体可以
 3MgH2+MgCu2。
3MgH2+MgCu2。注:铜莫氏硬度:3,镁莫氏硬度2.5;已知最软物质滑石莫氏硬度为1,最硬物质金刚石莫氏硬度为10。
(1)制备合金Mg2Cu时用氩气保护,原因是
A.氩气化学性质稳定 B.氩气密度比空气大 C.氩气燃烧时放出大量的热
(2)写出合金Mg2Cu的莫氏硬度范围
(3)氢化物MgH2中H的化合价是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】根据下图装置,回答下列有关问题:
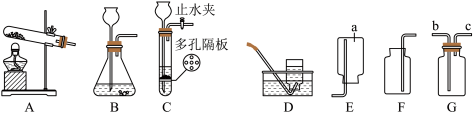
(1)装置图中仪器a的名称为___________________ 。
(2)采用加热氯酸钾和二氧化锰的混合物制取氧气,可选用的发生装置和收集装置的组合是_____________________ ,该反应的化学方程式是 ____________________ 。
(3)若用B装置来制取氧气,反应的化学方程式为_________________________________ 。
(4)若用G装置采用排空法收集氢气,氢气应从 进_______________ 。(选“b”或“c”)
(5)制取二氧化碳最好选用的发生装置是______ ,该装置与另一个可选用的装置相比,其主要优点是 _____________________________________ 。
(6)若用F装置收集二氧化碳气体,验满的方法是__________________________________________ 。

(1)装置图中仪器a的名称为
(2)采用加热氯酸钾和二氧化锰的混合物制取氧气,可选用的发生装置和收集装置的组合是
(3)若用B装置来制取氧气,反应的化学方程式为
(4)若用G装置采用排空法收集氢气,氢气应从 进
(5)制取二氧化碳最好选用的发生装置是
(6)若用F装置收集二氧化碳气体,验满的方法是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】结合下图所示实验装置,回答下列问题:
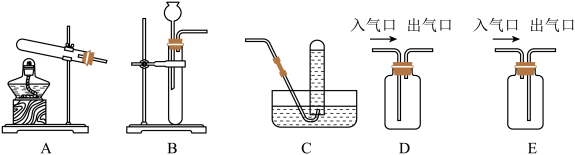
(1)实验室用碳酸钙制取二氧化碳气体时,应选用气体发生装置_______ (填字母),其反应的化学方程式为____________________ 。若将CO2和水蒸气混合气体通过盛装_____________ (填试剂名称)的D装置,可以得到干燥的CO2气体。
(2)实验室用氯酸钾和二氧化锰制取氧气,其反应的化学方程式为_____________________ 。实验结束后,从反应残留物中提取二氧化锰的主要操作步骤是溶解、___________ (填操作名称),第二步使用玻璃棒作用是__________________ 。
(3)实验室常用氯化铵和氢氧化钙固体加热反应来制取NH3。NH3是一种没有颜色而有刺激性气味的气体,极易溶于水,密度比空气小。那么,收集 NH3的装置为上图中的
____________ (填字母)。
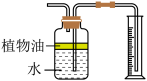
(4)将E装置改为下图,可用来测量生成的CO2气体的体积,在水面上放一层植物油的目的是__________________ ,植物油上方原有的空气对实验的结果____ (填“有”或“没有”)明显影响。

(1)实验室用碳酸钙制取二氧化碳气体时,应选用气体发生装置
(2)实验室用氯酸钾和二氧化锰制取氧气,其反应的化学方程式为
(3)实验室常用氯化铵和氢氧化钙固体加热反应来制取NH3。NH3是一种没有颜色而有刺激性气味的气体,极易溶于水,密度比空气小。那么,
(4)将E装置改为下图,可用来测量生成的CO2气体的体积,在水面上放一层植物油的目的是

您最近一年使用:0次
填空与简答-科普阅读题
|
较难
(0.4)
【推荐1】波尔多液的制备及组成测定波尔多液是常见的杀菌剂,为天蓝色碱性悬浊液。以硫酸铜、生石灰及水为原料,制备波尔多液。为测定从波尔多液中分离出的天蓝色固体[CuSO4•aCu(OH)2•bCa(OH)2•cH2O]的组成,设计如下实验:
【实验】称取64.4g天蓝色固体,加入足量稀HNO3使其完全溶解,再加入过量Ba(NO3)2溶液,过滤,洗涤干燥得白色固体23.3g。
(1)判断 Ba(NO3)2溶液已过量的方法是:静置,向上层清液中滴加______ 溶液,无现象。
(2)不能在铁制容器中配波尔多液。请用化学方程式解释原因______ 。
【实验Ⅱ】另取64.4g天蓝色固体,用如图装置进行热分解实验
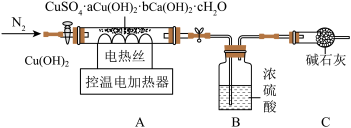
【资料】①CuSO4、Cu(OH)2、Ca(OH)2在一定温度下能受热分解,分别生成两种氧化物,分解过程中各元素的化合价均不改变。
②天蓝色固体在110℃时,完全失去结晶水。
③Cu(OH)2在100℃时分解完全。CuSO4和Ca(OH)2在580℃左右时开始分解,到650℃时均能分解完全。
④浓硫酸可用于吸收SO3。
(3)按图连接好装置,实验前要先______ 。
(4)控制温度在110℃充分加热,测得B装置增重10.8g。再升温至650℃充分加热,B装置又增重了15.2g。最终剩余固体中的成分是______ 。
(5)整个加热过程中,天蓝色固体分解生成水的总质量为______ g。
(6)天蓝色固体CuSO4•aCu(OH)2•bCa(OH)2•cH2O中,a:b:c=______ 。
【实验】称取64.4g天蓝色固体,加入足量稀HNO3使其完全溶解,再加入过量Ba(NO3)2溶液,过滤,洗涤干燥得白色固体23.3g。
(1)判断 Ba(NO3)2溶液已过量的方法是:静置,向上层清液中滴加
(2)不能在铁制容器中配波尔多液。请用化学方程式解释原因
【实验Ⅱ】另取64.4g天蓝色固体,用如图装置进行热分解实验

【资料】①CuSO4、Cu(OH)2、Ca(OH)2在一定温度下能受热分解,分别生成两种氧化物,分解过程中各元素的化合价均不改变。
②天蓝色固体在110℃时,完全失去结晶水。
③Cu(OH)2在100℃时分解完全。CuSO4和Ca(OH)2在580℃左右时开始分解,到650℃时均能分解完全。
④浓硫酸可用于吸收SO3。
(3)按图连接好装置,实验前要先
(4)控制温度在110℃充分加热,测得B装置增重10.8g。再升温至650℃充分加热,B装置又增重了15.2g。最终剩余固体中的成分是
(5)整个加热过程中,天蓝色固体分解生成水的总质量为
(6)天蓝色固体CuSO4•aCu(OH)2•bCa(OH)2•cH2O中,a:b:c=
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】氯化亚铜在工业上应用广泛。氯化亚铜(CuCl)为白色晶体,微溶于水,能溶于氨水、浓盐酸,并生成配合物,不溶于硫酸、稀硝酸和醇。下图是工业制取氯化亚铜的生产流程图。
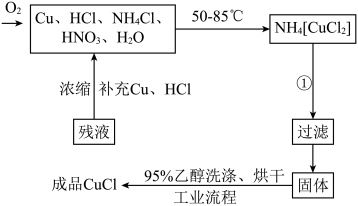
(1)已知反应①获得CuCl发生的是分解反应,写出该反应的化学方程式_______ 。
(2)用95%乙醇代替蒸馏水洗涤的主要目的是__________________________ 。
(3)除水以外流程中可以循环利用的物质有_____________ 。
(4)实验室可以用如图甲装置制备CuCl:
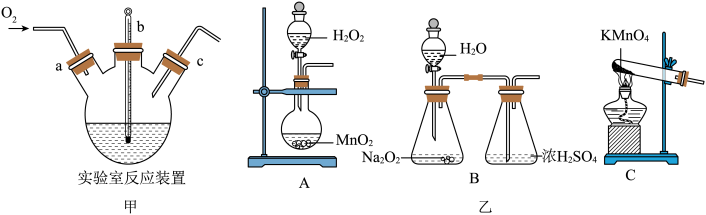
实验药品:铜丝20g、氯化铵20g、65% 硝酸10mL、36%盐酸15mL、水。
图乙中的A、B、C三套装置均有足量的氧气生成。
①实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,最宜选择图乙中的_____ 装置(填字母序号A、B、C)。
②按要求在反应装置甲中放入指定的实验药品后,发现温度计显示反应液温度明显低于室温,原因可能是_________________________________________ 。

(1)已知反应①获得CuCl发生的是分解反应,写出该反应的化学方程式
(2)用95%乙醇代替蒸馏水洗涤的主要目的是
(3)除水以外流程中可以循环利用的物质有
(4)实验室可以用如图甲装置制备CuCl:

实验药品:铜丝20g、氯化铵20g、65% 硝酸10mL、36%盐酸15mL、水。
图乙中的A、B、C三套装置均有足量的氧气生成。
①实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,最宜选择图乙中的
②按要求在反应装置甲中放入指定的实验药品后,发现温度计显示反应液温度明显低于室温,原因可能是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】某兴趣小组通过以下实验方案对空气中的氮气进行探究。

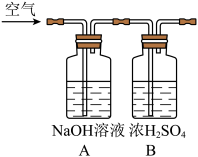
(1)除去二氧化碳和水蒸气:如图中装置A、B顺序能否颠倒________ (填“能”或“否”)。
(2)除去氧气:该小组根据教材中拉瓦锡研究空气成分的实验原理,除去了(1)中得到的气体中的氧气。在拉瓦锡的经典实验中(装置如图),使用汞的优点有_______ 。
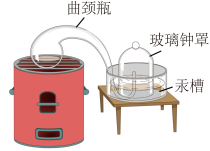
A 汞为液态,在加热的条件下只与氧气反应且生成物为固体
B 时间足够长,能将密闭装置中的氧气几乎耗尽
C 无法观察装置中气体体积的变化
D 得到的氧化汞粉末加热生成的气体体积+剩余气体体积=原空气体积
(3)分析误差:该小组按设计方案得到的氮气密度(假设要除去的气体均已除净)与氮气的实际密度有误差,产生误差的原因是_______________ 。
(4)拓展与延伸:实验室如何制取氮气呢?
请阅读资料并回答下列问题:
资料:1.重铬酸铵为橘黄色粉末,加热至180℃时可分解得到氮气;
2.氮气的化学性质不活泼,常温下很难跟其他物质发生反应,但在高温或点燃条件下可与某些物质反应,如镁能够在氮气中燃烧。
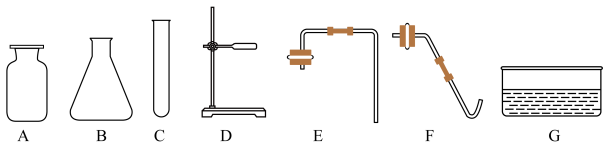
①仪器B的名称是______ 。
②利用上述仪器和重铬酸铵在实验室制取少量氮气,其发生装置应选择的仪器有_____
(填序号),还必须 补充的一种仪器是___ 。若用上述装置制氧气,反应的化学方程式为___________________________________ 。
③根据已有知识,收集氮气只能用________ 法。

(1)除去二氧化碳和水蒸气:如图中装置A、B顺序能否颠倒

(2)除去氧气:该小组根据教材中拉瓦锡研究空气成分的实验原理,除去了(1)中得到的气体中的氧气。在拉瓦锡的经典实验中(装置如图),使用汞的优点有

A 汞为液态,在加热的条件下只与氧气反应且生成物为固体
B 时间足够长,能将密闭装置中的氧气几乎耗尽
C 无法观察装置中气体体积的变化
D 得到的氧化汞粉末加热生成的气体体积+剩余气体体积=原空气体积
(3)分析误差:该小组按设计方案得到的氮气密度(假设要除去的气体均已除净)与氮气的实际密度有误差,产生误差的原因是
(4)拓展与延伸:实验室如何制取氮气呢?
请阅读资料并回答下列问题:
资料:1.重铬酸铵为橘黄色粉末,加热至180℃时可分解得到氮气;
2.氮气的化学性质不活泼,常温下很难跟其他物质发生反应,但在高温或点燃条件下可与某些物质反应,如镁能够在氮气中燃烧。

①仪器B的名称是
②利用上述仪器和重铬酸铵在实验室制取少量氮气,其发生装置应选择的仪器有
(填序号),还
③根据已有知识,收集氮气只能用
您最近一年使用:0次