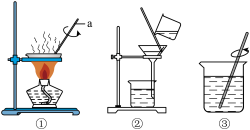
某 NaCl 样品中含少量 MgCl2、CaCl2等杂质,现要提纯 NaCl 样品。请回答:
(1)提纯中用到以下操作步骤,写出有关试剂或主要操作的名称。
①加水溶解;②依次加入过量的 NaOH 溶液、Na2CO3溶液;③___________ ;④加入适量的_____________ ;⑤蒸发结晶。
(2)加入过量的 NaOH 溶液,除去的离子是____________ (填离子符号)。
(3)加入过量的 Na2CO3溶液,所发生反应的化学方程式为_______________________ 。
(4)在“蒸发结晶”的操作中,容易造成食盐固体飞溅,为尽量减少飞溅,除用玻璃棒不断搅拌外,还可以采取的方法是_____________________________ 。
(1)提纯中用到以下操作步骤,写出有关试剂或主要操作的名称。
①加水溶解;②依次加入过量的 NaOH 溶液、Na2CO3溶液;③
(2)加入过量的 NaOH 溶液,除去的离子是
(3)加入过量的 Na2CO3溶液,所发生反应的化学方程式为
(4)在“蒸发结晶”的操作中,容易造成食盐固体飞溅,为尽量减少飞溅,除用玻璃棒不断搅拌外,还可以采取的方法是
更新时间:2017-05-27 09:08:24
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】为了测定粗盐(混有少量的泥沙及可溶性杂质)中氯化钠的纯度,进行如下操作:
①a 计算产率,b 过滤,c 溶解,d 蒸发,e 称量粗盐,f 称量精盐。实验步骤的正确顺序是:________ 、a(填编号)。
②称量时正确的操作次序是_______ (填字母序号)。
a 校正,b 去皮,c 放称量纸,d 放食盐,e 读数
③过滤时用到的玻璃仪器有玻璃棒、烧杯、_______ ,其中玻璃棒的作用是_______ 。实验过程中发现过滤两次滤液仍然浑浊,可能的原因是(写一点)___________ 。
④最后得到的精盐属于__________ (填“混合物”或“纯净物”)。
⑤已知:产率=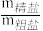 ×100%。各小组的产率及评价如下,对造成产率偏高或偏低的原因分析,正确的是
×100%。各小组的产率及评价如下,对造成产率偏高或偏低的原因分析,正确的是________ 。
A 第1组:烧杯里的食盐未溶解完就开始过滤
B 第2组:没有蒸发干,精盐中仍然有水分
C 第3组:滤液浑浊就开始蒸发
D 第4组:过滤时滤液高于滤纸的边缘
①a 计算产率,b 过滤,c 溶解,d 蒸发,e 称量粗盐,f 称量精盐。实验步骤的正确顺序是:
②称量时正确的操作次序是
a 校正,b 去皮,c 放称量纸,d 放食盐,e 读数
③过滤时用到的玻璃仪器有玻璃棒、烧杯、
④最后得到的精盐属于
| 组别 | 1 | 2 | 3 | 4 |
| 产率 | 75% | 65% | 88% | 72% |
| 教师评价 | 偏低 | 偏低 | 偏高 | 偏低 |
⑤已知:产率=
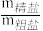 ×100%。各小组的产率及评价如下,对造成产率偏高或偏低的原因分析,正确的是
×100%。各小组的产率及评价如下,对造成产率偏高或偏低的原因分析,正确的是A 第1组:烧杯里的食盐未溶解完就开始过滤
B 第2组:没有蒸发干,精盐中仍然有水分
C 第3组:滤液浑浊就开始蒸发
D 第4组:过滤时滤液高于滤纸的边缘
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】用下列实验操作可分别完成“粗盐中难溶性杂质的去除”和“一定溶质质量分数的氯化钠溶液的配制”两个实验。

(1)“粗盐中难溶性杂质的去除”的实验操作步骤为___________________ 。
(2)操作E中得到的滤液仍浑浊,其原因可能是_______ (答出一点即可)。
(3)若图B所用的烧杯内壁沾有水,导致配制溶液中溶质的质量分数会_______ (填“偏大”、“偏小”或“不变”)。
(4)图D中玻璃棒的作用是_______________ 。
(5)图C中有一处明显的错误,请你改正:______________ 。

(1)“粗盐中难溶性杂质的去除”的实验操作步骤为
(2)操作E中得到的滤液仍浑浊,其原因可能是
(3)若图B所用的烧杯内壁沾有水,导致配制溶液中溶质的质量分数会
(4)图D中玻璃棒的作用是
(5)图C中有一处明显的错误,请你改正:
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】同学们完成实验后留下的废液中含有K2CO3、KCl和Na2SO4三种物质,在老师的指导下,化学小组的同学设计以下流程回收KCl晶体。
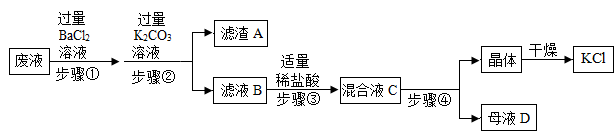
请回答:
(1)步骤①反应的化学方程式_____________________ 、________________ 。
(2)步骤②加入过量K2CO3溶液的目的是__________________ ;滤液B中的溶质是_______________ 、_____________ 、_______________ (写化学式)。
(3)在步骤③中判断盐酸适量的现象是________________________ 。
(4)混合液C中的溶质是KCl和NaCl,观察溶解度曲线,步骤④所包含的具体操作是_____________ 、降温结晶、过滤。降温结晶的最佳温度范围是______ ℃以下,晶体表面的杂质最好用_____________ 进行洗涤。


请回答:
(1)步骤①反应的化学方程式
(2)步骤②加入过量K2CO3溶液的目的是
(3)在步骤③中判断盐酸适量的现象是
(4)混合液C中的溶质是KCl和NaCl,观察溶解度曲线,步骤④所包含的具体操作是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】为了除去粗盐中MgCl2、CaC12、Na2SO4等可溶性杂质,需要进行如下操作:①溶解;②依次加入过量的NaOH、BaC12、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。加入过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,还有一个作用是___________ (用化学方程式表示);NaOH溶液和BaC12溶液的加入顺序___________ (填“可以”或“不可以”)调换。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】粗盐中含有MgCl2、CaCl2等杂质,工业提纯粗盐的工艺流程如下图所示:

(1)Na2CO3溶液的pH________ 7(选填“>”“=”或“<”);步骤②的实验目的是________ 。
(2)步骤③操作a的名称是________ 。步骤④加入适量盐酸的目的是除去滤液中的Na2CO3和________ 。
(3)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有________ 。

(1)Na2CO3溶液的pH
(2)步骤③操作a的名称是
(3)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有
您最近一年使用:0次
【推荐2】下图是实验室模拟“侯氏制碱法”生产纯碱的工艺流程图。________ (填实验名称),通过步骤Ⅲ所得滤渣的成分是________ 。
(2)步骤Ⅰ和步骤Ⅱ的顺序不能颠倒,否则___________ 。
(3)用实际参加反应的离子符号表示化学反应的式子叫做离子方程式,复分解反应的实质就是反应物的离子间结合生成了沉淀、气体或水。请用离子方程式表示步骤Ⅱ的反应___________ 。
(4)步骤Ⅳ与步骤Ⅴ之间还有一步重要操作,其名称是___________ ;步骤Ⅴ若先通入CO2再通入NH3,造成的后果是___________ 。

(2)步骤Ⅰ和步骤Ⅱ的顺序不能颠倒,否则
(3)用实际参加反应的离子符号表示化学反应的式子叫做离子方程式,复分解反应的实质就是反应物的离子间结合生成了沉淀、气体或水。请用离子方程式表示步骤Ⅱ的反应
(4)步骤Ⅳ与步骤Ⅴ之间还有一步重要操作,其名称是
您最近一年使用:0次