实验室现有硫酸镁和硫酸钠的固体混合物样品,小明同学想测定样品中硫酸镁的质量分数,先称取该混合物样品20g,完全溶于100g水中。然后取用了一定溶质质量分数的氢氧化钠溶液100 g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
(1)上表中X的数值为______;原固体混合物样品中硫酸镁的质量分数是 ;
(2)求恰好完全反应时,溶液中溶质的质量分数。(结果精确到0.1%)
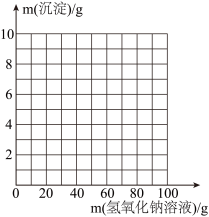
(3)请在下图中画出在20 g 样品中加氢氧化钠溶液的质量与产生沉淀质量变化关系的示意图。
(4)若用氢氧化钡溶液代替氢氧化钠溶液来测定样品中硫酸镁的质量分数,是否可行?并说明理由。
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
| 生成沉淀的质量/g | 2.9 | X | 8.7 | 8.7 |
(1)上表中X的数值为______;原固体混合物样品中硫酸镁的质量分数是 ;
(2)求恰好完全反应时,溶液中溶质的质量分数。(结果精确到0.1%)
(3)请在下图中画出在20 g 样品中加氢氧化钠溶液的质量与产生沉淀质量变化关系的示意图。

(4)若用氢氧化钡溶液代替氢氧化钠溶液来测定样品中硫酸镁的质量分数,是否可行?并说明理由。
更新时间:2017-06-28 19:58:10
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】有盐酸和氯化钙的混合溶液100g,向混合溶液中逐滴加入20%的Na2CO3溶液,生成沉淀的质量与加入Na2CO3溶液的质量关系如图。若CaCl2在原混合液中的质量分数为22.2%。
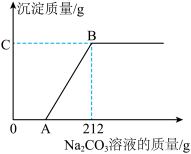
求:(1)A点表示的质量为_______。
(2)反应进行到B点时溶液的溶质质量分数。(请写出计算过程)

求:(1)A点表示的质量为_______。
(2)反应进行到B点时溶液的溶质质量分数。(请写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】化学研究小组利用加热后的废旧铜丝与100g 9.8%的稀硫酸溶液完全反应制备硫酸铜,再对溶液加热、冷却结晶得到硫酸铜晶体,并测定晶体中结晶水的含量。请回答下列问题:
(1)完全反应能制得多少g硫酸铜。
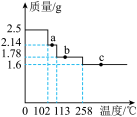
(2)取2.5g硫酸铜晶体加热失水,得到不同温度下固体的质量曲线(又叫热重曲线):
①通过计算确定硫酸铜晶体的化学式_________ 。
②通过计算确定b点固体物质的化学式_________ 。

(1)完全反应能制得多少g硫酸铜。
(2)取2.5g硫酸铜晶体加热失水,得到不同温度下固体的质量曲线(又叫热重曲线):
①通过计算确定硫酸铜晶体的化学式
②通过计算确定b点固体物质的化学式
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】向73克稀盐酸中加入50克溶质质量分数为8%的氢氧化钠溶液,二者恰好完全反应,则此稀盐酸溶液中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】在烧杯中加入2.14 g久置于空气中的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示。请回答下列问题:
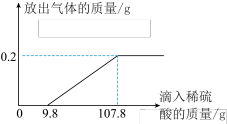
(1)总共产生氢气(H2)_____g;
(2)刚开始滴加稀硫酸没有氢气放出是因为铝箔与空气中的氧气反应生成了_____(填化学式),写出生成物与稀硫酸反应的化学方程式_____。
(3)计算所滴加的稀硫酸中溶质的质量分数(写出计算过程)。

(1)总共产生氢气(H2)_____g;
(2)刚开始滴加稀硫酸没有氢气放出是因为铝箔与空气中的氧气反应生成了_____(填化学式),写出生成物与稀硫酸反应的化学方程式_____。
(3)计算所滴加的稀硫酸中溶质的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】实验室测定一瓶稀硫酸中溶质的质量分数.取10g该待测液,向其中逐滴加入5%的NaOH溶液,加入NaOH溶液的质量与溶液pH的变化关系如图所示。
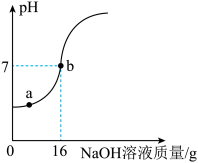
(1)16g5%的NaOH溶液中所含溶质的质量是________ g;
(2)a点对应溶液中的溶质是________ ;
(3)计算待测稀硫酸中溶质的质量分数_________ (写出计算过程及结果)。

(1)16g5%的NaOH溶液中所含溶质的质量是
(2)a点对应溶液中的溶质是
(3)计算待测稀硫酸中溶质的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入100g稀硫酸,恰好完全反应后,测得烧杯内所有物质的总质量为109.8g。
请完成下列分析及计算:
(1)反应中生成气体的质量是_______ g。
(2)计算合金中铜的质量分数?
(3)反应后所得溶液的质量分数?
请完成下列分析及计算:
(1)反应中生成气体的质量是
(2)计算合金中铜的质量分数?
(3)反应后所得溶液的质量分数?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】碳酸钠和碳酸氢钠的固体混合物充分加热至恒重,其质量变化如下图所示。另取相同质量的该混合物溶于水得到106.6 g溶液,向该溶液中加入100 g 7.3% 的稀盐酸,恰好完全反应。(已知:2NaHCO3 Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)
Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)

计算:(1)混合物与盐酸反应生成二氧化碳的质量。
(2)所得溶液中溶质的质量分数。
 Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)
Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)
计算:(1)混合物与盐酸反应生成二氧化碳的质量。
(2)所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】向100g硫酸铜溶液中,不断加入一定溶质质量分数的氯化钡溶液,实验数据如下表:
(1)当滴加氯化钡溶液的质量为100g时,所得溶液中的溶质有CuCl2和_______ 。
(2)选择合理的数据,计算该硫酸铜溶液中溶质的质量分数。
| 氯化钡溶液的质量/g | 20 | 40 | 80 | 100 |
| 生成沉淀的质量/g | 5.825 | 11.65 | 23.3 | 23.3 |
(2)选择合理的数据,计算该硫酸铜溶液中溶质的质量分数。
您最近一年使用:0次



