硫酸亚铁在工农业生产中有重要用途,也有较高的医用价值。工业上用废铁屑和含硫酸的废液来制取硫酸亚铁,变废为宝。现用5.6t铁屑与l00t废液恰好完全反应(已知铁屑只和废液中的硫酸反应),请你计算:
(1)可生成硫酸亚铁的质量
(2)所用废液中硫酸的溶质质量分数
(1)可生成硫酸亚铁的质量
(2)所用废液中硫酸的溶质质量分数
2017·山东德州·中考真题 查看更多[8]
2017年初中毕业升学考试(山东德州卷)化学2018年安徽省淮南市凤台县尚塘中学中考一模化学试题2018年安徽省阜阳市太和县朱庄中学中考一模化学试题河北省石家庄市新乐市2019-2020学年九年级上学期期末化学试题河北省石家庄市行唐县2019-2020学年九年级上学期期末化学试题(已下线)【万唯原创】2018年河南省中考化学面对面卷九年级第五单元(已下线)【万唯原创】2018年安徽省中考化学试题研究卷讲解册九年级中考题型研究专题七2023年甘肃省平凉市庄浪县南湖中学中考一模化学试题
更新时间:2017-09-14 11:21:03
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】某氢氧化钠样品中混有氯化钠,为测定样品中氢氧化钠的质量分数,称取5.0g样品,加水完全溶解后,缓慢加入稀盐酸,同时测定溶液的pH。当pH=7时,恰好用去10%的稀盐酸36.5g。(反应的化学方程式为:NaOH+HCl=NaCl+H2O)试计算:
(1)将100g质量分数为36 %的浓盐酸稀释成10%的稀盐酸,需加水的质量为_____g。
(2)样品中氢氧化钠的质量分数_____。
(1)将100g质量分数为36 %的浓盐酸稀释成10%的稀盐酸,需加水的质量为_____g。
(2)样品中氢氧化钠的质量分数_____。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】工业盐酸中通常含少量 而呈黄色,小亮为测定某工业盐酸中HCl的含量进行如下实验,取某工业盐酸100g,滴加溶质质量分数为20%的NaOH溶液,反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表。请根据表格和图象完成下列问题:
而呈黄色,小亮为测定某工业盐酸中HCl的含量进行如下实验,取某工业盐酸100g,滴加溶质质量分数为20%的NaOH溶液,反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表。请根据表格和图象完成下列问题:
(1)开始没有产生沉淀的原因是______ 。
(2)求该工业盐酸中HCl的质量分数(写出计算过程,下同)。
(3)求表中m的值。
 而呈黄色,小亮为测定某工业盐酸中HCl的含量进行如下实验,取某工业盐酸100g,滴加溶质质量分数为20%的NaOH溶液,反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表。请根据表格和图象完成下列问题:
而呈黄色,小亮为测定某工业盐酸中HCl的含量进行如下实验,取某工业盐酸100g,滴加溶质质量分数为20%的NaOH溶液,反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表。请根据表格和图象完成下列问题:
| 加入NaOH溶液的质量/g | 25 | 50 | 75 | 100 |
| 所得溶液的质量/g | 12 | 5150 | 175 | m |
(1)开始没有产生沉淀的原因是
(2)求该工业盐酸中HCl的质量分数(写出计算过程,下同)。
(3)求表中m的值。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】实验室常用大理石和稀盐酸制取二氧化碳。现取25g大理石样品于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如下图所示。求:

(1)在实验时可将大理石适当粉碎,这样做的目的是_______ 。
(2)该大理石样品中碳酸钙的质量为_______ g,其质量分数为_______ 。
(3)若将生成的气体通入澄清石灰水中,可以观察到的现象是_______ 。
(4)反应生成的CO2的质量为多少?(请写出完整的计算过程)

(1)在实验时可将大理石适当粉碎,这样做的目的是
(2)该大理石样品中碳酸钙的质量为
(3)若将生成的气体通入澄清石灰水中,可以观察到的现象是
(4)反应生成的CO2的质量为多少?(请写出完整的计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】取 样品
样品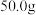 完全溶解于
完全溶解于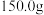 水中,并向其中逐渐加入一定浓度的
水中,并向其中逐渐加入一定浓度的 溶液,实验过程中生成沉淀的质量与加入
溶液,实验过程中生成沉淀的质量与加入 溶液的质量的关系如图所示,求样品
溶液的质量的关系如图所示,求样品 的质量分数。【温馨提示:化学方程式:
的质量分数。【温馨提示:化学方程式: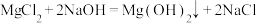 】
】
 样品
样品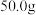 完全溶解于
完全溶解于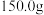 水中,并向其中逐渐加入一定浓度的
水中,并向其中逐渐加入一定浓度的 溶液,实验过程中生成沉淀的质量与加入
溶液,实验过程中生成沉淀的质量与加入 溶液的质量的关系如图所示,求样品
溶液的质量的关系如图所示,求样品 的质量分数。【温馨提示:化学方程式:
的质量分数。【温馨提示:化学方程式: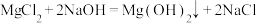 】
】
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】陈红同学为了测定家庭消毒用的过氧化氢溶液的浓度,取了100g溶液,加入2g二氧化锰后充分反应后,剩余溶液质量为100.4g(不考虑水的蒸发),请计算:
(1)生成氧气的质量为 g;
(2)过氧化氢溶液中溶质的质量分数。
(1)生成氧气的质量为 g;
(2)过氧化氢溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】铝合金的生产与销售是潍坊市一条重要的产业链,为测定某种铝铜合金中铝的质量分数,探究小组进行了如下实验:
(1)所用稀硫酸溶质的质量分数为__________。
(2)该铝铜合金中铝的质量分数是多少?_____
| 实验编号 | 铝铜合金的质量(g) | 加入稀硫酸的质量(g) | 生成H2的质量(g) |
| 实验1 | 30 | 392 | 2 |
| 实验2 | 30 | 588 | 3 |
| 实验3 | 30 | 600 | 3 |
(2)该铝铜合金中铝的质量分数是多少?_____
您最近一年使用:0次

 ,充分反应后得46.6g沉淀。
,充分反应后得46.6g沉淀。


