(1)请填写下表有关空白并回答下列问题:
(2)上表中物质属于氧化物的是_________ (填序号,下同);属于碱的是________ ;属于盐的是_________ 。
(3)若要测定氢氧化钾溶液的酸碱度,应选用下列选项中__________ (填字母,下同)。
A.无色酚酞试液 B.紫色石蕊试液 C.pH试纸
(4)槟榔芋皮上含有一种碱性物质——皂角素,沾上它会使皮肤奇痒难忍。选用下列____ 来涂抹止痒。
A.食醋 B.熟石灰 C.纯碱
| 序 号 | ① | ② | ③ | ④ |
| 物 质 | 碳酸 | 水 | 氢氧化钾 | 纯碱 |
| 化学式 | H2O | Na2CO3 |
(3)若要测定氢氧化钾溶液的酸碱度,应选用下列选项中
A.无色酚酞试液 B.紫色石蕊试液 C.pH试纸
(4)槟榔芋皮上含有一种碱性物质——皂角素,沾上它会使皮肤奇痒难忍。选用下列
A.食醋 B.熟石灰 C.纯碱
更新时间:2017-09-19 22:23:22
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】
(1)钢铁的最大的弱点是易生锈,铁生锈的条件是_________ 。铜表面也容易生成绿色的铜锈,铜锈的主要成分是碱式碳酸铜,【化学式为Cu 2(OH)2CO3】,碱式碳酸铜属于_________ (选填“酸”、“碱”、“盐”)。
(2)老师用生锈的铜片、铁粉和稀硫酸进行实验,实验过程如下图所示(部分生成物已略去)。

反应①中产生的无色气体的化学式为_________ ,写出反应②中反应的化学方程式_________ (任写一个即可 )。
(1)钢铁的最大的弱点是易生锈,铁生锈的条件是
(2)老师用生锈的铜片、铁粉和稀硫酸进行实验,实验过程如下图所示(部分生成物已略去)。

反应①中产生的无色气体的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】我国“嫦娥五号”月球探测器成功将月球上的岩石和土壤带回地球。
(1)月球岩石中富含钛铁矿,其主要成分是FeTiOx,其中钛(Ti)元素的化合价为+4,则FeTiOx中x为______ 。
(2)嫦娥五号的登月着陆器使用的是砷化镓太阳能电池,镓(Ga)的原子结构示意图如图,则镓元素的氧化物化学式为______ 。

(3)长征运载火箭使用的燃料为液氢。已知MgH2可与水反应得到氢气和一种碱,其化学方程式为______ 。
(1)月球岩石中富含钛铁矿,其主要成分是FeTiOx,其中钛(Ti)元素的化合价为+4,则FeTiOx中x为
(2)嫦娥五号的登月着陆器使用的是砷化镓太阳能电池,镓(Ga)的原子结构示意图如图,则镓元素的氧化物化学式为

(3)长征运载火箭使用的燃料为液氢。已知MgH2可与水反应得到氢气和一种碱,其化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】用化学用语填空:
(1)三个水分子_____ ;
(2)标出氯化镁中镁元素的化合价________ ;
(3)铝离子_________ ;
(4)两个硫原子_____________ 。
(1)三个水分子
(2)标出氯化镁中镁元素的化合价
(3)铝离子
(4)两个硫原子
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是某矿物质水中商品标签部分内容,阅读后用化学符号回答下列问题。
(1)矿物质水中含有的钠元素__________ 。
(2)久置的水中会溶有一定量的氧气。请写出两个氧分子__________ 。
(3)写出标签中阴离子的符号__________ 。
(4)偏硅酸(H2SiO3)中硅元素的化合价为__________ 。
| 矿物质水中主要成分(mg/L) | |
| 偏硅酸(H2SiO3)≥25 硫酸根≥0.05 ······ | 钙≥0.2 钠≥0.2 钾≥0.2 ····· |
(2)久置的水中会溶有一定量的氧气。请写出两个氧分子
(3)写出标签中阴离子的符号
(4)偏硅酸(H2SiO3)中硅元素的化合价为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
名校
【推荐3】俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于提出了现代元素周期表的雏形。下表为元素周期表的部分元素的相关信息,利用下表回答相关问题
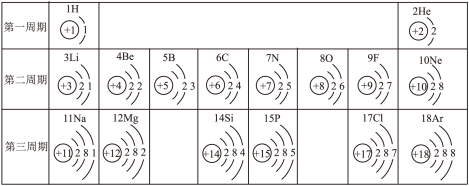
(1)请画出16号元素原子结构示意图______________ 化学反应中该原子比较容易__________
(填“得到”或“失去”)电子变成离子;
(2) 表示的是
表示的是______ (填离子符号);
(3)上表中最活泼的金属元素与地壳中含量最多的元素组成的化合物是__________
(填化学式,任意填写一种);
(4)上表中第二、三周期元素最外层电子数的变化规律是_____________________ 。

(1)请画出16号元素原子结构示意图
(填“得到”或“失去”)电子变成离子;
(2)
 表示的是
表示的是(3)上表中最活泼的金属元素与地壳中含量最多的元素组成的化合物是
(填化学式,任意填写一种);
(4)上表中第二、三周期元素最外层电子数的变化规律是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】生活处处有化学
(1)“沙里淘金”说明黄金在自然界中主要以______ (填:单质、化合物)形式存在。
(2)若装白磷的储罐起火,可以用水冷却罐体、再用沙土围堰填埋灭火。则白磷燃烧的化学方程式为:______ ;其灭火的原理是______ 。
(3)人被昆虫叮咬后皮肤红肿起泡,这是由于昆虫在皮肤内注入了少量甲酸,此时应选择表中所列的_______ (填编号)涂在被咬的皮肤上。
(1)“沙里淘金”说明黄金在自然界中主要以
(2)若装白磷的储罐起火,可以用水冷却罐体、再用沙土围堰填埋灭火。则白磷燃烧的化学方程式为:
(3)人被昆虫叮咬后皮肤红肿起泡,这是由于昆虫在皮肤内注入了少量甲酸,此时应选择表中所列的
| 物质 | A | B | C | D |
| 肥皂水 | 食醋 | 牙膏 | 食盐水 | |
| pH | 10 | 3 | 9 | 7 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】化学与生活密切相关。回答下列问题:
(1)“杂交水稻之父”袁隆平“一稻济天下”,在不断培育高产杂交水稻的同时,还成功培育出了适宜在盐碱地上种植的“海水稻”。
①“杂交水稻”富含淀粉,淀粉属于六大基本营养素中的______ 。
②“海水稻”富含硒,硒是人体必需的______ (选填“微量”“常量”)元素。
(2)在治疗胃酸过多症的药物成分中,含有的物质不可能是______(填字母)。
(3)自来水硬度较大不宜直接饮用。为了降低水的硬度,生活中常采用的方法是______ 。
(4)扑灭森林火灾时,通常将大火蔓延路线前的一片树木砍掉,其灭火原理是______ 。
(1)“杂交水稻之父”袁隆平“一稻济天下”,在不断培育高产杂交水稻的同时,还成功培育出了适宜在盐碱地上种植的“海水稻”。
①“杂交水稻”富含淀粉,淀粉属于六大基本营养素中的
②“海水稻”富含硒,硒是人体必需的
(2)在治疗胃酸过多症的药物成分中,含有的物质不可能是______(填字母)。
| A.碳酸氢钠 | B.氢氧化铝 | C.氢氧化钠 | D.碳酸钙 |
(4)扑灭森林火灾时,通常将大火蔓延路线前的一片树木砍掉,其灭火原理是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。
(1)下列含碳元素的物质中,属于有机物的是______(填字母序号)。
(2)近期,浙江大学实验室里诞生了世界上最轻的材料﹣﹣“碳海绵”。(如图所示),由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是:______(填字母序号)。

(3)如图所示,二氧化碳是很重要的化工原料,科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环。

①步骤1的化学方程式为______ 。
②为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量______ 溶液,若观察到试管内______ ,则分解不完全。
③上述设想的优点有______ (填字母序号)。
a、原料易得且可循环利用 b、充分利用太阳能 c、可全地域全天候使用
④CO2是宝贵的碳氧资源。CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为______ ,若要检验1%甲酸水溶液是否显酸性,能选用的有______ (填字母序号)。
a、无色酚酞溶液 b、紫色石蕊溶液 c、pH试纸
(4)如图,在A瓶中盛满CO2气体,将装有96℃以上但未沸腾热水的B瓶,放入装有相同热水的烧杯中,进行如下实验:

①先用注射器抽取20mL的水,注入A瓶中,充分振荡,其化学方程式为:______ ,但未见B瓶中发生现象。
②再用另一只注射器抽取20mL的浓NaOH,注入A瓶中,充分振荡,其化学方程式为:______ ,观察到的现象为______ ,产生此现象的原因是______ 。
(1)下列含碳元素的物质中,属于有机物的是______(填字母序号)。
| A.碳酸钙 | B.乙醇(C2H5OH) | C.二氧化碳 | D.纤维素 |
(2)近期,浙江大学实验室里诞生了世界上最轻的材料﹣﹣“碳海绵”。(如图所示),由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是:______(填字母序号)。

| A.有吸附性 | B.重复利用 | C.处理海上石油泄漏 |
(3)如图所示,二氧化碳是很重要的化工原料,科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环。

①步骤1的化学方程式为
②为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量
③上述设想的优点有
a、原料易得且可循环利用 b、充分利用太阳能 c、可全地域全天候使用
④CO2是宝贵的碳氧资源。CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为
a、无色酚酞溶液 b、紫色石蕊溶液 c、pH试纸
(4)如图,在A瓶中盛满CO2气体,将装有96℃以上但未沸腾热水的B瓶,放入装有相同热水的烧杯中,进行如下实验:

①先用注射器抽取20mL的水,注入A瓶中,充分振荡,其化学方程式为:
②再用另一只注射器抽取20mL的浓NaOH,注入A瓶中,充分振荡,其化学方程式为:
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
真题
【推荐2】工业上用电解饱和食盐水的方法制得的烧碱中常含有一定量的氯化钠。为测定某烧碱样品的纯度,同学们设计了如下方案。
方案一:称取mg烧碱样品 测定消耗稀盐酸的质量。
测定消耗稀盐酸的质量。
方案二:称取mg烧碱样品 测定生成沉淀的质量。
测定生成沉淀的质量。
请回答:
(1)方案一中发生反应的化学方程式为______ 。
(2)方案一中为减少误差,最好选择下列方法中的______ 。(填字母)来判断反应恰好完全进行。
A向样品溶液中滴加2~3滴无色酚酞溶液,根据溶液颜色变化判断.
B测定过程中边滴加稀盐酸边用pH试纸频繁测定混合液的pH
C向样品溶液中滴加2~3滴紫色石蕊溶液,根据颜色变化判断。
(3)小李同学认为判断方案二中,氯化铁FeCl3溶液过量的化学方法是______ 。
(4)小李同学可将方案二中的FeCl3溶液换成稀硝酸和_______ (填化学式)溶液也能达到实验的目的。
方案一:称取mg烧碱样品
 测定消耗稀盐酸的质量。
测定消耗稀盐酸的质量。方案二:称取mg烧碱样品
 测定生成沉淀的质量。
测定生成沉淀的质量。请回答:
(1)方案一中发生反应的化学方程式为
(2)方案一中为减少误差,最好选择下列方法中的
A向样品溶液中滴加2~3滴无色酚酞溶液,根据溶液颜色变化判断.
B测定过程中边滴加稀盐酸边用pH试纸频繁测定混合液的pH
C向样品溶液中滴加2~3滴紫色石蕊溶液,根据颜色变化判断。
(3)小李同学认为判断方案二中,氯化铁FeCl3溶液过量的化学方法是
(4)小李同学可将方案二中的FeCl3溶液换成稀硝酸和
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某废酸液主要含H2SO4和FeSO4,研究人员利用CaCO3消耗部分酸,再加入廉价的电石渣(主要成分为CaO),通过一系列操作可得到磁性铁,成本较低且有利于保护环境。工艺流程如图:

(1)该废酸液的pH______ 7(填“<”或“>”)。操作I的名称为_________ 。
(2)电石渣转化为石灰乳的过程会______ (填“吸收”或“放出”)热量。
(3)“沉铁”过程中,溶液中的FeSO4和石灰乳中的Ca(OH)2发生复分解反应,生成的产物是_______ 和________ (填化学式)。
(4)磁性铁是铁的一种氧化物,且为磁铁矿的主要成分,其化学式为___________ 。工业上常用磁铁矿炼铁的原理,写出其化学方程式__________ 。
(5)研究发现,“沉铁”后,溶液的pH对磁性铁产率的影响如下表。欲获得高的产率,最适宜的pH为_________ , pH较低时产率较低的主要原因是_________ 。

(1)该废酸液的pH
(2)电石渣转化为石灰乳的过程会
(3)“沉铁”过程中,溶液中的FeSO4和石灰乳中的Ca(OH)2发生复分解反应,生成的产物是
(4)磁性铁是铁的一种氧化物,且为磁铁矿的主要成分,其化学式为
(5)研究发现,“沉铁”后,溶液的pH对磁性铁产率的影响如下表。欲获得高的产率,最适宜的pH为
| 溶液的pH | 6.0 | 6.5 | 7.0 | 7.5 | 8.0 | 9.0 |
| 产物颜色 | 黄褐色 | 黄褐色 | 较黑 | 很黑 | 很黑 | 灰黑色 |
| 产率(%) | 43.9 | 50.6 | 86.2 | 93.0 | 92.3 | 91.6 |
您最近一年使用:0次




