如图是古代铜质辅币——铜钱。黄铜在明清时期就用于铸造铜钱了,小明对铜钱(主要成分为铜和锌)中铜的质量分数产生了好奇,他称取10g铜钱样品放入烧杯中,然后往烧杯中加入稀硫酸93.5g,恰好完全反应,反应后称得烧杯内物质共103.3g。试计算:

(1)反应产生氢气多少g;
(2)该铜钱样品中铜的质量分数。

(1)反应产生氢气多少g;
(2)该铜钱样品中铜的质量分数。
更新时间:2017/11/01 21:41:22
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】现有4.6g 的M(相对分子质量为46)在氧气中充分燃烧,生成了4.4g CO2、2.8g CO和5.4 gH2O,消耗氧气的质量为______ g,M的化学式为______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】市场出售家庭食用碱(主要成分为碳酸钠),产品中碳酸钠的含量达到85%以上才算合格,小敏从家中取12g食用碱样品放入烧杯(烧杯质量为50g)中,加入100g稀盐酸,使其恰好完全反应。经测定,反应后溶液连同烧杯其质量为157.6g(产生的气体全部逸出)。试计算:
(1)反应生成二氧化碳的质量为_____ g。
(2)该产品是否合格?_____ (写出计算过程)。
(1)反应生成二氧化碳的质量为
(2)该产品是否合格?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某化学兴趣小组为了测定当地的石灰石(主要成分是CaCO3)的质量分数,他们做了如下实验:取24克样品放入烧杯中,向其中逐渐加入100克一定质量分数的稀盐酸(杂质不溶于水也不与酸反应),所用盐酸的质量分数与剩余固体的质量关系如图所示,请根据图中的数据进行计算:
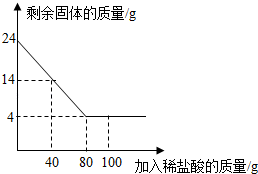
(1)石灰石样品中CaCO3的质量为_____ 克。。
(2)求所得溶液的溶质质量分数_____ 。(请根据化学方程式写出完整的计算步骤,结果保留一位小数)

(1)石灰石样品中CaCO3的质量为
(2)求所得溶液的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】写出碳酸钙与盐酸反应的化学方程式,并计算在实验室中制取8.8g二氧化碳,需要碳酸钙的质量至少是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】已知金属钠能与水发生如下反应:2Na+2H2O=2NaOH+H2↑,若把4.6 g金属钠投有足量水的烧杯中(如图),充分反应后烧杯中剩余溶液的质量是40 g,请计算:
(1)生成NaOH的质量。
(2)反应后所得NaOH溶液的溶质质量分数。

(1)生成NaOH的质量。
(2)反应后所得NaOH溶液的溶质质量分数。
您最近一年使用:0次

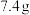 ,先加热完全氧化后,再加入
,先加热完全氧化后,再加入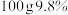 的稀硫酸恰好完全反应,求固体混合物中铜元素的质量分数。(计算结果精确到0.1%)
的稀硫酸恰好完全反应,求固体混合物中铜元素的质量分数。(计算结果精确到0.1%)


