小新用20 g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。操作过程如下。请计算:
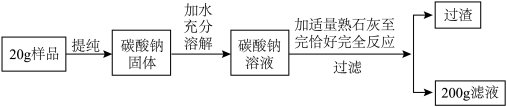
(1)20 g样品中碳酸钠的质量为多少g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)

(1)20 g样品中碳酸钠的质量为多少g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
2017九年级下·全国·专题练习 查看更多[4]
人教版2018届九年级下册化学同步练习:专题复习(五)计算应用题(已下线)题型 计算应用题·课后特训6(已下线)第十一单元 盐 化肥 单元测试——2020-2021学年人教版九年级化学下册同步精品课堂黑龙江省大庆市让胡路区庆新中学2020-2021学年九年级下学期第一次月考(一模)化学试题
更新时间:2017-11-09 12:49:14
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】质量相等的两份Zn粉,分别与质量相同、质量分数不同的稀盐酸反应。
(1)配制盐酸时有白雾,说明盐酸具有 性。
(2)两种稀盐酸反应生成氢气的图象如图所示,两种稀盐酸的浓度比较:Ⅰ% Ⅱ%(填“>”“<”“=”)。
氢气的体积所对应的质量如下表:
(4)完全反应时,加入稀盐酸Ⅱ的质量为100g,求稀盐酸Ⅱ中溶质的质量分数。
(1)配制盐酸时有白雾,说明盐酸具有 性。
(2)两种稀盐酸反应生成氢气的图象如图所示,两种稀盐酸的浓度比较:Ⅰ% Ⅱ%(填“>”“<”“=”)。
氢气的体积所对应的质量如下表:
| H2(V/L) | 1.11 | 1.67 | 2.22 | 2.78 |
| H2(m/g) | 0.10 | 0.15 | 0.20 | 0.25 |
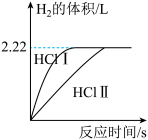
(4)完全反应时,加入稀盐酸Ⅱ的质量为100g,求稀盐酸Ⅱ中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】某化学兴趣小组为测定大理石中碳酸钙的含量,进行如图 1 所示实验:将过量的稀盐酸加入到20 g大理石中(其他成分不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量 C 瓶烧碱溶液增加的质量,结果如下表所示:
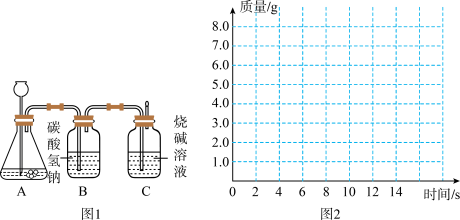
(1)上表中,第 10 分钟时,x=__________。
(2)计算大理石样品中碳酸钙的质量分数。_________(要写计算过程)
(3)请在如图 2 的坐标纸上,以时间为横坐标,以产生 CO2 气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线(假设第 8 分钟是恰好反应结束)______________。
(4)B 中所装药品为碳酸氢钠溶液,作用是吸收挥发出的 HCl 气体,该装置使测量结果________(填“偏 大”“偏小”或“没有影响”)。

| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| C 增加质量/g | 0 | 3.0 | 5.0 | 6.0 | 6.6 | x | 6.6 |
(2)计算大理石样品中碳酸钙的质量分数。_________(要写计算过程)
(3)请在如图 2 的坐标纸上,以时间为横坐标,以产生 CO2 气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线(假设第 8 分钟是恰好反应结束)______________。
(4)B 中所装药品为碳酸氢钠溶液,作用是吸收挥发出的 HCl 气体,该装置使测量结果________(填“偏 大”“偏小”或“没有影响”)。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
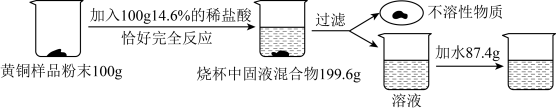
【推荐1】某同学为了测定一种补钙保健食品中CaCO3的质量分数,(其包装说明如下图所示)进行了如下实验:将100片该食品研碎后放入一烧杯中,向其中慢慢滴加稀盐酸,直到不再产生气泡时,共消耗稀盐酸200g,(该保健食品中其它成分不与盐酸反应)并测得烧杯内剩余物质的总质量为232.4g.请你根据以上数据计算:

(1)所用盐酸的溶质质量分数_____
(2)该保健食品中CaCO3的质量分数为____?

(1)所用盐酸的溶质质量分数_____
(2)该保健食品中CaCO3的质量分数为____?
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】南岸区文峰水泥厂新进了一批石灰石原料,为了测定石灰石在碳酸钙的质量分数,该厂化验室取一定量的石灰石样品与100g过量的稀盐酸在烧杯中反应(样品中杂质不溶于水,也不与稀盐酸反应),有关实验数据如下表:
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为___________g;
(2)该石灰石中碳酸钙的质量分数为___________;
(3)将烧杯中的混合物过滤,向滤液中加入过量的硝酸银溶液,充分反应生成57.4g白色沉淀。假定实验过程中无损耗,则稀盐酸中溶质的质量分数为多少?(结果保留一位小数)
| 反应前 | 反应后 | |
| 烧杯和稀盐酸的总重量 | 石灰石样品的质量 | 烧杯和其中混合物的总质量 |
| 200.0g | 12.5g | 208.1g |
(2)该石灰石中碳酸钙的质量分数为___________;
(3)将烧杯中的混合物过滤,向滤液中加入过量的硝酸银溶液,充分反应生成57.4g白色沉淀。假定实验过程中无损耗,则稀盐酸中溶质的质量分数为多少?(结果保留一位小数)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】取碳酸钠和氯化钠的固体混合物13.6g,与质量为73g的稀盐酸恰好完全反应,产生二氧化碳气体的质量为4.4g。计算:
(1)固体混合物中碳酸钠的质量_____。
(2)该稀盐酸中溶质的质量分数_____。
(3)反应所得的溶液中溶质的质量分数_____(要计算过程,最后结果保留一位小数)。
(1)固体混合物中碳酸钠的质量_____。
(2)该稀盐酸中溶质的质量分数_____。
(3)反应所得的溶液中溶质的质量分数_____(要计算过程,最后结果保留一位小数)。
您最近一年使用:0次