人类的生产生活离不开金属.
(1)金属钛(Ti)的合金具有密度小,熔点高、可塑性好,抗腐蚀性强等性能,钛合金与人体有很好的“相容性”。工业上冶炼金属钛的过程是以钛矿石(主要成分为钛酸亚铁,化学式为FeTiO3)、焦炭、氯气为原料,在高温条件下制取TiCl4,其反应的化学方程式为:2FeTiO3+6C+7Cl2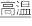 2TiCl4+2X+6CO,然后用镁与TiCl4在高温条件下反应生成金属钛和氯化镁。请根据以上信息回答下列问题:
2TiCl4+2X+6CO,然后用镁与TiCl4在高温条件下反应生成金属钛和氯化镁。请根据以上信息回答下列问题:
①FeTiO3中钛元素的化合价为_____________ 。
②制取TiCl4的反应中,X的化学式为________________ 。
③镁与TiCl4反应的基本类型为________________ 。
④下列关于钛合金用途的说法不正确的是________________ 。
A.做保险丝 B.用于航空、航天工业
C.制人造骨 D.用于船舶、核潜艇的制造
(2)某小组用图1所示装置对铁生锈的条件进行探究,一段时间后发现A中铁钉表面生锈,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是______________ 。

(3)将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合后加热到约800℃,得到一种锌和铜的合金—黄铜,外观似黄金但质地坚硬。(提示:ZnCO3受热会分解,生成两种氧化物)。
①写出赤铜和木炭粉反应的化学方程式____________________________________ 。
②有不法商人用黄铜冒充黄金,制假销售,下列鉴别真假黄金的方法不正确的是________ 。
A.灼烧 B.看外观 C.滴加稀盐酸 D.滴加硫酸铝溶液
(1)金属钛(Ti)的合金具有密度小,熔点高、可塑性好,抗腐蚀性强等性能,钛合金与人体有很好的“相容性”。工业上冶炼金属钛的过程是以钛矿石(主要成分为钛酸亚铁,化学式为FeTiO3)、焦炭、氯气为原料,在高温条件下制取TiCl4,其反应的化学方程式为:2FeTiO3+6C+7Cl2
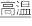 2TiCl4+2X+6CO,然后用镁与TiCl4在高温条件下反应生成金属钛和氯化镁。请根据以上信息回答下列问题:
2TiCl4+2X+6CO,然后用镁与TiCl4在高温条件下反应生成金属钛和氯化镁。请根据以上信息回答下列问题:①FeTiO3中钛元素的化合价为
②制取TiCl4的反应中,X的化学式为
③镁与TiCl4反应的基本类型为
④下列关于钛合金用途的说法不正确的是
A.做保险丝 B.用于航空、航天工业
C.制人造骨 D.用于船舶、核潜艇的制造
(2)某小组用图1所示装置对铁生锈的条件进行探究,一段时间后发现A中铁钉表面生锈,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是

(3)将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合后加热到约800℃,得到一种锌和铜的合金—黄铜,外观似黄金但质地坚硬。(提示:ZnCO3受热会分解,生成两种氧化物)。
①写出赤铜和木炭粉反应的化学方程式
②有不法商人用黄铜冒充黄金,制假销售,下列鉴别真假黄金的方法不正确的是
A.灼烧 B.看外观 C.滴加稀盐酸 D.滴加硫酸铝溶液
更新时间:2018-01-05 09:33:14
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
【推荐1】A~H是初中化学常见物质,它们之间的转化关系如图所示(部分产物已略去)。已知B是目前世界年产量最高的金属,C是气体,H的水溶液呈蓝色,G、H的溶液中的阴离子相同。

(1)列举D物质的一种用途___________ 。
(2)反应Ⅱ的化学方程式为___________ 。
(3)写出一个符合条件的反应Ⅰ的化学方程式___________ 。
(4)如图所示的转化关系中,涉及到的基本反应类型是___________ 。

(1)列举D物质的一种用途
(2)反应Ⅱ的化学方程式为
(3)写出一个符合条件的反应Ⅰ的化学方程式
(4)如图所示的转化关系中,涉及到的基本反应类型是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】如图是初中化学中几种常见物质间的转化关系已知每种物质中都含有相对原子质量为40的一种元素,且A、D均含有两种元素。转化①至⑥的化学反应中,不包含的基本反应类型是______ ;C→D的化学方程式为______ ;物质B在生产、生活中的一种用途是______ 。


您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐3】A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系。请回答:

⑴写出物质的化学式:A________ ;B_________ ,X溶液中的溶质是__________ (填化学式)。
⑵写出反应①的化学方程式:_________ ,反应④的实验现象_________ 。
⑶C和D的化学性质不同,其原因是_________ 。
⑷如图转化中产生无色气体G的原因是________ (用化学方程式表示)。
⑸A与G反应的基本类型是__________ 。

⑴写出物质的化学式:A
⑵写出反应①的化学方程式:
⑶C和D的化学性质不同,其原因是
⑷如图转化中产生无色气体G的原因是
⑸A与G反应的基本类型是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】航天员王亚平在“天宫课堂”中介绍了空间站中的生活。在轨演示了水球变气球等一系列炫酷又好玩的实验。
I.“天宫”中水和氧气的最大化利用是保障生活的重要措施。下图是空间站常用资源再利用模拟图。

(1)“尿处理子系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的_______ 不同进行分离的。
(2)“水电解系统"中产生氧气的反应的化学方程式为_______ 。
(3)在水化系统中,用臭氧(O3)消毒,臭氧转化为氧气的化学方程式为_______ 。
(4)“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式为_______ 。生成的CH4如果量比较大,在空间站可以用于_______ 。
Ⅱ.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3_______ (补全化学方程式)。如果在空间站失重状态下收集制得的氧气。可以选用下列装置中_______ (填序号)。

I.“天宫”中水和氧气的最大化利用是保障生活的重要措施。下图是空间站常用资源再利用模拟图。

(1)“尿处理子系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的
(2)“水电解系统"中产生氧气的反应的化学方程式为
(3)在水化系统中,用臭氧(O3)消毒,臭氧转化为氧气的化学方程式为
(4)“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式为
Ⅱ.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐2】硫酸锰可用于饲料营养强化剂和媒染剂,其生产原材料软锰矿(MnO2)、菱锰矿(MnCO3)中常混有硫酸亚铁和硫酸镁等杂质。其生产工艺如图1:(提示:完全沉淀离子的pH值:Fe3+为3.5,Mn2+为10.8,Mg2+为11.6)

(1)酸浸时,需将原材料固体研碎,其目的是______ 。
(2)碳酸锰与硫酸发生复分解反应,该反应的化学方程式为:______ ;反应器中,还发生反应MnO2+2H2SO4+2FeSO4=MnSO4+Fe2(SO4)3+2X,则X是______ (用化学式表示)。
(3)反应器所得溶液含过量的硫酸,所以酸度小于3.5.生产时,需往沉淀池加入适量的MnCO3,其目的是______ 。
(4)过滤所得混合液中的成分是硫酸锰和硫酸镁,它们的溶解度曲线如图2所示。操作I是指在______ (填“60”或“100”)℃时,蒸发水分、浓缩结晶,得到较多的MnSO4•H2O,然后要趁热过滤。趁热过滤的目的是______ 。


(1)酸浸时,需将原材料固体研碎,其目的是
(2)碳酸锰与硫酸发生复分解反应,该反应的化学方程式为:
(3)反应器所得溶液含过量的硫酸,所以酸度小于3.5.生产时,需往沉淀池加入适量的MnCO3,其目的是
(4)过滤所得混合液中的成分是硫酸锰和硫酸镁,它们的溶解度曲线如图2所示。操作I是指在

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】铁红(Fe2O3)常用于油漆、油墨、橡胶等工业中,现以FeSO4·7H2O为原料制备铁红(Fe2O3)的一种方法如下:
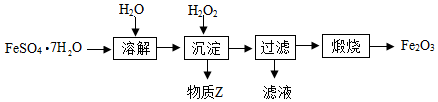
已知沉淀时的主要反应为: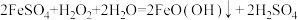
(1)FeO(OH)中铁元素的化合价为______ 。
(2)沉淀时需调节溶液的初始pH约为4,过程中需不断加入物质Z调节溶液的pH,保持溶液的pH为3.0-4.5,Z应该具备的性质是______ (填字母)。
A.不与FeO(OH)反应 B.能与酸反应 C.能与碱反应
(3)为保证产品纯度,需对沉淀进行洗涤。检验沉淀是否洗涤干净的方法:用适量蒸馏水淋洗过滤器中的沉淀2-3次,取少量最后一次淋洗下来的液体,______ (写出操作和现象),则沉淀已洗涤干净。
(4)在煅烧过程中需要不断加热,以达到高温条件,说明该反应可能属于______ 反应(选填“放热”或“吸热”)。为了加快煅烧的反应速率,可以将固体______ (填操作名称)。
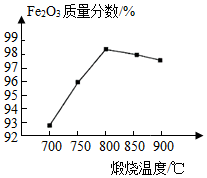
(5)如图为其他条件相同时,不同煅烧温度对产品中Fe2O3质量分数的影响。当煅烧温度达______ ℃时,Fe2O3的质量分数最高。若继续升高温度,所得产品发黑且铁元素质量分数升高,同时有无色气体产生,其可能原因是______ (用化学反应方程式表示)。

已知沉淀时的主要反应为:
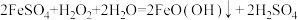
(1)FeO(OH)中铁元素的化合价为
(2)沉淀时需调节溶液的初始pH约为4,过程中需不断加入物质Z调节溶液的pH,保持溶液的pH为3.0-4.5,Z应该具备的性质是
A.不与FeO(OH)反应 B.能与酸反应 C.能与碱反应
(3)为保证产品纯度,需对沉淀进行洗涤。检验沉淀是否洗涤干净的方法:用适量蒸馏水淋洗过滤器中的沉淀2-3次,取少量最后一次淋洗下来的液体,
(4)在煅烧过程中需要不断加热,以达到高温条件,说明该反应可能属于
(5)如图为其他条件相同时,不同煅烧温度对产品中Fe2O3质量分数的影响。当煅烧温度达

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】工业上用闪锌矿(主要成分是ZnS、FeS)冶炼锌,主要流程如下:

(1)焙烧炉中,ZnS转化为ZnO。补全该反应的化学方程式。
___________ ZnS+___________ 
___________ ZnO+___________ SO2
(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液。反应过程中需不断搅拌,其目的是___________ 。
(3)酸浸渣的主要成分是铁酸锌(ZnFe2O4,其中Fe为+3价)。底吹炉中,主要发生如下反应:
①3ZnFe2O4+C 2Fe3O4+3ZnO+CO↑
2Fe3O4+3ZnO+CO↑
②ZnFe2O4+CO 2FeO+ZnO+CO2
2FeO+ZnO+CO2
③ZnO+CO Zn(蒸气)+CO2
Zn(蒸气)+CO2
反应①~③中,化合价发生改变的元素有___________ 。
(4)最终可以获得锌的设备有___________ 。

(1)焙烧炉中,ZnS转化为ZnO。补全该反应的化学方程式。

(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液。反应过程中需不断搅拌,其目的是
(3)酸浸渣的主要成分是铁酸锌(ZnFe2O4,其中Fe为+3价)。底吹炉中,主要发生如下反应:
①3ZnFe2O4+C
 2Fe3O4+3ZnO+CO↑
2Fe3O4+3ZnO+CO↑②ZnFe2O4+CO
 2FeO+ZnO+CO2
2FeO+ZnO+CO2③ZnO+CO
 Zn(蒸气)+CO2
Zn(蒸气)+CO2反应①~③中,化合价发生改变的元素有
(4)最终可以获得锌的设备有
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】氯碱工业和钢铁工业都是最基本的化学工业之一。
(1)氯碱工业指的是工业上通过电解饱和食盐水可获得氢气、氯气(Cl2)和烧碱(NaOH)。
①写出该反应的化学方程式_____ 。
②“84消毒液”就是氯碱工业产品之一,可用于疫情防治,主要成分是次氯酸钠(NaClO),制备次氯酸钠的化学方程式为: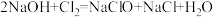 ,其中NaClO中,钠元素和氧元素的质量比是
,其中NaClO中,钠元素和氧元素的质量比是_____ (填写最简整数比)。
③运输液态氯气过程中,如果发生泄露,消防处理人员为尽快吸收液氯(Cl2),减少其对环境的污染,最好选用下列各项中的_____ (填序号)作吸收剂。
A食盐水 B氢氧化钠溶液 C水 D稀硫酸
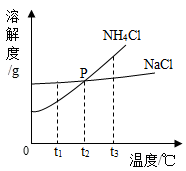
④我国著名化学家侯德榜在世界氯碱工业发展中做出过重要贡献,他在氨碱法的基础上创立的“侯氏制碱法”,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl两种物质的溶解度曲线如图所示。若把t1℃时NH4Cl和NaCl的饱和溶液,均升温到t3℃,则t3℃时NH4Cl溶液的溶质质量分数_____ NaCl溶液的溶质质量分数(填“大于”、“小于”、“等于”之一)。t2℃时,NH4Cl的溶解度__________________ NaCl的溶解度(填写“大于”“等于”“小于”之一)。
(2)早在春秋战国时期,我国就开始生产和使用铁器。
①以赤铁矿(主要成分Fe2O3)为原料炼铁的主要化学方程式为: ,该化学反应属于
,该化学反应属于_____ 反应(填“分解”“化合”“置换”“复分解”“氧化还原”之一)。
②工人师傅切割铁板时,用硫酸铜溶液在铁板上画线可留下红色的印迹。其反应的化学方程式为_____ 。
③利用新技术能将不锈钢加工成柔软的金属丝,用它和棉纤维一起编织成性能优良的劳保防护服,这是利用了不锈钢的_____ (填序号)。
A耐腐蚀性 B延展性 C导热性 D导电性
④金属钛具有硬度大、密度小、熔点高、抗腐蚀性远优于不锈钢等优良性能,被誉为“未来金属”。地球表面富含钛铁矿石,钛铁矿石的主要成分是FeTiO3。已知FeTiO3中铁的化合价为+2价,则钛的化合价为_____ 。铁比钛易生锈,请写出防止铁生锈的一种方法_____ 。
(1)氯碱工业指的是工业上通过电解饱和食盐水可获得氢气、氯气(Cl2)和烧碱(NaOH)。
①写出该反应的化学方程式
②“84消毒液”就是氯碱工业产品之一,可用于疫情防治,主要成分是次氯酸钠(NaClO),制备次氯酸钠的化学方程式为:
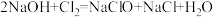 ,其中NaClO中,钠元素和氧元素的质量比是
,其中NaClO中,钠元素和氧元素的质量比是③运输液态氯气过程中,如果发生泄露,消防处理人员为尽快吸收液氯(Cl2),减少其对环境的污染,最好选用下列各项中的
A食盐水 B氢氧化钠溶液 C水 D稀硫酸
④我国著名化学家侯德榜在世界氯碱工业发展中做出过重要贡献,他在氨碱法的基础上创立的“侯氏制碱法”,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl两种物质的溶解度曲线如图所示。若把t1℃时NH4Cl和NaCl的饱和溶液,均升温到t3℃,则t3℃时NH4Cl溶液的溶质质量分数

(2)早在春秋战国时期,我国就开始生产和使用铁器。
①以赤铁矿(主要成分Fe2O3)为原料炼铁的主要化学方程式为:
 ,该化学反应属于
,该化学反应属于②工人师傅切割铁板时,用硫酸铜溶液在铁板上画线可留下红色的印迹。其反应的化学方程式为
③利用新技术能将不锈钢加工成柔软的金属丝,用它和棉纤维一起编织成性能优良的劳保防护服,这是利用了不锈钢的
A耐腐蚀性 B延展性 C导热性 D导电性
④金属钛具有硬度大、密度小、熔点高、抗腐蚀性远优于不锈钢等优良性能,被誉为“未来金属”。地球表面富含钛铁矿石,钛铁矿石的主要成分是FeTiO3。已知FeTiO3中铁的化合价为+2价,则钛的化合价为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】金属与生活密切相关.阅读下列材料,回答问题.
材料一:合金是人类应用最早的金属材料.如青铜、黄铜(铜、锌合金,外观与黄金极其相似).合金比组成它的纯金属有更多优良性能,如抗腐蚀性好、硬度大等.
材料二:锂是银白色固体、质软、自然界密度最小的金属,跟水反应生成氢气和氢氧化锂.在电池、航空航天等领域有广泛的用途.
材料三:锂的原子结构示意图及他与钠在周期表中的信息如图所示.

(1)用黄铜片在纯铜片上刻画_____ (填“会”或“不会”)留下痕迹.一块由黄铜冒充的黄金,检验其真伪可用稀盐酸,发生反应的化学方程式为________________ .
(2)金属锂的物理性质有_____ ;金属锂与钠有相似的化学性质,其原因是_____ .
(3)将一定量的铜和锌同时投入硝酸银溶液,充分反应后过滤,得到固体和蓝色滤液.由此,能否判断金属活动性:Zn>Cu>Ag,说明理由_________
材料一:合金是人类应用最早的金属材料.如青铜、黄铜(铜、锌合金,外观与黄金极其相似).合金比组成它的纯金属有更多优良性能,如抗腐蚀性好、硬度大等.
材料二:锂是银白色固体、质软、自然界密度最小的金属,跟水反应生成氢气和氢氧化锂.在电池、航空航天等领域有广泛的用途.
材料三:锂的原子结构示意图及他与钠在周期表中的信息如图所示.

(1)用黄铜片在纯铜片上刻画
(2)金属锂的物理性质有
(3)将一定量的铜和锌同时投入硝酸银溶液,充分反应后过滤,得到固体和蓝色滤液.由此,能否判断金属活动性:Zn>Cu>Ag,说明理由
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】(1)合金的使用推动了社会的发展,目前用的1元硬币为钢芯镀镍合金,具有耐磨性好,______ 等优点。
(2)4g铁和镁的混合粉末与100g 9.8%的稀硫酸恰好反应,将所得溶液蒸干,可得到硫酸亚铁和硫酸镁的质量为______ g。
(2)4g铁和镁的混合粉末与100g 9.8%的稀硫酸恰好反应,将所得溶液蒸干,可得到硫酸亚铁和硫酸镁的质量为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】人类社会发展离不开金属材料,铝合金是工业中应用最广泛的金属材料之一。
(1)硬铝是一种铝合金,纯铝的熔点_______ (选填“高”或“低”)于硬铝。
(2)硬铝中主要含铝、镁、铜。将适量硬铝(已用砂纸打磨处理)放入足量稀硫酸(不考虑杂质与硫酸反应)中,反应的化学方程式有_______ 。
(3)将足量硬铝粉末放入硝酸银溶液中,充分反应后,溶液出现蓝色,写出此时溶液中所含的阳离子:_________ 。
(4)利用下图的实验方案从含有氯化亚铁、氯化铜的废液中回收金属铜和氯化亚铁晶体。

①操作Ⅱ中加入过量的试剂B的目的是___________ 。
②操作Ⅲ除去的物质是________ (填化学式)。
(5)Mg的活动性大于Al,请设计实验方案验证_____________________ (写出具体的操作和现象)。
(6)铝硅合金(含Al、Cu、Si)具有铸造性能好等优点。为测定某铝硅合金中铝的质量分数,某同学将5.6克该合金放入足量的硫酸铜溶液中,充分反应后,过滤出固体物质,干燥后称量为12.5g。则该硬铝样品中铝的质量分数为______ (结果保留一位小数)。
(1)硬铝是一种铝合金,纯铝的熔点
(2)硬铝中主要含铝、镁、铜。将适量硬铝(已用砂纸打磨处理)放入足量稀硫酸(不考虑杂质与硫酸反应)中,反应的化学方程式有
(3)将足量硬铝粉末放入硝酸银溶液中,充分反应后,溶液出现蓝色,写出此时溶液中所含的阳离子:
(4)利用下图的实验方案从含有氯化亚铁、氯化铜的废液中回收金属铜和氯化亚铁晶体。

①操作Ⅱ中加入过量的试剂B的目的是
②操作Ⅲ除去的物质是
(5)Mg的活动性大于Al,请设计实验方案验证
(6)铝硅合金(含Al、Cu、Si)具有铸造性能好等优点。为测定某铝硅合金中铝的质量分数,某同学将5.6克该合金放入足量的硫酸铜溶液中,充分反应后,过滤出固体物质,干燥后称量为12.5g。则该硬铝样品中铝的质量分数为
您最近一年使用:0次



