为区别NaOH和Na2CO3两种无色溶液,某同学设计以下两种实验方案:
方案1:分别取少许两种溶液,各滴入几滴无色酚酞试液,根据酚酞试液是否变红色判断各是哪种溶液?
方案2:分别取少许两种溶液,各加入少量澄清石灰水,根据是否有白色沉淀生成判断各是哪种溶液?
请回答:
(1)该同学设计的两个方案有一个是正确的,该方案是_____ ;理由是(用化学方程式表示):_____ ,另一个方案是不正确的,原因是_____ 。
(2)请你再设计一个实验,区别上述两种溶液:
方案1:分别取少许两种溶液,各滴入几滴无色酚酞试液,根据酚酞试液是否变红色判断各是哪种溶液?
方案2:分别取少许两种溶液,各加入少量澄清石灰水,根据是否有白色沉淀生成判断各是哪种溶液?
请回答:
(1)该同学设计的两个方案有一个是正确的,该方案是
(2)请你再设计一个实验,区别上述两种溶液:
| 实验操作步骤 | 实验现象 | 实验结论 |
| 用胶头滴管分别吸取少量NaOH、Na2CO3溶液于试管①、②中,并分别向其中滴入少量的 | 试管①: 试管②: | 试管①是NaOH。 试管②是Na2CO3.理由是:(用化学方程式表示): |
17-18九年级下·广东梅州·阶段练习 查看更多[4]
山东省济宁市微山县兴体中学2019届九年级下学期中考一模化学试题广东省梅州市梅江区伯聪学校2019届九年级下学期第一次月考化学试题(已下线)专题10 酸碱盐性质的探究(预测题)-决胜2018中考化学压轴题全揭秘精品广东省梅州市梅江区实验中学2018届九年级下学期第一次质检化学试题
更新时间:2018-04-23 20:49:05
|
相似题推荐
【推荐1】酸碱盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出______ 。
(2)检验敞口放置的氢氧化钠溶液是否变质,可以选用的一种试剂是______ 。
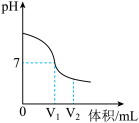
(3)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图,当滴入溶液为V2mL时,所得溶液中溶质化学式为______ ,所得溶液能使紫色石蕊溶液变成______ 色。
(4)氯化钠是生活中常见的盐,为除去某粗盐水中的MgSO4、CaCl2杂质,得到NaCl溶液,某化学小组设计了如下实验方案。

①过滤操作中所用到的玻璃仪器有烧杯、漏斗和______ 。
②以上方案中有关反应的化学方程式为____________ 。(写一个即可)
③写出溶液乙中含有的杂质______ ,并将以上方案补充完整________________ 。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出
(2)检验敞口放置的氢氧化钠溶液是否变质,可以选用的一种试剂是
(3)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图,当滴入溶液为V2mL时,所得溶液中溶质化学式为

(4)氯化钠是生活中常见的盐,为除去某粗盐水中的MgSO4、CaCl2杂质,得到NaCl溶液,某化学小组设计了如下实验方案。

①过滤操作中所用到的玻璃仪器有烧杯、漏斗和
②以上方案中有关反应的化学方程式为
③写出溶液乙中含有的杂质
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】工业上常用电解饱和食盐水的方法制取烧碱,其反应原理为:2NaCl+2H2O 2NaOH+H2↑+Cl2↑,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
2NaOH+H2↑+Cl2↑,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
①取少量样品于烧杯中,加入过量稀盐酸,观察到有气泡产生,说明样品中含有________ 。
②继续向烧杯中加入硝酸银溶液,出现白色沉淀,甲同学得出结论:样品中还含有氯化钠,乙同学对该结论提出了质疑,认为不一定含有氯化钠,其理由是________ ;丙同学提出只需将试剂 _____ 换成 ______ 就可以确定氯化钠是否存在。
③丁同学认为还需要确认样品中是否含有氢氧化钠,于是大家取少量样品配成溶液后进行以下实验:
通过实验,兴趣小组同学得出结论:该工业烧碱中含有Na2CO3、NaCl和NaOH。
④同学们还想测定该烧碱中碳酸钠的质量分数。他们取10克烧碱样品配成溶液,向其中
逐滴加入BaCl2溶液,产生沉淀的量与所加BaCl2的量关系如图所示。(NaOH和BaCl2不反应)

(1)求样品中Na2CO3的质量分数_____ 。( 写出计算过程)
(2)B点处所得溶液中溶质有________ 。
 2NaOH+H2↑+Cl2↑,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
2NaOH+H2↑+Cl2↑,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:①取少量样品于烧杯中,加入过量稀盐酸,观察到有气泡产生,说明样品中含有
②继续向烧杯中加入硝酸银溶液,出现白色沉淀,甲同学得出结论:样品中还含有氯化钠,乙同学对该结论提出了质疑,认为不一定含有氯化钠,其理由是
③丁同学认为还需要确认样品中是否含有氢氧化钠,于是大家取少量样品配成溶液后进行以下实验:
实验操作 | 现象 | 结论 |
样品中有氢氧化钠 |
④同学们还想测定该烧碱中碳酸钠的质量分数。他们取10克烧碱样品配成溶液,向其中
逐滴加入BaCl2溶液,产生沉淀的量与所加BaCl2的量关系如图所示。(NaOH和BaCl2不反应)

(1)求样品中Na2CO3的质量分数
(2)B点处所得溶液中溶质有
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】NaOH是重要的化工原料,研究其制备、检验、贮存及应用具有重要意义。
(1)某化学兴趣实验小组的同学在探究碱的化学性质实验时,用到了氢氧化钠溶液和氢氧化钙溶液。小甲同学不小心将这两种溶液混合在-一起,结果产生__________________ 的现象,说明氢氧化钠溶液变质了,这是NaOH与空气中的__________ 反应的结果。
(2)小乙同学想用酚酞试液检验氢氧化钠溶液是否变质,你认为这种方法是否可行,为什么?___________________ 。
(3)NaOH俗称“火碱”、“烧碱” ,有很强的腐蚀性,不小心洒到皮肤上,应立即用大量水冲洗,再涂上__________________ 溶液(写名称)。
(4)小丙同学欲用氢氧化钠固体与水配制50g溶质质量分数为10%的氢氧化钠溶液,下列选项错误的是_________________ (填“A”、“B”、“C”、“D”之一)。
①需称取氢氧化钠固体5.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,可将氢氧化钠放在纸上称量
④用量筒量取水的体积时,俯视读数
⑤溶解时用玻璃棒搅拌,玻璃棒的作用是引流
A只有①③④
B只有②④⑤
C只有③④⑤
D只有②③⑤
(5)小丁同学将10%的氢氧化钠溶液,逐滴加入到60g硫酸镁溶液中。当滴入10%氢氧化钠溶液40g时,恰好完全反应。试通过计算,求此时所得不饱和溶液的质量___________________ (计算结果精确至0.1g)。
(1)某化学兴趣实验小组的同学在探究碱的化学性质实验时,用到了氢氧化钠溶液和氢氧化钙溶液。小甲同学不小心将这两种溶液混合在-一起,结果产生
(2)小乙同学想用酚酞试液检验氢氧化钠溶液是否变质,你认为这种方法是否可行,为什么?
(3)NaOH俗称“火碱”、“烧碱” ,有很强的腐蚀性,不小心洒到皮肤上,应立即用大量水冲洗,再涂上
(4)小丙同学欲用氢氧化钠固体与水配制50g溶质质量分数为10%的氢氧化钠溶液,下列选项错误的是
①需称取氢氧化钠固体5.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,可将氢氧化钠放在纸上称量
④用量筒量取水的体积时,俯视读数
⑤溶解时用玻璃棒搅拌,玻璃棒的作用是引流
A只有①③④
B只有②④⑤
C只有③④⑤
D只有②③⑤
(5)小丁同学将10%的氢氧化钠溶液,逐滴加入到60g硫酸镁溶液中。当滴入10%氢氧化钠溶液40g时,恰好完全反应。试通过计算,求此时所得不饱和溶液的质量
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】学校进行消防演练时,同学们学习并使用了某品牌的干粉灭火器。
(1)该干粉灭火器的主要成分有:碳酸氢钠(俗名______ )、硬脂酸镁、滑石粉。
(2)干粉灭火器的灭火原理是______ ,使用干粉灭火器灭火的正确操作顺序是______ 。
A 按下压把,对准火焰根部扫射
按下压把,对准火焰根部扫射
B 拔出保险销
拔出保险销
C 解脱喷管
解脱喷管
(3)同学们对灭火后残留的白色固体产生了兴趣,并进行了如下的探究:
【查阅资料】Ⅰ.硬脂酸镁、滑石粉不溶于水,碳酸氢钠可溶于水。
Ⅱ.碳酸氢钠受热易分解,生成碳酸钠、水、和二氧化碳。
Ⅲ NaHCO3与CaCl2不反应,CaCl2溶液呈中性, NaHCO3与 可以发生如下反应:
可以发生如下反应:
【实验探究】称取25g白色固体,加足量的水溶解、过滤得滤液100g。
①甲组同学取少量滤液于试管中,滴加足量的稀盐酸,产生大量气泡的原因是______ (用化学方程式表示,写一个即可)。
②乙组同学取40g滤液于烧杯中,加入足量CaCl2溶液后过滤、洗涤、干燥,得5g白色固体;再向反应后的滤液滴加酚酞试液,显红色,则碳酸氢钠的水溶液呈______ 性(选填“酸性”或“碱性”或“中性”)。原100g的滤液中一定含有______ 。
③丙组同学另取40g滤液,滴加足量的氢氧化钙溶液,充分反应后过滤、洗涤、干燥得10g固体。计算25g白色固体中NaHCO3的质量分数______ (写出计算过程)。
(1)该干粉灭火器的主要成分有:碳酸氢钠(俗名
(2)干粉灭火器的灭火原理是
A
 按下压把,对准火焰根部扫射
按下压把,对准火焰根部扫射B
 拔出保险销
拔出保险销C
 解脱喷管
解脱喷管(3)同学们对灭火后残留的白色固体产生了兴趣,并进行了如下的探究:
【查阅资料】Ⅰ.硬脂酸镁、滑石粉不溶于水,碳酸氢钠可溶于水。
Ⅱ.碳酸氢钠受热易分解,生成碳酸钠、水、和二氧化碳。
Ⅲ NaHCO3与CaCl2不反应,CaCl2溶液呈中性, NaHCO3与
 可以发生如下反应:
可以发生如下反应:
【实验探究】称取25g白色固体,加足量的水溶解、过滤得滤液100g。
①甲组同学取少量滤液于试管中,滴加足量的稀盐酸,产生大量气泡的原因是
②乙组同学取40g滤液于烧杯中,加入足量CaCl2溶液后过滤、洗涤、干燥,得5g白色固体;再向反应后的滤液滴加酚酞试液,显红色,则碳酸氢钠的水溶液呈
③丙组同学另取40g滤液,滴加足量的氢氧化钙溶液,充分反应后过滤、洗涤、干燥得10g固体。计算25g白色固体中NaHCO3的质量分数
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究。
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】(1)按图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论_____________ (选填“合理”或“不合理”).

(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀与试管中加稀盐酸,有气泡产生.写出产生沉淀的化学方程式____________ .分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清液于两支试管中,按下图探究.
②乙组认为甲组实验不能证明清液中一定有氢氧化钠,理由是 ____________ .他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红.
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是____________
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的____________ .(填序号)
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】(1)按图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论

(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀与试管中加稀盐酸,有气泡产生.写出产生沉淀的化学方程式
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清液于两支试管中,按下图探究.
| 方案 |  |  |
| 现象 | 溶液变红 | 产生 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐3】某校化学兴趣小组进行了甲、乙两个实验。

(1)甲实验中反应的化学方程式为_____ ;
(2)乙实验观察到的现象是_____ 。
(3)实验结束后,小组同学把实验后的两支试管的溶液倒入同一个烧杯中,发现烧杯中仅得到无色溶液,他们决定对烧杯中溶液的溶质成分进行探究。
【提出问题】烧杯中溶液的溶质成分是什么?
一致认为认为溶液的溶质一定有Na2SO4和_____ ;溶质中还可能有什么?
【进行猜想】小明认为烧杯中溶液的溶质可能有NaOH,小亮认为烧杯中溶液的溶质可能有_____ ;小红认为烧杯中溶液的溶质可能有Na2CO3和NaOH。
【验证猜想】
【结论分析】小刚认为实验操作②的结论不严谨,因为 _____ (用文字表述);若要确定小红的猜想是否成立,应另取少量烧杯中的溶液于试管中,滴加 _____ ,然后观察是否有 _____ 出现,反应的方程式为 _____ 。
【拓展与思考】如果实验操作①中测得的pH=7,烧杯中溶液的溶质成分是_____ ;
可见,探究反应后所得物质的成分时,既要考虑生成物,还要考虑反应物是否过量。
【综合计算】向50g硫酸铜溶液中,逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:

(1)恰好完全反应时,溶液的质量为_____ g。
(2)求原硫酸铜溶液中溶质的质量分数_____ (写出计算过程)。
(3)在实验过程中,以下说法正确的是_____ 。
A 0至b段溶液中溶质质量逐渐增加
B a、b、c点对应的溶液中溶质均为一种
C 向c点对应的溶液中滴加酚酞溶液,溶液变红
D 整个过程中,溶液中氢元素的质量一直在增加

(1)甲实验中反应的化学方程式为
(2)乙实验观察到的现象是
(3)实验结束后,小组同学把实验后的两支试管的溶液倒入同一个烧杯中,发现烧杯中仅得到无色溶液,他们决定对烧杯中溶液的溶质成分进行探究。
【提出问题】烧杯中溶液的溶质成分是什么?
一致认为认为溶液的溶质一定有Na2SO4和
【进行猜想】小明认为烧杯中溶液的溶质可能有NaOH,小亮认为烧杯中溶液的溶质可能有
【验证猜想】
| 实验操作 | 现象 | 结论 |
| ①取少量烧杯中的溶液于试管,测定pH. | pH>7 | 溶液呈 |
| ②另取少量烧杯中的溶液于试管中,滴加足量BaCl2溶液,静置,再滴加无色酚酞。 | 溶液由无色变为红色。 | 小红的猜想成立 |
【拓展与思考】如果实验操作①中测得的pH=7,烧杯中溶液的溶质成分是
可见,探究反应后所得物质的成分时,既要考虑生成物,还要考虑反应物是否过量。
【综合计算】向50g硫酸铜溶液中,逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:

(1)恰好完全反应时,溶液的质量为
(2)求原硫酸铜溶液中溶质的质量分数
(3)在实验过程中,以下说法正确的是
A 0至b段溶液中溶质质量逐渐增加
B a、b、c点对应的溶液中溶质均为一种
C 向c点对应的溶液中滴加酚酞溶液,溶液变红
D 整个过程中,溶液中氢元素的质量一直在增加
您最近一年使用:0次



