水和溶液是生活中常见的物质。
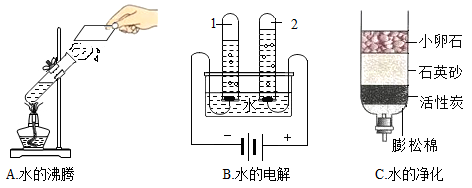
(1)图B中发生反应的化学方程式为__________ , 图 C 中活性炭的作用的是_____ 。
(2)从微观角度解释图A与图B中所发生的变化的本质不同是___________________ 。
(3)甲乙两种不含结晶水的固体物质的溶解度曲线如图所示。

①t2℃时,甲、乙两种物质的溶解度比较:甲___________ 乙(填“>”“<”或“=”)。
②t1℃,将50 g水加入25 g甲物质中,充分搅拌, 可得到_________ g 溶液。
③要使接近饱和的乙溶液转化为饱和溶液,可采用__________ 方法。

(1)图B中发生反应的化学方程式为
(2)从微观角度解释图A与图B中所发生的变化的本质不同是
(3)甲乙两种不含结晶水的固体物质的溶解度曲线如图所示。

①t2℃时,甲、乙两种物质的溶解度比较:甲
②t1℃,将50 g水加入25 g甲物质中,充分搅拌, 可得到
③要使接近饱和的乙溶液转化为饱和溶液,可采用
更新时间:2018-05-15 10:21:16
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】根据所学知识回答下列问题:
(1)氧气是一种与人类生活紧密相关的气体,请根据要求回答:
①现有三瓶无色气体分别是氧气、空气、氮气,下列方法中,能直接鉴别出这三种无色气体的是___________ (填选项序号之一)。
A 观察气体颜色 B.澄清石灰水 C.燃着的木条 D.闻气体气味
②动植物的生命活动都离不开氧气,说明氧气具有___________ 的用途。
(2)构建知识网络是学习化学的重要方法。如图是小明同学绘制的表示氧气制取和化学性质的部分网络图(图中“→”表示一种物质能转化成另一种物质,部分反应的条件、反应物及生成物已经略去),A、B、C分别表示初中化学常见的物质,已知A是最常用的溶剂, B是一种含铜元素的黑色氧化物。

试结合图示回答问题:
①写出物质的化学式:A___________ , B___________ 。
②A物质、H2O2、KMnO4都可以制得氧气,是因为这三种物质中都含有___________ 元素。
③写出上图中反应生成MgO的化学方程式___________ 。
④木炭在氧气中充分燃烧生成的气体B能使澄清石灰水变___________ 。
⑤请从微观角度分析木炭在氧气中燃烧比在空气中更剧烈的原因是___________ 。
(1)氧气是一种与人类生活紧密相关的气体,请根据要求回答:
①现有三瓶无色气体分别是氧气、空气、氮气,下列方法中,能直接鉴别出这三种无色气体的是
A 观察气体颜色 B.澄清石灰水 C.燃着的木条 D.闻气体气味
②动植物的生命活动都离不开氧气,说明氧气具有
(2)构建知识网络是学习化学的重要方法。如图是小明同学绘制的表示氧气制取和化学性质的部分网络图(图中“→”表示一种物质能转化成另一种物质,部分反应的条件、反应物及生成物已经略去),A、B、C分别表示初中化学常见的物质,已知A是最常用的溶剂, B是一种含铜元素的黑色氧化物。

试结合图示回答问题:
①写出物质的化学式:A
②A物质、H2O2、KMnO4都可以制得氧气,是因为这三种物质中都含有
③写出上图中反应生成MgO的化学方程式
④木炭在氧气中充分燃烧生成的气体B能使澄清石灰水变
⑤请从微观角度分析木炭在氧气中燃烧比在空气中更剧烈的原因是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】2023年6月,中国航天捷报频传,神舟十六号顺利升天,神舟十五号成功返回,航天梦,照亮中国科技兴国路,请回答下列问题:
(1)下表为航天器所用的燃料和氧化剂,请回答:
①上述所有物质中属于混合物的有________ (填名称),属于单质的有________ (填化学式)。
②标出高氯酸铵(NH4ClO4)中氯元素的化合价________ 。
③火箭中偏二甲肼(C2H8N2)与四氧化二氮(N2O4)点燃后,反应生成空气中最多气体和另外两种氧化物,并放出大量的热,请写出其化学方程式为:________ 。
(2)宇宙飞船所用的新型材料里其中应用了镁锂合金,请回答下列问题:
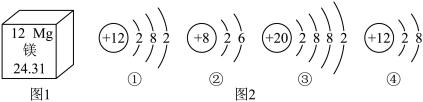
①图1为镁在元素周期表中的部分信息,则镁的相对原子质量为________ 。
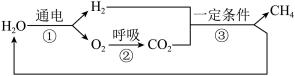
②图2为几种粒子的结构示意图,其中属于同种元素的是________ (填序号,下同),与镁元素化学性质相似的是________ 。
(3)天宫空间站中水气整合系统简易流程如图,该过程中,可循环利用的化合物是________ (填化学式),请写出反应③的化学方程式________ ,空间站内所需要的氧气来自水的电解,若实验室用10%的NaOH溶液配制200g4%的NaOH溶液用于电解实验,则需要10%的NaOH溶液________ g。
(4)航天员出舱需携带高压氧气罐,并将氧气罐集成到舱外航天服上,氧气可以压缩储存在氧气罐中的微观实质是________ ,此外,在航天服生命保障系统中还常用过氧化钠吸收航天员呼出的CO2,反应原理为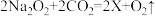 则X的化学式
则X的化学式________ ,若一定时间内航天员所排出CO2的质量为110g,若将其完全吸收,则同时产生氧气的体积为________ 升(通常状况下的氧气密度约为1.4g/L,计算结果精确到0.1),航天员在空间站内不需要穿笨重的航天服也能正常地生活和工作,则空间站为航天员提供的必要条件是________ 。
A.适宜的温度B.纯氧环境 C.饮用水 D.与地球相仿的气压
(5)神舟号载人飞船返回舱返回时,与大气剧烈摩擦,舱表面会产生数千度的高温,此时,舱表面的“烧蚀层”会汽化燃烧保护返回舱不因高温而烧毁。从燃烧的条件解释返回舱不会被烧毁的原因可能是________ ,返回舱的返回动力来自液氢和液氧,在即将着陆前要迅速释放剩余的燃料,这样做的目的是________ 。(答一点即可)
(1)下表为航天器所用的燃料和氧化剂,请回答:
| 一级火箭 | 二级火箭 | 三级火箭 | 固体燃料 | |
| 燃料 | 煤油 | 液氢 | 偏二甲肼(液态) | 铝粉 |
| 氧化剂 | 液氧 | 液氧 | 四氧化二氮(液态) | 高氯酸铵 |
②标出高氯酸铵(NH4ClO4)中氯元素的化合价
③火箭中偏二甲肼(C2H8N2)与四氧化二氮(N2O4)点燃后,反应生成空气中最多气体和另外两种氧化物,并放出大量的热,请写出其化学方程式为:
(2)宇宙飞船所用的新型材料里其中应用了镁锂合金,请回答下列问题:


①图1为镁在元素周期表中的部分信息,则镁的相对原子质量为
②图2为几种粒子的结构示意图,其中属于同种元素的是
(3)天宫空间站中水气整合系统简易流程如图,该过程中,可循环利用的化合物是
(4)航天员出舱需携带高压氧气罐,并将氧气罐集成到舱外航天服上,氧气可以压缩储存在氧气罐中的微观实质是
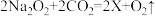 则X的化学式
则X的化学式A.适宜的温度B.纯氧环境 C.饮用水 D.与地球相仿的气压
(5)神舟号载人飞船返回舱返回时,与大气剧烈摩擦,舱表面会产生数千度的高温,此时,舱表面的“烧蚀层”会汽化燃烧保护返回舱不因高温而烧毁。从燃烧的条件解释返回舱不会被烧毁的原因可能是
您最近一年使用:0次
【推荐3】带着对钠电池开发的期待,某同学对钠及其化合物开展了系列探究。
【探究一】钠和水的反应取一小块钠,放入50mL水中,观察到钠浮在水面做不规则游动,变成闪亮的小球,发出“嘶嘶”声响,偶尔气体爆鸣并火光闪现,小球变小最后消失。用pH传感器和温度传感器分别获得相关变化曲线如图所示。

(1)根据图,该反应属于_____ (填“放热”或“吸热”)反应,反应后溶液呈_______ (填“酸”“中”或“碱”)性。
(2)根据上述现象写出钠的一条物理性质__________ (合理即可)。
(3)反应的化学方程式为__________ 。
【探究二】久置氢氧化钠的变质情况
【提出问题】①氢氧化钠是否变质?
②氢氧化钠是部分变质还是完全变质?
【查阅资料】氯化钙溶液、氯化钡溶液、硝酸钙溶液、硝酸钡溶液呈中性;
【设计实验】探究氢氧化钠固体的变质情况
(4)小红同学取少量该固体样品置于试管中,向其中加入少量稀盐酸,无明显变化,她认为该样品没有发生变质。你认为她说的是否正确,理由是________ 。
(5)为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如表所示的实验,请将下表填写完整。
【探究一】钠和水的反应取一小块钠,放入50mL水中,观察到钠浮在水面做不规则游动,变成闪亮的小球,发出“嘶嘶”声响,偶尔气体爆鸣并火光闪现,小球变小最后消失。用pH传感器和温度传感器分别获得相关变化曲线如图所示。

(1)根据图,该反应属于
(2)根据上述现象写出钠的一条物理性质
(3)反应的化学方程式为
【探究二】久置氢氧化钠的变质情况
【提出问题】①氢氧化钠是否变质?
②氢氧化钠是部分变质还是完全变质?
【查阅资料】氯化钙溶液、氯化钡溶液、硝酸钙溶液、硝酸钡溶液呈中性;
【设计实验】探究氢氧化钠固体的变质情况
(4)小红同学取少量该固体样品置于试管中,向其中加入少量稀盐酸,无明显变化,她认为该样品没有发生变质。你认为她说的是否正确,理由是
(5)为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如表所示的实验,请将下表填写完整。
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
| 取少量该固体样品溶于水配成溶液,滴加 | 有关反应的化学方程式为 | ||
| 检验样品中是否还含有氢氧化钠 | 向过滤后的滤液中滴入 | 该样品中还含有氢氧化钠 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】水是一切生物生存所必需的物质,我们应该了解有关水的一些知识。
(1)水是生命之源。净化水的主要操作步骤有沉淀、过滤、______ 、杀菌消毒等;硬水给生活和生产带来很多麻烦,生活中常用______ 方法降低水的硬度;“节约用水,从你我做起”,你的一种具体做法是______ 。
(2)有一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,该反应的化学方程式为______ 。从能量变化角度看,该反应将电能转化为______ 能;实验室用“电解水”或“氢气在氧气中燃烧”的实验探究水的组成元素,理论依据是______ 。
(3)水分子在特定条件下能够解离而得到 和
和 ,
, 易与水分子形成水合氢离子
易与水分子形成水合氢离子 ,与水分子相比,下列对水合氢离子描述不合理的是
,与水分子相比,下列对水合氢离子描述不合理的是______ 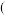 填字母序号
填字母序号 。
。
A.微粒的构成发生了改变 B.氧元素的化合价发生了改变
C.微粒的化学性质发生了改变 D.微粒的电子数发生了改变
(4)溶液有广泛的应用。某同学配制溶液时,在用量筒量取所需水的过程中,他俯视读数,这样配制得到的溶液溶质质量分数会______  填“偏大”、“偏小”、或“无影响”
填“偏大”、“偏小”、或“无影响” 。
。
(1)水是生命之源。净化水的主要操作步骤有沉淀、过滤、
(2)有一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,该反应的化学方程式为
(3)水分子在特定条件下能够解离而得到
 和
和 ,
, 易与水分子形成水合氢离子
易与水分子形成水合氢离子 ,与水分子相比,下列对水合氢离子描述不合理的是
,与水分子相比,下列对水合氢离子描述不合理的是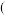 填字母序号
填字母序号 。
。A.微粒的构成发生了改变 B.氧元素的化合价发生了改变
C.微粒的化学性质发生了改变 D.微粒的电子数发生了改变
(4)溶液有广泛的应用。某同学配制溶液时,在用量筒量取所需水的过程中,他俯视读数,这样配制得到的溶液溶质质量分数会
 填“偏大”、“偏小”、或“无影响”
填“偏大”、“偏小”、或“无影响” 。
。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】水是生命之源,也是人类宝贵的自然资源。
天然水净化为自来水的主要流程如图1所示:
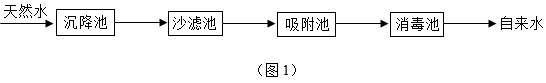
(1)“吸附池”中常用_____ (填物质名称)吸附一些可溶性杂质,除去色素和异味。
(2)“消毒池”中可用高铁酸钠(Na2FeO4)作消毒剂。高铁酸钠中铁元素的化合价为_____ ;高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,其反应的化学方程式为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3X+5H2O,X的化学式为_____ 。
(3)下面是小明在实验室里进行水净化的部分操作:将浑浊的湖水倒入烧杯中,先加入明矾搅拌溶解,静置,然后进行如图2所示的操作。请写出如图2所示操作的错误之处:

①_____ ;②_____ 。
(4)如图3是阳离子交换柱软化硬水的原理(图中阴离子未画出)。交换后的水仍然呈电中性。
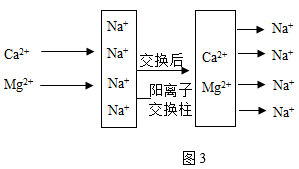
①生活中可用_____ (填物质名称)鉴别硬水和软水。
②2个Na+可以交换出水中_____ 个Ca2+。
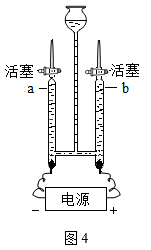
(5)请设计实验检验电解水实验(如图4所示)中b玻璃管中产生的气体,并完成实验报告。
天然水净化为自来水的主要流程如图1所示:

(1)“吸附池”中常用
(2)“消毒池”中可用高铁酸钠(Na2FeO4)作消毒剂。高铁酸钠中铁元素的化合价为
(3)下面是小明在实验室里进行水净化的部分操作:将浑浊的湖水倒入烧杯中,先加入明矾搅拌溶解,静置,然后进行如图2所示的操作。请写出如图2所示操作的错误之处:

①
(4)如图3是阳离子交换柱软化硬水的原理(图中阴离子未画出)。交换后的水仍然呈电中性。

①生活中可用
②2个Na+可以交换出水中
(5)请设计实验检验电解水实验(如图4所示)中b玻璃管中产生的气体,并完成实验报告。

| 实验步骤 | 实验现象 | 实验结论 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】水是生命之源。请回答下列问题。

(1)生活中可用图甲装置来净化天然水,石英砂的作用是_____ 。检验净化后的水是软水和硬水可用物质_____ 。
(2)实验室中图乙过滤操作中,玻璃棒的作用是_____ ;图丙蒸馏操作中,圆底烧瓶中碎瓷 片的作用是_____ 。
(3)载人飞船中核心舱环控生保半封闭系统工作原理如图丁。

①“水净化系统”中用到明矾,其作用是_____ 。
②“二氧化碳收集系统”中的分子筛结构类似于活性炭,具有_____ 作用。
③“萨巴蒂尔反应器”内,在一定条件下可实现 CO2 的吸收和转化,反应的符号表达式为_______ 。
④“水电解系统”中负极产生的是_____ ;正极产生的气体用于氢氧燃料电池,表现出 了_____ 性。
⑤要在失重的状态下收集制得的 O2 可选用下列装置中的_____ (填序号)。


(1)生活中可用图甲装置来净化天然水,石英砂的作用是
(2)实验室中图乙过滤操作中,玻璃棒的作用是
(3)载人飞船中核心舱环控生保半封闭系统工作原理如图丁。

①“水净化系统”中用到明矾,其作用是
②“二氧化碳收集系统”中的分子筛结构类似于活性炭,具有
③“萨巴蒂尔反应器”内,在一定条件下可实现 CO2 的吸收和转化,反应的符号表达式为
④“水电解系统”中负极产生的是
⑤要在失重的状态下收集制得的 O2 可选用下列装置中的

您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】数型图象是研究化学问题的一种常见描述方法,根据下列图象进行回答:

(1)图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线 向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为
向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为 ______  填离子符号
填离子符号 ;
;
(2)图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系.
①由图可知中和反应是放热反应,你的依据为______ ;
②甲同学用氢氧化钠固体与稀盐酸反应也能得到相同结论,乙同学认为不严密,因为______ ;
③图三是a、b、c三种物质的溶解度曲线a与c的溶解度相交于P点,据图回答:
①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用______ 的方法达到饱和状态;
②将t2℃时,150ga物质的饱和溶液降温到t1℃时,可以析出____ g a物质.

(1)图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线
 向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为
向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为  填离子符号
填离子符号 ;
;(2)图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系.
①由图可知中和反应是放热反应,你的依据为
②甲同学用氢氧化钠固体与稀盐酸反应也能得到相同结论,乙同学认为不严密,因为
③图三是a、b、c三种物质的溶解度曲线a与c的溶解度相交于P点,据图回答:
①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用
②将t2℃时,150ga物质的饱和溶液降温到t1℃时,可以析出
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】请回答下列问题。
(1)2021年5月15日,中国“天问一号”探测器成功着陆火星,它应用的新型镁锂合金材料由西安某公司自主研发。回答下列问题:
①镁锂合金硬度比其纯金属的硬度_____ (填“大”或“小”)
②图1为镁元素在元素周期表中的信息,从图1中可获取的信息________ (写一条)。
图2为几种粒子的结构示意图,其中属于同种元素的是________ (填序号),化学性质相似的是_____ (填序号)。

(2)如图是a、b、c三种固体物质的溶解度曲线,据图回答问题:

①现有t1℃接近饱和的c溶液,若不改变溶质的质量分数,将其变成饱和溶液的方法是________
②将t2℃时a、b的饱和溶液分别降温到t1℃,析出晶体的质量大小关系为:______ (填序号)。
A.a>b B. a < b C.a=b D.无法确定
(1)2021年5月15日,中国“天问一号”探测器成功着陆火星,它应用的新型镁锂合金材料由西安某公司自主研发。回答下列问题:
①镁锂合金硬度比其纯金属的硬度
②图1为镁元素在元素周期表中的信息,从图1中可获取的信息
图2为几种粒子的结构示意图,其中属于同种元素的是

(2)如图是a、b、c三种固体物质的溶解度曲线,据图回答问题:

①现有t1℃接近饱和的c溶液,若不改变溶质的质量分数,将其变成饱和溶液的方法是
②将t2℃时a、b的饱和溶液分别降温到t1℃,析出晶体的质量大小关系为:
A.a>b B. a < b C.a=b D.无法确定
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】如表是KNO3和NH4Cl分别在不同温度时的溶解度。
(1)根据数据,绘制二者的溶解度曲线如图所示,a点为曲线的交点。回答下列问题:下列说法错误的是______。(填序号)。

(2)60℃时,c点的KNO3溶液属于______ (填“饱和”或“不饱和”)状态。欲将处于c点的KNO3溶液转变为b点,可以采取______ (填“降低温度”或“增加溶质”)的措施。
(3)若不改变溶剂的质量,将60℃时的155.2g饱和NH4Cl溶液降温至10℃,能析出NH4Cl晶体的质量为______ g。
(4)将t1℃时M、N的饱和溶液,均升温到60℃,所得两溶液的溶质质量分数的大小关系是M______ N(填“>”、“<”或“=”)。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
(1)根据数据,绘制二者的溶解度曲线如图所示,a点为曲线的交点。回答下列问题:下列说法错误的是______。(填序号)。

| A.二者的溶解度均随温度升高而增大 |
| B.曲线M为KNO3的溶解度曲线 |
| C.a点对应的温度在30℃与40℃之间 |
| D.a点对应的溶解度在37.2g与41.4g之间 |
(2)60℃时,c点的KNO3溶液属于
(3)若不改变溶剂的质量,将60℃时的155.2g饱和NH4Cl溶液降温至10℃,能析出NH4Cl晶体的质量为
(4)将t1℃时M、N的饱和溶液,均升温到60℃,所得两溶液的溶质质量分数的大小关系是M
您最近一年使用:0次
【推荐1】溶液在生产生活中有着广泛的应用。
(1)一瓶合格的生理盐水密封放置一段时间后,不会出现浑浊现象,原因是_______ 。
(2)0℃时,101kPa时氮气溶解度为0.024,其意义为_______ 。
(3)甲、乙两种固体物质的溶解度曲线如图1所示,析出的晶体均不含结晶水,回答下列问题:

①乙物质的溶解性属于______ (填“易溶”或“可溶”或“微溶”或“无法确定”)。
②A是40℃含有120g水的甲溶液,经过如图2操作。得到50g甲固体。

对以上过程的分析,正确的是______ (选填编号)。
A.A到B的过程中,溶质质量没有改变
B.B中溶质与溶剂的质量比为138:100
C.B到C的过程中,溶质甲已全部析出
D.A溶液的质量等于255g
(4)如图3是利用海水提取粗盐的过程。

根据海水晒盐的原理,下列说法正确的是_______ (选填编号)。
(5)现有一瓶蒸馏水和一瓶稀氯化钾溶液,请设计实验把它们鉴别开,并填写实验报告。
(1)一瓶合格的生理盐水密封放置一段时间后,不会出现浑浊现象,原因是
(2)0℃时,101kPa时氮气溶解度为0.024,其意义为
(3)甲、乙两种固体物质的溶解度曲线如图1所示,析出的晶体均不含结晶水,回答下列问题:

①乙物质的溶解性属于
②A是40℃含有120g水的甲溶液,经过如图2操作。得到50g甲固体。

对以上过程的分析,正确的是
A.A到B的过程中,溶质质量没有改变
B.B中溶质与溶剂的质量比为138:100
C.B到C的过程中,溶质甲已全部析出
D.A溶液的质量等于255g
(4)如图3是利用海水提取粗盐的过程。

根据海水晒盐的原理,下列说法正确的是
| A.海水进入贮水池,其中氯化钠的质量减少 |
| B.在蒸发池中,海水中氯化钠的质量逐渐增加 |
| C.在蒸发池中,海水中水的质量逐渐减少 |
| D.析出晶体后的母液是氯化钠的饱和溶液 |
(5)现有一瓶蒸馏水和一瓶稀氯化钾溶液,请设计实验把它们鉴别开,并填写实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】(1)济南市政府近年来逐步加大对黄河两岸生产、生活燃料结构的调整,以新能源代替传统能源。例如:提高居民家中天然气的使用率,改善家居环境,提高生活质量。天然气是洁净环保的优质能源,其主要成分是甲烷(化学式是CH4)。
①写出天然气充分燃烧的化学方程式_____ 。
②天然气属于清洁能源,其理由是_____ 。
(2)工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图1在①~③三个过程中,发生分解反应的是_____ (填序号)。

(3)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠、Na2CO3和NaCl的溶解度曲线如图2所示,试回答下列问题:

①在t1℃时,Na2CO3的溶解度是_____ 。
②t2℃时,NaCl的溶解度_____ Na2CO3的溶解度(填“大于”“等于”“小于”之一)
③要从海水中提取NaCl,应采用的方法是_____ (填“蒸发结晶”或“降温结晶”)
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是_____ g。
①写出天然气充分燃烧的化学方程式
②天然气属于清洁能源,其理由是
(2)工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图1在①~③三个过程中,发生分解反应的是

(3)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠、Na2CO3和NaCl的溶解度曲线如图2所示,试回答下列问题:

①在t1℃时,Na2CO3的溶解度是
②t2℃时,NaCl的溶解度
③要从海水中提取NaCl,应采用的方法是
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是
您最近一年使用:0次
【推荐3】水是一切生合体生在所必委的物质。
(1)爱护水资源,在节约用水的同时防治水体污染,下列做法合理的是_____(填标号)。
(2)①某同学从三河中取间水样、用自制冷水器处理,净水器中活性炭可以_____ (填“吸附”或“蒸馏”)水样中的异味和色素。
②向处理后的水样中加入肥皂水,振荡。观察到泡沫较少,浮渣较多,则该水样属于_____ (填“硬水”或“软水")。
(3)碳酸氢钠和氯化铵的溶解度曲线如图所示。下列说法正确的是_____。
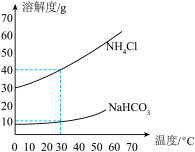
(1)爱护水资源,在节约用水的同时防治水体污染,下列做法合理的是_____(填标号)。
| A.水龙头漏水不及时更换 | B.生活河水集中处理和排放 |
| C.洗脸水冲厕所 | D.农业上合理使用农药和化肥 |
②向处理后的水样中加入肥皂水,振荡。观察到泡沫较少,浮渣较多,则该水样属于
(3)碳酸氢钠和氯化铵的溶解度曲线如图所示。下列说法正确的是_____。

| A.30℃时,NaHCO3的溶解度是40g |
| B.30℃时,饱和溶液的溶质质量分数NH4Cl小于NaHCO3 |
| C.将50℃时NH4Cl的饱和溶液降低到10℃,该饱和溶液的溶质质量分数变大 |
| D.饱和NaCl溶液通NH3至饱和再通入CO2,生成NaHCO3和NH4Cl,NaHCO3将结晶析出 |
您最近一年使用:0次



