一包白色粉末,可能含有CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的一种或几种。为探究其组成进行如下实验:
①取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
②取实验①滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体;
③取实验①得到的滤液,向其中通入CO2,产生白色沉淀;
根据以上实验现象,判断白色粉末。下列结论不正确 的是
①取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
②取实验①滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体;
③取实验①得到的滤液,向其中通入CO2,产生白色沉淀;
根据以上实验现象,判断白色粉末。下列结论
| A.白色粉末中一定不含CuSO4、Na2SO4 | B.白色粉末中一定含有CaCO3、BaCl2 |
| C.白色粉末中一定含有CaCO3、BaCl2、NaOH | D.白色粉末中可能含有NaOH |
更新时间:2018-05-15 12:22:52
|
相似题推荐
选择题-单选题
|
较难
(0.4)
真题
解题方法
【推荐1】医疗上常用硫酸钡作透视肠胃的内服剂,俗称“钡餐”。一旦误将碳酸钡代替硫酸钡作“钡餐” ,就会致人中毒,此时可服用硫酸镁溶液解毒。某化学兴趣小组用如下实验模拟了碳酸钡在胃液中的变化,并验证了硫酸镁解毒的原理:
I.取一定量碳酸钡固体于烧杯中,逐滴加入稀盐酸至过量,并不断搅拌,烧杯内固体质量与加入稀盐酸的质量关系如图甲所示;
II.再向该烧杯中逐滴加入硫酸镁溶液,并不断搅拌,烧杯内溶液质量与加入硫酸镁溶液的质量关系如图乙所示。
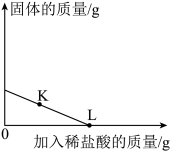

甲 乙
下列有关说法正确的是
I.取一定量碳酸钡固体于烧杯中,逐滴加入稀盐酸至过量,并不断搅拌,烧杯内固体质量与加入稀盐酸的质量关系如图甲所示;
II.再向该烧杯中逐滴加入硫酸镁溶液,并不断搅拌,烧杯内溶液质量与加入硫酸镁溶液的质量关系如图乙所示。


甲 乙
下列有关说法正确的是
| A.图甲中K点和L点时,溶液中的溶质都为一种;图乙中M点和N点时,溶液中的溶质都为两种 |
| B.取少量步骤I所得溶液于试管中,滴加硝酸银溶液和足量稀硝酸,有白色沉淀生成,说明步骤I中加入的稀盐酸已过量 |
| C.根据图乙数据分析,步骤II最终生成硫酸钡沉淀的质量为4.5g |
| D.硫酸镁解毒的原理是:MgSO4+BaCl2=MgCl2+BaSO4↓。因此,本身无毒且能与氯化钡反应生成沉淀的物质,如纯碱也可解毒 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐2】向盛有一定质量未打磨的铝片的烧杯中,逐渐加入一定浓度的稀盐酸。下列图像能正确反映其对应变化关系的是
A. | B. |
C. | D.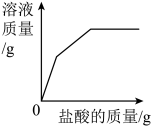 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐3】不列图象能正确反映其对应操作中各量变化关系的是
A. 等质量铝和锌分别加入足量的稀硫酸中 等质量铝和锌分别加入足量的稀硫酸中 |
B. 向一定质量的水中加入生石灰 向一定质量的水中加入生石灰 |
C. 在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量 在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量 |
D. 向等质量的镁和氧化镁中分别加入足量的稀盐酸 向等质量的镁和氧化镁中分别加入足量的稀盐酸 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
名校
【推荐1】除去下列物质中的少量杂质.所用试剂和操作方法都正确的是
| 选项 | 物质 | 杂质 | 试剂和操作方法 |
| A | CO2 | CO | 点燃 |
| B | NH3 | H2O | 通过足量的浓硫酸 |
| C | CuSO4溶液 | H2SO4 | 加入过量的氧化铜,过滤 |
| D | FeSO4溶液 | ZnSO4 | 加入过量的镁粉,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐2】下列各组溶液利用组内的试剂,不能鉴别的是( )
| A.NaOH Ba(NO3)2 HNO3 MgSO4 |
| B.CuSO4 NaOH BaCl2 NaCl |
| C.FeCl3 NaCl KOH K2SO4 |
| D.Na2CO3 KCl Ca(OH)2 HCl |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐1】某溶液中可能含有以下几种离子中的一种或几种:Ba2+、Na+、Ag+、C1-、 、
、 ,现将溶液等分两份:第一份加入AgNO3溶液有白色沉淀产生,再加入过量的稀硝酸后沉淀部分溶解;另一份加足量的BaC12溶液,有白色沉淀产生,再加入过量的稀硝酸沉淀全部溶解。请你根据实验现象,推测原溶液中含有的离子说法正确的是
,现将溶液等分两份:第一份加入AgNO3溶液有白色沉淀产生,再加入过量的稀硝酸后沉淀部分溶解;另一份加足量的BaC12溶液,有白色沉淀产生,再加入过量的稀硝酸沉淀全部溶解。请你根据实验现象,推测原溶液中含有的离子说法正确的是
 、
、 ,现将溶液等分两份:第一份加入AgNO3溶液有白色沉淀产生,再加入过量的稀硝酸后沉淀部分溶解;另一份加足量的BaC12溶液,有白色沉淀产生,再加入过量的稀硝酸沉淀全部溶解。请你根据实验现象,推测原溶液中含有的离子说法正确的是
,现将溶液等分两份:第一份加入AgNO3溶液有白色沉淀产生,再加入过量的稀硝酸后沉淀部分溶解;另一份加足量的BaC12溶液,有白色沉淀产生,再加入过量的稀硝酸沉淀全部溶解。请你根据实验现象,推测原溶液中含有的离子说法正确的是A.一定存在 ,可能存在Ag+ ,可能存在Ag+ | B.可能存在Na+,一定不存在Ag+ |
C.一定不存在 ,可能存在Ca2+ ,可能存在Ca2+ | D.一定存在Na+、Cl-和 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐2】某溶液的溶质可能是 、
、 、
、 、
、 中的一种或几种。某同学取4份此溶液样品,分别进行如下实验:①测定溶液的
中的一种或几种。某同学取4份此溶液样品,分别进行如下实验:①测定溶液的 ;②加入硝酸银溶液,产生白色沉淀,再加稀硝酸,沉淀部分溶解产生气体;③加入足量氯化钡溶液,产生白色沉淀,该沉淀部分溶于稀硝酸且放出气体;④加入足量硝酸钡溶液,产生白色沉淀,过滤后向滤液中加入硝酸银溶液,产生白色沉淀。该同学最终确定该溶液中仅存在
;②加入硝酸银溶液,产生白色沉淀,再加稀硝酸,沉淀部分溶解产生气体;③加入足量氯化钡溶液,产生白色沉淀,该沉淀部分溶于稀硝酸且放出气体;④加入足量硝酸钡溶液,产生白色沉淀,过滤后向滤液中加入硝酸银溶液,产生白色沉淀。该同学最终确定该溶液中仅存在 、
、 、
、 三种溶质。请分析,该同学只需完成上述哪两个实验,即可得出此结论?( )
三种溶质。请分析,该同学只需完成上述哪两个实验,即可得出此结论?( )
 、
、 、
、 、
、 中的一种或几种。某同学取4份此溶液样品,分别进行如下实验:①测定溶液的
中的一种或几种。某同学取4份此溶液样品,分别进行如下实验:①测定溶液的 ;②加入硝酸银溶液,产生白色沉淀,再加稀硝酸,沉淀部分溶解产生气体;③加入足量氯化钡溶液,产生白色沉淀,该沉淀部分溶于稀硝酸且放出气体;④加入足量硝酸钡溶液,产生白色沉淀,过滤后向滤液中加入硝酸银溶液,产生白色沉淀。该同学最终确定该溶液中仅存在
;②加入硝酸银溶液,产生白色沉淀,再加稀硝酸,沉淀部分溶解产生气体;③加入足量氯化钡溶液,产生白色沉淀,该沉淀部分溶于稀硝酸且放出气体;④加入足量硝酸钡溶液,产生白色沉淀,过滤后向滤液中加入硝酸银溶液,产生白色沉淀。该同学最终确定该溶液中仅存在 、
、 、
、 三种溶质。请分析,该同学只需完成上述哪两个实验,即可得出此结论?( )
三种溶质。请分析,该同学只需完成上述哪两个实验,即可得出此结论?( )| A.①② | B.③④ | C.②③ | D.②④ |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐1】溶液的特征颜色,为我们判断溶液中存在的物质提供了重要依据。小聪同学为探究硫酸铜溶液呈蓝色的原因,设计了下面的实验:①取硫酸铜溶液,加水稀释,颜色变浅②比较硫酸铜、硫酸钠两种溶液,硫酸铜溶液为蓝色,硫酸钠溶液为无色③向硫酸铜溶液中滴加过量氢氧化钠溶液至沉淀完全,静置后溶液为无色
其中,能证明Cu2+为硫酸铜溶液呈蓝色原因的方案是
其中,能证明Cu2+为硫酸铜溶液呈蓝色原因的方案是
| A.①② | B.①③ | C.②③ | D.①②③ |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐2】某气体由H2、CO2、CO中的一种或两种组成,为确定其成分进行了下面的实验:
①将气体通过澄清的石灰水,未出现浑浊现象 ②将气体通过灼热的氧化铜,有红色固体生成③将气体点燃后的产物通入澄清的石灰水,有浑浊现象。那么对该气体成分的推断中合理的是
①将气体通过澄清的石灰水,未出现浑浊现象 ②将气体通过灼热的氧化铜,有红色固体生成③将气体点燃后的产物通入澄清的石灰水,有浑浊现象。那么对该气体成分的推断中合理的是
| A.一定有 CO,可能有H2 | B.一定有CO、CO2 |
| C.一定有 CO,可能有CO2 | D.一定有H2、CO2 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
名校
解题方法
【推荐3】有一包白色粉末,可能含有 MgSO4、Na2SO4、K2SO4、CuSO4、NaOH 、BaCl2中的一种或几种。某化学兴趣小组对这包白色粉末的成分展开如下探究:
[查阅资料]氯化钡溶液显中性。
步骤(1):取 13g 白色粉末,投入 50g 水中,搅拌,得到无色溶液。
步骤(2):向(1)所得溶液中加入 100g 足量的 Ba(NO3)2,得到白色沉淀,过滤得滤液质量 139.7g。
结合以上探究过程,下列推理正确的是 ( )
[查阅资料]氯化钡溶液显中性。
步骤(1):取 13g 白色粉末,投入 50g 水中,搅拌,得到无色溶液。
步骤(2):向(1)所得溶液中加入 100g 足量的 Ba(NO3)2,得到白色沉淀,过滤得滤液质量 139.7g。
结合以上探究过程,下列推理正确的是 ( )
| A.白色粉末一定是纯净物 |
| B.白色粉末中至少含 Na2SO4、K2SO4、NaOH 中的某一种或几种 |
| C.白色粉末中至少含 Na2SO4和 K2SO4中的某一种 |
| D.白色粉末中一定不含 CuSO4和 BaCl2,可能含有 NaOH |
您最近一年使用:0次




