某商品碳酸钙粉末包装袋上注明:碳酸钙的含量≥96%。为测定该产品中含碳酸钙的质量分数:取11.0g碳酸钙样品放入烧杯中,称得烧杯及所盛碳酸钙样品的总质量为168.0g,再把100.0g稀盐酸平均分成25.0g依次加入样品中,每次均充分反应(碳酸钙中其它成分不参加反应)。实验数据记录如下:
请你分析并计算(保留一位小数):
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是______ g;
(2)实验过程中,所加盐酸在第_______ 次时碳酸钙已经完全反应;
(3)产品中碳酸钙的质量______ g;碳酸钙的质量分数______ ;该产品________ (填“合格”或“不合格”)。
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 反应后烧杯及所盛物质的总质量/g | 191.2 | 214.4 | 238.6 | 263.6 |
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是
(2)实验过程中,所加盐酸在第
(3)产品中碳酸钙的质量
更新时间:2018-05-17 18:01:59
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】碳酸钙和炭黑的混合物常用作制作橡胶轮胎的填充料,用来改良橡胶性能。取21g样品粉碎后放入烧杯中,向杯中倒入稀盐酸(炭黑不溶于水,也不与稀盐酸反应),当倒入100g稀盐酸后发现不再产生气泡时,测得烧杯内总质量为112.2g。
(1)产生气体的质量为________ g;
(2)计算样品中碳酸钙的质量分数。(计算结果精确到0.1%)
(1)产生气体的质量为________ g;
(2)计算样品中碳酸钙的质量分数。(计算结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某石灰石厂实验室用5.55g石灰石样品高温煅烧制得生石灰(主要成分为氧化钙),实验室过程中进行了四次称量,记录数据如下表(杂质不参加反应,也不分解)
(提示:CaCO3 CaO+CO2)计算:
CaO+CO2)计算:
(1)完全反应后生成二氧化碳_____克。
(2)石灰石中碳酸钙的质量分数是___。(要求计算完整过程,计算结果精确到0.1%)
(3)所得产品生石灰中钙元素的质量是___。(要求计算完整过程。提示:杂质中不含钙元素)
| 操作次数 | 1 | 2 | 3 | 4 |
| 剩余固体质量(g) | 4.25 | 3.95 | 3.35 | 3.35 |
(提示:CaCO3
 CaO+CO2)计算:
CaO+CO2)计算:(1)完全反应后生成二氧化碳_____克。
(2)石灰石中碳酸钙的质量分数是___。(要求计算完整过程,计算结果精确到0.1%)
(3)所得产品生石灰中钙元素的质量是___。(要求计算完整过程。提示:杂质中不含钙元素)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】铝与氢氧化钠溶液反应时生成偏铝酸钠(NaAlO2)和氢气,反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,向盛有20g氢氧化钠溶液的烧杯中加入3.0g铝,充分反应后称量,烧杯内混合物的总质量为22.7g。
计算:
(1)生成氢气的质量为____ g。
(2)该氢氧化钠溶液中溶质的质量分数。
计算:
(1)生成氢气的质量为
(2)该氢氧化钠溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】为了检测某石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得据如下表:
试回答:
①样品中碳酸钙的质量分数为多少?.
②12.5g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程)
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 12.5 | 12.5 | 12.5 | 12.5 |
| 加入盐酸的质量(g) | 30.0 | 40.0 | 55.0 | 70.0 |
| 剩余固体的质量(g) | 6.5 | 4.5 | 2.5 | 2.5 |
试回答:
①样品中碳酸钙的质量分数为多少?.
②12.5g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】铜合金是一种常用的金属材料。
(1)赤铜(Cu2O)是我国古代制取黄铜的一种原料。Cu2O的相对分子质量为 ,Cu2O中铜元素和氧元素的质量比是 。
(2)欲测定某铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下表(Mg+H2SO4=MgSO4+H2↑)。
请计算:①表中m= g,该铜镁合金样品中铜的质量= 。
②所加稀硫酸中溶质的质量分数。(写出计算过程)
(1)赤铜(Cu2O)是我国古代制取黄铜的一种原料。Cu2O的相对分子质量为 ,Cu2O中铜元素和氧元素的质量比是 。
(2)欲测定某铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下表(Mg+H2SO4=MgSO4+H2↑)。
| 次 数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 17.6 | m | 13.2 | 13.2 |
请计算:①表中m= g,该铜镁合金样品中铜的质量= 。
②所加稀硫酸中溶质的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】兴趣小组为测量某品牌纯碱样品(含氯化钠)中碳酸钠的含量,称取该纯碱样品 ,加入
,加入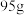 一定溶质质量分数的稀盐酸,恰好完全反应,得到溶液
一定溶质质量分数的稀盐酸,恰好完全反应,得到溶液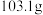 。
。
请回答下列问题:
(1)恰好完全反应时,溶液中的溶质是___________ 。
(2)反应生成二氧化碳的质量为___________ g。
(3)计算该纯碱样品中碳酸钠的质量分数。
(4)我国化学家侯德榜发明了侯氏制碱法,生产过程涉及的主要化学反应为:
I.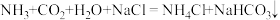 ;
;
II.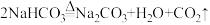 。
。
①反应I后,从混合物中得到 固体的操作是
固体的操作是___________ 。
②若 粉末中混有少量的
粉末中混有少量的 ,除杂的方法是
,除杂的方法是___________ 。
 ,加入
,加入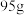 一定溶质质量分数的稀盐酸,恰好完全反应,得到溶液
一定溶质质量分数的稀盐酸,恰好完全反应,得到溶液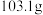 。
。请回答下列问题:
(1)恰好完全反应时,溶液中的溶质是
(2)反应生成二氧化碳的质量为
(3)计算该纯碱样品中碳酸钠的质量分数。
(4)我国化学家侯德榜发明了侯氏制碱法,生产过程涉及的主要化学反应为:
I.
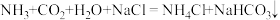 ;
;II.
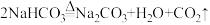 。
。①反应I后,从混合物中得到
 固体的操作是
固体的操作是②若
 粉末中混有少量的
粉末中混有少量的 ,除杂的方法是
,除杂的方法是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为测定实验室制取二氧化碳后液体中氯化钙的溶质质量分数,取溶液100g,逐滴加入碳酸钠溶液,生成沉淀的质量与加入碳酸钠溶液的质量关系如图。___________ g。
(2)计算制取二氧化碳后液体中氯化钙的溶质质量分数。
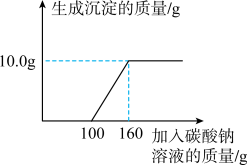
(2)计算制取二氧化碳后液体中氯化钙的溶质质量分数。
您最近一年使用:0次



