乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:____________ ;猜想三:Ca(OH)2,他的依据是______________ 。
【交流反思】经交流讨论,认为猜想一不成立,理由是:_________________ 。
【进行实验】
(1)取少量白色固体放入试管中,滴加稀盐酸,没有观察到____________ ,证明猜想二不成立。
(2)取少量白色固体加入到水中,取上层清液,_________________ ,有白色沉淀出现,证明猜想三成立。该反应的化学方程式为:______________________ 。
结论:白色固体是Ca(OH)2。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:
【交流反思】经交流讨论,认为猜想一不成立,理由是:
【进行实验】
(1)取少量白色固体放入试管中,滴加稀盐酸,没有观察到
(2)取少量白色固体加入到水中,取上层清液,
结论:白色固体是Ca(OH)2。
2018·安徽马鞍山·二模 查看更多[5]
2021年新疆克孜勒苏柯尔克孜自治州阿合奇县同心中学中考一模化学试题2020年甘肃省酒泉市玉门市中考八模化学试题(已下线)【万唯原创】2015年安徽省中考化学试题研究卷九年级题型研究题型四类型一2015年安徽省淮北市杜集区非凡学校中考模拟(4月)化学试题【全国市级联考】安徽省马鞍山市2018届九年级下学期二模化学试题
更新时间:2018-06-01 19:12:26
|
相似题推荐
【推荐1】沙尘暴是我国常见的自然现象。某校环境监测实践小组的同学们,对沙尘暴的成因、危害、成分以及对水资源的影响产生了浓厚的兴趣,在老师的指导下,开启了项目学习的探究之旅。
(1)任务一:分析沙尘暴的影响
当人暴露于沙尘天气中时,含有各种有毒的化学物质、病菌等的尘土可进入到口、鼻、眼、耳中引发各种疾病。我国黄土高原上的厚层黄土是千百万年以来,通过沙尘暴这一自然现象逐渐将其他地方的土壤转移到黄土高原处。黄土肥沃,是因为土壤中富含磷、钾、钙、硫等元素,在黄土上种植庄稼,还需施的肥料主要是______________________ 肥。
(2)任务二:探究沙尘暴的成分
【信息检索】我国西北地区,含有大量钠盐的干涸盐湖和盐碱地总面积约有 50 万平方公里,为沙尘暴的形成埋下隐患。
据此可以猜想:由此引发的沙尘暴中可能含有碳酸钠等碱性物质。
取少量盐碱地的土壤与蒸馏水按 1∶5 的质量比在烧杯中混合,充分搅拌后静置,取上层清液,用如下图装置完成如下实验。

反思:
Ⅰ.步骤①中发生反应的化学方程式为__________________ 。
Ⅱ.自然界的土壤中通常不含 NaOH,理由是__________________ 。
Ⅲ.若加入的 X 是氢氧化钙,则对本次探究的影响是__________________ 。
(3)任务三:沙尘暴对水质的影响
小组同学在老师的帮助下从某西北地区环保部门获得当地河流在沙尘暴发生前后几天河水的pH数据。
发生沙尘暴的日期是______ 。
(1)任务一:分析沙尘暴的影响
当人暴露于沙尘天气中时,含有各种有毒的化学物质、病菌等的尘土可进入到口、鼻、眼、耳中引发各种疾病。我国黄土高原上的厚层黄土是千百万年以来,通过沙尘暴这一自然现象逐渐将其他地方的土壤转移到黄土高原处。黄土肥沃,是因为土壤中富含磷、钾、钙、硫等元素,在黄土上种植庄稼,还需施的肥料主要是
(2)任务二:探究沙尘暴的成分
【信息检索】我国西北地区,含有大量钠盐的干涸盐湖和盐碱地总面积约有 50 万平方公里,为沙尘暴的形成埋下隐患。
据此可以猜想:由此引发的沙尘暴中可能含有碳酸钠等碱性物质。
取少量盐碱地的土壤与蒸馏水按 1∶5 的质量比在烧杯中混合,充分搅拌后静置,取上层清液,用如下图装置完成如下实验。
| 项目 | 实验步骤 | 实验现象 | 实验结论 |
| 方案 | ①挤压胶头滴管a,滴入 | 产生白色沉淀 | 沙尘暴中含有Na2CO3,不含NaOH |
| ②挤压胶头滴管b,滴入几滴酚酞溶液 | 酚酞溶液不变色 |

反思:
Ⅰ.步骤①中发生反应的化学方程式为
Ⅱ.自然界的土壤中通常不含 NaOH,理由是
Ⅲ.若加入的 X 是氢氧化钙,则对本次探究的影响是
(3)任务三:沙尘暴对水质的影响
小组同学在老师的帮助下从某西北地区环保部门获得当地河流在沙尘暴发生前后几天河水的pH数据。
| 测定时间 | 3 月 31 日 | 4 月 1 日 | 4 月 2 日 | 4 月 3 日 |
| pH | 7.73 | 8.05 | 7.78 | 7.76 |
发生沙尘暴的日期是
您最近一年使用:0次
【推荐2】某化学兴趣小组的同学设计了如图所示的装置,探究影响化学反应速率的因素。

(1)如图装置中使用注射器的优点是_____ 。
(2)写出该实验涉及反应的化学方程式:_____ 。
(3)下面是用上述装置实验时,收集的相关数据:
由实验①和②对比可知,化学反应速率与_____ 有关。
由实验③和④对比可知,化学反应速率与温度的关系是_____ 。
(4)发现问题:实验时温度最难控制,反应一段时间后溶液的温度总是比起始时温度高,说明反应_____ ;(填“吸收”或者“放出”)热量。

(1)如图装置中使用注射器的优点是
(2)写出该实验涉及反应的化学方程式:
(3)下面是用上述装置实验时,收集的相关数据:
| 实验 序号 | H2O2溶液 的浓度/% | H2O2溶液 的体积/mL | MnO2的 用量/g | 温度/°C | 收集O2的体积/mL | 反应所需 的时间/s |
| ① | 5 | 2 | 0.1 | 20 | 4 | 18 |
| ② | 10 | 2 | 0.1 | 20 | 4 | 6 |
| ③ | 30 | 8 | / | 40 | 2 | 64 |
| ④ | 30 | 8 | / | 60 | 2 | 25 |
由实验③和④对比可知,化学反应速率与温度的关系是
(4)发现问题:实验时温度最难控制,反应一段时间后溶液的温度总是比起始时温度高,说明反应
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】草酸的化学式为H2C2O4,甲、乙两同学对草酸受热分解及其产物的检验做了探究:
【猜想与假设】
第一种:草酸分解产物是CO2和H2;
第二种:草酸分解产物是CO2、CO和H2O;
第三种:草酸分解产物是CO2和H2O;
第四种:草酸分解产物是CO2、CO;
以上哪种猜想不合理________ 。
【查阅资料】无水硫酸铜遇水由白色变成蓝色,碱石灰是一种常用的干燥剂。
【实验设计】(图中铁架台略去)甲同学设计了甲装置,乙同学设计了乙装置。
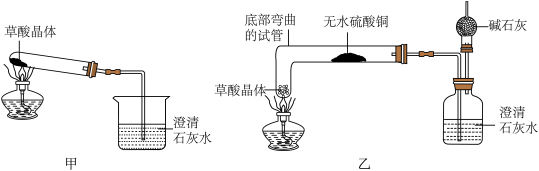
【实验过程】甲同学按甲装置实验,在给草酸晶体加热后,过一会儿观察到澄清石灰水变浑浊;乙同学按乙装置实验,观察到无水硫酸铜由白色变成蓝色,澄清的石灰水变浑浊,且生成的气体通过碱石灰后,在干燥管的尖嘴处点火能燃烧,乙同学进一步通过实验验证燃烧的气体为CO,他的操作是________ ,现象是________ 。
【实验结论】第________ 种猜想是正确的,请写出草酸受热分解的化学方程式________ 。
【反思与评价】乙同学认为甲同学设计的实验装置有缺陷。由于试管口向下倾斜,而且草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中常会出现熔融的草酸流进导管而影响后续实验。甲同学认为乙同学的设计是科学合理的。请你谈谈乙装置优于甲装置之处________ 。(答出一点即可)
【猜想与假设】
第一种:草酸分解产物是CO2和H2;
第二种:草酸分解产物是CO2、CO和H2O;
第三种:草酸分解产物是CO2和H2O;
第四种:草酸分解产物是CO2、CO;
以上哪种猜想不合理
【查阅资料】无水硫酸铜遇水由白色变成蓝色,碱石灰是一种常用的干燥剂。
【实验设计】(图中铁架台略去)甲同学设计了甲装置,乙同学设计了乙装置。

【实验过程】甲同学按甲装置实验,在给草酸晶体加热后,过一会儿观察到澄清石灰水变浑浊;乙同学按乙装置实验,观察到无水硫酸铜由白色变成蓝色,澄清的石灰水变浑浊,且生成的气体通过碱石灰后,在干燥管的尖嘴处点火能燃烧,乙同学进一步通过实验验证燃烧的气体为CO,他的操作是
【实验结论】第
【反思与评价】乙同学认为甲同学设计的实验装置有缺陷。由于试管口向下倾斜,而且草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中常会出现熔融的草酸流进导管而影响后续实验。甲同学认为乙同学的设计是科学合理的。请你谈谈乙装置优于甲装置之处
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】化学老师在取生石灰时,发现装满生石灰的塑料试剂瓶已膨胀破裂。据此,某兴趣小组的同学在老师的指导下开展了以下探究活动。
【提出问题】该样品的成分是什么?
【作出猜想】可能是CaO、Ca(OH)2和CaCO3中的一种或几种。
【实验探究】小华同学设计如下实验进行探究。
【交流讨论】
(1)完成表格。
(2)小雨同学认为通过实验②不能得出样品中一定含有Ca(OH)2,理由可以用化学方程式表示为______ 。
(3)小哲同学认为实验③结论也不正确。他改进实验③的操作为______ ,观察到有大量气泡产生,证明了样品中的确含有碳酸钙,产生气泡的化学方程式为______ 。
【提出问题】该样品的成分是什么?
【作出猜想】可能是CaO、Ca(OH)2和CaCO3中的一种或几种。
【实验探究】小华同学设计如下实验进行探究。
【交流讨论】
(1)完成表格。
实验 | 实验操作 | 实验现象 | 实验结论 |
① | 取样品于烧杯中,加水溶解, 用手触摸烧杯壁。 | 烧杯壁发热 | |
② | 取①中所得上层清液少许于试 管中,滴入 | 溶液变红 | 有Ca(OH)2 |
③ | 在烧杯中剩余白色悬浊液中, 滴加少量稀盐酸。 | 无CaCO3 |
(3)小哲同学认为实验③结论也不正确。他改进实验③的操作为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】胜利中学外出研学时,同学们自带了不同种类的自热食品,对于自热食品中的发热包,他们非常感兴趣,进行了以下系列探究。
【查阅资料】
Ⅰ.如下所示是同学们所带食品中某品牌发热包说明书中的部分内容。
Ⅱ.铝能和NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气,偏铝酸钠溶于水。
【知识应用】
(1)说明书中的生石灰是物质_____ (填名称)的俗称。
探究一:
【提出问题】发热包的发热原理是什么?
【进行实验】
(2)小组同学取出发热包,撕去塑料膜,放入适量凉水中,可观察到的现象是_____ ,固体迅速膨胀,同时还可观察到发热包内固体变硬结块,其可能的原因是 _____ (用化学方程式表示)。
探究二:
【提出问题】反应后固体混合物中含有什么物质?
【进行实验】
①取适量反应后的固体于烧杯中,加入足量蒸馏水溶解,无明显现象。过滤、得到滤渣和滤液。
②取步骤①的滤渣于试管中,加入足量稀盐酸,将产生的气体按如图1所示进行操作。观察到澄清石灰水变浑浊,干冷烧杯内壁有水珠。
【解释与结论】
(3)同学们依据上述实验现象,得出反应后固体中含有_____ 的结论。
(4)上述实验中浓硫酸的作用是_____ 。
【拓展延伸】
(5)根据探究一的实验现象,同学们推测,自热米饭的盖子上有一个透气孔,如果透气孔堵塞,容易造成_____ ,甚至烫伤人。
(6)根据实验探究和你的生活经验,请完善发热包说明书中的贮存条件_____ 。
【查阅资料】
Ⅰ.如下所示是同学们所带食品中某品牌发热包说明书中的部分内容。
| 产品名称:食品专用发热包 主要成分:生石灰、铝粉、碳酸钠 贮存条件:…… |
【知识应用】
(1)说明书中的生石灰是物质
探究一:
【提出问题】发热包的发热原理是什么?
【进行实验】
(2)小组同学取出发热包,撕去塑料膜,放入适量凉水中,可观察到的现象是
探究二:
【提出问题】反应后固体混合物中含有什么物质?
【进行实验】
①取适量反应后的固体于烧杯中,加入足量蒸馏水溶解,无明显现象。过滤、得到滤渣和滤液。
②取步骤①的滤渣于试管中,加入足量稀盐酸,将产生的气体按如图1所示进行操作。观察到澄清石灰水变浑浊,干冷烧杯内壁有水珠。

【解释与结论】
(3)同学们依据上述实验现象,得出反应后固体中含有
(4)上述实验中浓硫酸的作用是
【拓展延伸】
(5)根据探究一的实验现象,同学们推测,自热米饭的盖子上有一个透气孔,如果透气孔堵塞,容易造成
(6)根据实验探究和你的生活经验,请完善发热包说明书中的贮存条件
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐3】生石灰常用作食品干燥剂,其包装上除了表明主要成分为生石灰外,还提醒了人们注意不可食用、不可浸水、不可开袋、儿童勿喷。甲、乙两同学想知道刚从食品袋中取出的生石灰的成分,进行了如下探究:
【提出问题】生石灰干燥剂中含有哪些物质?
【猜想与假设】猜想Ⅰ:含有氧化钙[CaO]、氢氧化钙[Ca(OH)2];
猜想Ⅱ:含有氧化钙[CaO]、碳酸钙[CaCO3];
猜想Ⅲ:含有含有氧化钙[CaO]、氢氧化钙[Ca(OH)2]、碳酸钙[CaCO3]。
【活动与探究】甲、乙两同学为了验证猜想,进行如下实验:
甲同学实验:取少量样品于试管中,加入适量的水充分反应后,再滴加几滴无色酚酞试液,可观察到溶液呈红色。
乙同学实验:取少量样品于试管中,加入足量的稀盐酸,有无色无味气体产生,该气体能使澄清石灰水变浑浊。
【结论与反思】
(1)猜想____ 错误(填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
(2)甲同学实验中发生的反应的方程式:_______________ ,
溶液变红色的原因:_____________________________ 。
(3)乙同学检验气体的方程式:_______________________ 。
(4)乙同学认为甲同学的实验是多余的,因为:___________________________ 。
【拓展应用】甲、乙最终无法确定该生石灰干燥剂的成分,实验失败,丙同学认为可以通过定量实验来确定,在定量实验时,一定要用到的实验操作是:_________ 。
【提出问题】生石灰干燥剂中含有哪些物质?
【猜想与假设】猜想Ⅰ:含有氧化钙[CaO]、氢氧化钙[Ca(OH)2];
猜想Ⅱ:含有氧化钙[CaO]、碳酸钙[CaCO3];
猜想Ⅲ:含有含有氧化钙[CaO]、氢氧化钙[Ca(OH)2]、碳酸钙[CaCO3]。
【活动与探究】甲、乙两同学为了验证猜想,进行如下实验:
甲同学实验:取少量样品于试管中,加入适量的水充分反应后,再滴加几滴无色酚酞试液,可观察到溶液呈红色。
乙同学实验:取少量样品于试管中,加入足量的稀盐酸,有无色无味气体产生,该气体能使澄清石灰水变浑浊。
【结论与反思】
(1)猜想
(2)甲同学实验中发生的反应的方程式:
溶液变红色的原因:
(3)乙同学检验气体的方程式:
(4)乙同学认为甲同学的实验是多余的,因为:
【拓展应用】甲、乙最终无法确定该生石灰干燥剂的成分,实验失败,丙同学认为可以通过定量实验来确定,在定量实验时,一定要用到的实验操作是:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组同学在做硫酸铜和氢氧化钠反应的实验时发现滴加试剂的顺序不同会产生不同的现象,于是他们对产物进行了探究。

【查阅资料】①NaOH和CuSO4溶液混合可生成Cu(OH)2、Cux(OH)y(SO4)z等多种产物
②68℃时,Cu(OH)2发生分解;300℃左右,Cu(OH)2、Cux(OH)y(SO4)z等能发生分解。
(1)实验一中产生的蓝色沉淀是氢氧化铜,将该沉淀加热会分解生成两种氧化物,其中一种为黑色固体,该反应的化学方程式为_________ 。
(2)将实验二反应后的物质过滤、洗涤、低温干燥得浅蓝绿色固体。小组同学称取9.8g该固体,在老师的指导下进行下列实验。

①装配好装置后,实验前先要__________ 。
②控制温度为6对固体进行加热分解至固体质量不再减少,再提高加热器温度至100℃继续通一段时间N2。冷却后测得浓硫酸增重1.2g。
a.实验中利用了浓硫酸的_____ 性来吸收水。通一段时间N2的目的是_______ 。
b.小组同学通过分析得出结论:固体中含有Cu(OH)2和其他物质。得出还含有其他物质的理由是__ (合理即可)。

【查阅资料】①NaOH和CuSO4溶液混合可生成Cu(OH)2、Cux(OH)y(SO4)z等多种产物
②68℃时,Cu(OH)2发生分解;300℃左右,Cu(OH)2、Cux(OH)y(SO4)z等能发生分解。
(1)实验一中产生的蓝色沉淀是氢氧化铜,将该沉淀加热会分解生成两种氧化物,其中一种为黑色固体,该反应的化学方程式为
(2)将实验二反应后的物质过滤、洗涤、低温干燥得浅蓝绿色固体。小组同学称取9.8g该固体,在老师的指导下进行下列实验。

①装配好装置后,实验前先要
②控制温度为6对固体进行加热分解至固体质量不再减少,再提高加热器温度至100℃继续通一段时间N2。冷却后测得浓硫酸增重1.2g。
a.实验中利用了浓硫酸的
b.小组同学通过分析得出结论:固体中含有Cu(OH)2和其他物质。得出还含有其他物质的理由是
您最近一年使用:0次
【推荐2】某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们进行了以下探究。
【提出问题】氢氧化钠溶液是否变质?变质程度如何?
【做出猜想】猜想一:氢氧化钠溶液未变质;猜想二:氢氧化钠溶液完全变质;猜想三:______ 。
【查阅资料】NaOH、Ca(OH)2、KOH、Ba(OH)2分别与HCl、H2SO4、HNO3反应生成的盐溶液呈中性。
【设计实验】请完成实验报告
【反思拓展】
(1)氢氧化钠溶液应______ 保存。
(2)分别取两份完全变质的氢氧化钠溶液样品于试管中,向其中一份加入盐酸有气泡冒出,另一份加入氢氧化钙溶液有白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,所得溶液中溶质一定有______ 。
【提出问题】氢氧化钠溶液是否变质?变质程度如何?
【做出猜想】猜想一:氢氧化钠溶液未变质;猜想二:氢氧化钠溶液完全变质;猜想三:
【查阅资料】NaOH、Ca(OH)2、KOH、Ba(OH)2分别与HCl、H2SO4、HNO3反应生成的盐溶液呈中性。
【设计实验】请完成实验报告
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量溶液于试管中,加入 | 猜想二成立 | |
| (2)将步骤(1)试管中的物质过滤,向滤液中加入 | 无明显现象 |
(1)氢氧化钠溶液应
(2)分别取两份完全变质的氢氧化钠溶液样品于试管中,向其中一份加入盐酸有气泡冒出,另一份加入氢氧化钙溶液有白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,所得溶液中溶质一定有

您最近一年使用:0次
【推荐3】化学实践活动课上,老师拿来一包久置空气中的碱石灰干燥剂(氧化钙和氢氧化钠的混合物),让同学们设计实验进行探究。
(1)碱石灰极易与空气中的水蒸气、二氧化碳反应而变质,其中氧化钙与水变质,氢氧化钠在空气中变质的原因,用化学方程式解释为______ ,因此碱石灰要密封保存。
同学们决定对这包碱石灰成分进行探究。
【猜想假设】
猜想I:未变质,只含有氧化钙和氢氧化钠:
猜想Ⅱ:部分变质,有氢氧化钙、碳酸钙和碳酸钠等:
猜想Ⅲ:完全变质,只含有碳酸钙和碳酸钠。
【查阅资料】氯化钙溶液呈中性,碳酸钠溶液呈碱性。
【设计实验】
(2)设计如下流程进行实验:
【讨论分析】
(3)实验3是否可以先滴加过量氯化钙溶液,再滴入酚酞溶液______ 。
(1)碱石灰极易与空气中的水蒸气、二氧化碳反应而变质,其中氧化钙与水变质,氢氧化钠在空气中变质的原因,用化学方程式解释为
同学们决定对这包碱石灰成分进行探究。
【猜想假设】
猜想I:未变质,只含有氧化钙和氢氧化钠:
猜想Ⅱ:部分变质,有氢氧化钙、碳酸钙和碳酸钠等:
猜想Ⅲ:完全变质,只含有碳酸钙和碳酸钠。
【查阅资料】氯化钙溶液呈中性,碳酸钠溶液呈碱性。
【设计实验】
(2)设计如下流程进行实验:
实验 | 实验步骤 | 现象 | 结论 |
实验1 | 取少量碱石灰样品于烧杯中,加入足量的水,触摸烧杯外壁,充分搅拌后过滤,得到滤渣和滤液 | 温度 | 猜想Ⅲ正确 |
实验2 | 取少量上述滤渣于试管中,滴加过量 | 产生气泡,澄清石灰水 | |
实验3 | 取少量上述滤液于另一支试管中,先滴加酚酞溶液,再滴加过量氯化钙溶液 | 溶液先变成红色, |
【讨论分析】
(3)实验3是否可以先滴加过量氯化钙溶液,再滴入酚酞溶液
您最近一年使用:0次
【推荐1】某兴趣小组对镁条在空气中的变化进行如下实验。
【查阅资料】①MgO、Mg(OH)2均为白色固体;Mg2(OH)2CO3为黑色固体。
②部分物质的熔沸点。
【实验探究】用如图1所示进行实验(镁条固定在试管塞上),并进行了一周的观察。
(1)用化学方程式表示B中镁条不再光亮的原因:___________ 。
(2)D、E试管中有少量黑斑的原因是___________ 。
【实验验证】将F中镁条表面的黑色物质用小刀刮下,向其中加入稀硫酸有气泡产生。
(3)乙同学提出有气泡产生并不能说明黑色物质中有碳酸盐,原因是___________ 。
(4)要证明黑色固体中有碳酸盐,还需补充的实验为___________ 。
(5)根据上述实验,实验室保存镁条时最需要注意的是___________ 。
【拓展延伸】取0.56g去除表面物质的镁条,在空气中点燃得到0.29g固体,将所得产物按照图2所示进行实验,观察到湿润的红色石蕊试纸变蓝。___________ 。
(7)湿润的红色石蕊试纸变蓝说明镁条燃烧时空气中的___________ 参加了反应。
【查阅资料】①MgO、Mg(OH)2均为白色固体;Mg2(OH)2CO3为黑色固体。
②部分物质的熔沸点。
| Mg | MgO | |
| 熔点 | 651 | 2852 |
| 沸点 | 1170 | 3600 |

| 试管编号 | 实验现象 |
| A | 镁条表面无明显变化 |
| B | 镁条表面不再光亮 |
| C | 镁条表面不再光亮 |
| D | 第二天表面有少量黑斑,后不再增加 |
| E | 第二天表面有少量黑斑,后不再增加 |
| F | 第二天开始表面有黑斑产生,第7天时表面完全变黑 |
(2)D、E试管中有少量黑斑的原因是
【实验验证】将F中镁条表面的黑色物质用小刀刮下,向其中加入稀硫酸有气泡产生。
(3)乙同学提出有气泡产生并不能说明黑色物质中有碳酸盐,原因是
(4)要证明黑色固体中有碳酸盐,还需补充的实验为
(5)根据上述实验,实验室保存镁条时最需要注意的是
【拓展延伸】取0.56g去除表面物质的镁条,在空气中点燃得到0.29g固体,将所得产物按照图2所示进行实验,观察到湿润的红色石蕊试纸变蓝。

(7)湿润的红色石蕊试纸变蓝说明镁条燃烧时空气中的
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】学校化学实践小组的同学们准备在本校的劳动基地——蔬菜大棚里种植小红薯。蔬菜大棚的土质适合种植小红薯吗?同学们在老师的指导下,对土壤的酸碱度、酸碱度的成因、改良的方法等展开了项目化学习的探究。
任务一:测定土壤的酸碱度
(1)【进行实验】实践小组同学取蔬菜大棚里的少量土壤置于烧杯中,向其中加入适量蒸馏水,充分搅拌后静置。一段时间后,小组同学测定土壤酸碱度的操作为:在干燥、洁净的玻璃片上放一片pH试纸,______ 。把试纸显示的颜色与标准比色卡比较,读出pH=5。
【查阅资料】小红薯最适宜种植的土壤pH为6.5~7.5。
(2)【分析交流】该土地的土壤偏______ 性,不适合种植小红薯。
任务二:探究土壤酸碱度的成因
【调查咨询】同学们向蔬菜大棚的管理员咨询土壤酸碱度的成因,据管理员介绍,该土地之前施用过大量氯化铵化肥,土壤中可能有氯化铵残留。
【教师指导】氯化铵的水溶液呈酸性。
【猜想假设】该土壤中可能含有氯化铵。
(3)【进行实验】
(4)【反思评价】步骤②中发生反应的化学方程式为______ 。
任务三:选择土壤改良剂
【查阅资料】酸性土壤的改良可以施用生石灰、熟石灰、草木灰(主要成分为K2CO3)、贝壳灰(主要成分为CaCO3)等。
【进行实验】同学们取两份土壤样品各500g,分别加入0.2g不同的改良剂和1L左右的水,充分搅拌后静置,测上层清液的pH,得到下表结果。
【分析交流】
(5)用熟石灰改良此土壤时,需要注意的是______ (写一条)。
(6)用草木灰改良土壤的优点是______ (写一条)。
任务四:制作小红薯种植区域的标牌
(7)【成果交流】同学们按自己的选择改良了土壤的酸碱度,几周以后,同学们再次来到蔬菜大棚,在改良后的土壤中种植了小红薯,并在种植区域周边设立了小红薯的标牌,请你与同学们共同完成标牌的制作(如下图)。
任务一:测定土壤的酸碱度
(1)【进行实验】实践小组同学取蔬菜大棚里的少量土壤置于烧杯中,向其中加入适量蒸馏水,充分搅拌后静置。一段时间后,小组同学测定土壤酸碱度的操作为:在干燥、洁净的玻璃片上放一片pH试纸,
【查阅资料】小红薯最适宜种植的土壤pH为6.5~7.5。
(2)【分析交流】该土地的土壤偏
任务二:探究土壤酸碱度的成因
【调查咨询】同学们向蔬菜大棚的管理员咨询土壤酸碱度的成因,据管理员介绍,该土地之前施用过大量氯化铵化肥,土壤中可能有氯化铵残留。
【教师指导】氯化铵的水溶液呈酸性。
【猜想假设】该土壤中可能含有氯化铵。
(3)【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量土壤样品,向其中加入少量熟石灰,混合、研磨 | 土壤中含 有氯化铵 | |
| ②取少量任务一中的土壤样品浸出液,向其中滴加 | 产生白色沉淀 |
任务三:选择土壤改良剂
【查阅资料】酸性土壤的改良可以施用生石灰、熟石灰、草木灰(主要成分为K2CO3)、贝壳灰(主要成分为CaCO3)等。
【进行实验】同学们取两份土壤样品各500g,分别加入0.2g不同的改良剂和1L左右的水,充分搅拌后静置,测上层清液的pH,得到下表结果。
| 加入的改良剂 | 熟石灰 | 草木灰 |
| 测得的pH | 11 | 6 |
(5)用熟石灰改良此土壤时,需要注意的是
(6)用草木灰改良土壤的优点是
任务四:制作小红薯种植区域的标牌
(7)【成果交流】同学们按自己的选择改良了土壤的酸碱度,几周以后,同学们再次来到蔬菜大棚,在改良后的土壤中种植了小红薯,并在种植区域周边设立了小红薯的标牌,请你与同学们共同完成标牌的制作(如下图)。
| 小红薯 适宜土壤pH:6.5~7.5。 肥料需求:以 |
您最近一年使用:0次
【推荐3】沙尘暴是我国常见的自然现象。某校环境监测实践小组的同学们,对沙尘暴的成因、危害、成分以及对水资源的影响产生了浓厚的兴趣,在老师的指导下,开启了项目学习的探究之旅。
(1)任务一:分析沙尘暴的影响
当人暴露于沙尘天气中时,含有各种有毒的化学物质、病菌等的尘土可进入到口、鼻、眼、耳中引发各种疾病。我国黄土高原上的厚层黄土是千百万年以来,通过沙尘暴这一自然现象逐渐将其他地方的土壤转移到黄土高原处。黄土肥沃,是因为土壤中富含磷、钾、钙、硫等元素,在黄土上种植庄稼,还需施的肥料主要是______________________ 肥。
(2)任务二:探究沙尘暴的成分
【信息检索】我国西北地区,含有大量钠盐的干涸盐湖和盐碱地总面积约有 50 万平方公里,为沙尘暴的形成埋下隐患。
据此可以猜想:由此引发的沙尘暴中可能含有碳酸钠等碱性物质。
取少量盐碱地的土壤与蒸馏水按 1∶5 的质量比在烧杯中混合,充分搅拌后静置,取上层清液,用如下图装置完成如下实验。

反思:
Ⅰ.步骤①中发生反应的化学方程式为__________________ 。
Ⅱ.自然界的土壤中通常不含 NaOH,理由是__________________ 。
Ⅲ.若加入的 X 是氢氧化钙,则对本次探究的影响是__________________ 。
(3)任务三:沙尘暴对水质的影响
小组同学在老师的帮助下从某西北地区环保部门获得当地河流在沙尘暴发生前后几天河水的pH数据。
发生沙尘暴的日期是______ 。
(1)任务一:分析沙尘暴的影响
当人暴露于沙尘天气中时,含有各种有毒的化学物质、病菌等的尘土可进入到口、鼻、眼、耳中引发各种疾病。我国黄土高原上的厚层黄土是千百万年以来,通过沙尘暴这一自然现象逐渐将其他地方的土壤转移到黄土高原处。黄土肥沃,是因为土壤中富含磷、钾、钙、硫等元素,在黄土上种植庄稼,还需施的肥料主要是
(2)任务二:探究沙尘暴的成分
【信息检索】我国西北地区,含有大量钠盐的干涸盐湖和盐碱地总面积约有 50 万平方公里,为沙尘暴的形成埋下隐患。
据此可以猜想:由此引发的沙尘暴中可能含有碳酸钠等碱性物质。
取少量盐碱地的土壤与蒸馏水按 1∶5 的质量比在烧杯中混合,充分搅拌后静置,取上层清液,用如下图装置完成如下实验。
| 项目 | 实验步骤 | 实验现象 | 实验结论 |
| 方案 | ①挤压胶头滴管a,滴入 | 产生白色沉淀 | 沙尘暴中含有Na2CO3,不含NaOH |
| ②挤压胶头滴管b,滴入几滴酚酞溶液 | 酚酞溶液不变色 |

反思:
Ⅰ.步骤①中发生反应的化学方程式为
Ⅱ.自然界的土壤中通常不含 NaOH,理由是
Ⅲ.若加入的 X 是氢氧化钙,则对本次探究的影响是
(3)任务三:沙尘暴对水质的影响
小组同学在老师的帮助下从某西北地区环保部门获得当地河流在沙尘暴发生前后几天河水的pH数据。
| 测定时间 | 3 月 31 日 | 4 月 1 日 | 4 月 2 日 | 4 月 3 日 |
| pH | 7.73 | 8.05 | 7.78 | 7.76 |
发生沙尘暴的日期是
您最近一年使用:0次



