为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
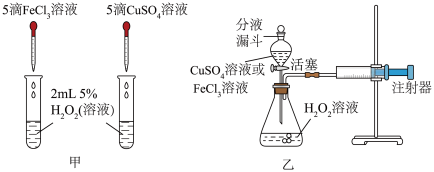
(1)请写出H2O2分解的化学方程式_______________ 。
【定性研究】(2)如图甲,可通过观察__________ 来定性比较两者的催化效果。
【定量研究】(3)要定量比较两者的催化效果,可测量生成等体积气体所需的____________ 。
【深入研究】(4)在CuSO4溶液中,究竟是哪种粒子起催化作用呢?
猜想1:铜离子(Cu2+)起催化作用;
猜想2:___________ 起催化作用;
猜想3:___________ 起催化作用;
(5)请设计实验,验证猜想1

(1)请写出H2O2分解的化学方程式
【定性研究】(2)如图甲,可通过观察
【定量研究】(3)要定量比较两者的催化效果,可测量生成等体积气体所需的
【深入研究】(4)在CuSO4溶液中,究竟是哪种粒子起催化作用呢?
猜想1:铜离子(Cu2+)起催化作用;
猜想2:
猜想3:
(5)请设计实验,验证猜想1
| 实验操作 | 实验现象及结论 |
更新时间:2018-06-01 19:12:26
|
相似题推荐
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某班化学兴趣小组同学探究“催化剂的种类对氯酸钾分解催化效果的影响”,设计了如下实验。
(1)实验数据记录如下:
①在相同条件下比较上述三组实验产生氧气的快慢,实验Ⅲ中x的值应为_______ 。
②写出氧化铁催化氯酸钾分解的文字表达式:_______ 。
③在相同温度下,本实验中测量氧气的体积可选用下列图中的_______ (填字母序号)。
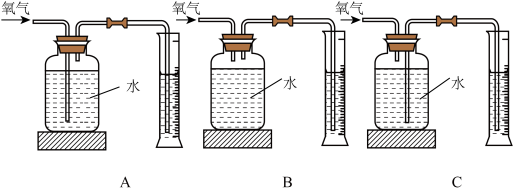
④若V1<V2,可得出的结论是_______ 。
(2)若要证明氧化铝和氧化铁是该反应的催化剂,还要验证它们在化学反应前后的质量和_______ 不变。
(3)小明想探究反应物与催化剂的质量比不同,催化效果是否不同。于是他调节氯酸钾和氧化铁的质量比制备氧气,整理数据绘制出如图。从图中得出氧化铁和氯酸钾的最佳质量比是_______ 。

(1)实验数据记录如下:
| 氯酸钾的质量/g | 催化剂种类 | 催化剂的质量/g | 相同时间内产生氧气的体积 | |
| Ⅰ | 3.0 | V | ||
| Ⅱ | 3.0 | 氧化铝 | 0.5 | V1 |
| Ⅲ | 3.0 | 氧化铁 | x | V2 |
②写出氧化铁催化氯酸钾分解的文字表达式:
③在相同温度下,本实验中测量氧气的体积可选用下列图中的

④若V1<V2,可得出的结论是
(2)若要证明氧化铝和氧化铁是该反应的催化剂,还要验证它们在化学反应前后的质量和
(3)小明想探究反应物与催化剂的质量比不同,催化效果是否不同。于是他调节氯酸钾和氧化铁的质量比制备氧气,整理数据绘制出如图。从图中得出氧化铁和氯酸钾的最佳质量比是

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验:
(1)请你帮小丽同学填写下表中未填完的空格。
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是_________ 。
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
①第一方面的实验操作中包含了两次称量,即在“实验三”开始前和结束后分别对二氧化锰的质量进行称量。其目的是_____________ 。
②第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。操作方法是在“实验三”结束后,倾倒掉反应后的液体,在剩余固体中重新加入过氧化氢溶液,有大量气泡产生。说明_________ 。
| 实验操作 | 实验现象 | 实验结论与总结 | ||
| 结论 | 总结 | |||
| 实验一 | 取5ml5%的过氧化氢溶液于试管中,伸入带火星的布条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应速率 | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气 | |
| 实验三 | 向盛有5mL5%的过氧化氢溶液中,加入 | 有大量气泡产生,并且 | 二氧化锰能加快过氧化氢的分解 | |
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
①第一方面的实验操作中包含了两次称量,即在“实验三”开始前和结束后分别对二氧化锰的质量进行称量。其目的是
②第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。操作方法是在“实验三”结束后,倾倒掉反应后的液体,在剩余固体中重新加入过氧化氢溶液,有大量气泡产生。说明
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】以下是王辉同学未完成的实验分析报告,请你帮助完成。
(一)探究影响化学反应快慢的一些因素的相关数据
(1)通过实验①和②对比可知,化学反应快慢与________________ 有关;
(2)通过实验②和③对比可知,化学反应快慢与________________ 有关;
(3)通过实验④和⑤对比可知,化学反应快慢与温度的关系是________ 。
(4)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是___________ 。
(二)继续检验催化剂二氧化锰的有关问题:
(1)实验②结束后,重新提纯残余固体,称量其质量是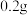 ,其目的是验证
,其目的是验证______ 。
(2)向提纯的固体中重新加入过氧化氢溶液,看到有大量气泡冒出,其目的是验证_________ 。
(一)探究影响化学反应快慢的一些因素的相关数据
| 实验序号 | 过氧化氢溶液浓度 | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ | 反应所需时间/s |
| ① | 5% | 12 | 20 | 0.4 | 125 | 3 |
| ② | 5% | 12 | 20 | 0.2 | 125 | 11 |
| ③ | 30% | 12 | 20 | 0.2 | 125 | 2 |
| ④ | 30% | 12 | 30 | 0 | 125 | 148 |
| ⑤ | 30% | 12 | 50 | 0 | 125 | 120 |
(2)通过实验②和③对比可知,化学反应快慢与
(3)通过实验④和⑤对比可知,化学反应快慢与温度的关系是
(4)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是
(二)继续检验催化剂二氧化锰的有关问题:
(1)实验②结束后,重新提纯残余固体,称量其质量是
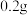 ,其目的是验证
,其目的是验证(2)向提纯的固体中重新加入过氧化氢溶液,看到有大量气泡冒出,其目的是验证
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】根据下列的实验装置图回答问题。

(1)装置Ⅰ在实验中可用于过氧化氢溶液制氧气,其反应的化学方程式为______________ 。
(2)在化学实验中,对装置稍加改装或采用不同的组合时,就能完成多种实验。如将装置Ⅱ改为Ⅳ后,可以顺利进行草酸受热扫解的实验。
草酸是一种有机物,常温时为一种无色透明的晶体,加热时易分解。草酸受热分解的化学方程式为:C2H2O2==H2O+CO2+CO
根据改进后图Ⅳ所示实验装置推测草酸还具有的物理性质为_______________ 。

(3)现将装置Ⅳ与装置Ⅲ相连,对草酸受热分解后所得产物的组成和性质进行探究。实验开始前E中左右液面在同一水平面上。
①装置Ⅲ中A可用于收集反应生成的水,还具有________ 的作用;
②实验过程中,D中一直无明显现象,E中球容器内液面________ (填“升高”、“降低”或“不变”)。

(1)装置Ⅰ在实验中可用于过氧化氢溶液制氧气,其反应的化学方程式为
(2)在化学实验中,对装置稍加改装或采用不同的组合时,就能完成多种实验。如将装置Ⅱ改为Ⅳ后,可以顺利进行草酸受热扫解的实验。
草酸是一种有机物,常温时为一种无色透明的晶体,加热时易分解。草酸受热分解的化学方程式为:C2H2O2==H2O+CO2+CO
根据改进后图Ⅳ所示实验装置推测草酸还具有的物理性质为

(3)现将装置Ⅳ与装置Ⅲ相连,对草酸受热分解后所得产物的组成和性质进行探究。实验开始前E中左右液面在同一水平面上。
①装置Ⅲ中A可用于收集反应生成的水,还具有
②实验过程中,D中一直无明显现象,E中球容器内液面
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】在二氧化锰的催化作用下,过氧化氢迅速分解生成氧气和水。哪些因素还影响着过氧化氢分解的速率?课外活动小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
请你设计:请选择以下实验仪器和用品完成探究实验二:
实验仪器、用品:试管、烧杯、热水、冷水、3%过氧化氢溶液、5%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
探究实验一:浓度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
| 1.取一支试管加入3~5mL浓度为1%的过氧化氢溶液,然后加入少量二氧化锰。 | 缓慢有少量气泡冒出 | |
| 2.另取一支试管加入3~5mL浓度为5%的过氧化氢溶液,然后加入少量二氧化锰。 | 迅速有大量气泡冒出 |
请你设计:请选择以下实验仪器和用品完成探究实验二:
实验仪器、用品:试管、烧杯、热水、冷水、3%过氧化氢溶液、5%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
| 实验步骤 | 现 象 | 结 论 |
| 相同条件下,温度越高,过氧化氢分解的速率越大 | ||
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。(实验装置如图所示,夹持仪器已略去)
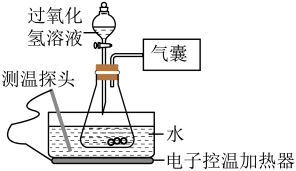
【猜想与假设】
影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂用量。
【实验记录】
同学们进行6组实验,实验记录如下:
【解释与结论】
(1)实验②中应加入过氧化氢溶液的体积x是________ mL。
(2)实验①-⑥可以通过测定__________ 来比较过氧化氢的分解速率。
A 相同时间内产生氧气的体积
B 产生相同体积的氧气所需时间
C 相同时间内产生氧气的质量
(3)得出“过氧化氢溶液的浓度越大分解速率越快”结论所依据的实验是____ (填序号)。
(4)通过实验①、②、④可得出的结论是_________ 。
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是________ (答一点即可)

【猜想与假设】
影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂用量。
【实验记录】
同学们进行6组实验,实验记录如下:
| 实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 过氧化氢溶液的 浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
| 过氧化氢溶液的 体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
| 水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
| 锥形瓶中的物质 | 0.1g MnO2 | 0.5g MnO2 | ||||
| 6min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(1)实验②中应加入过氧化氢溶液的体积x是
(2)实验①-⑥可以通过测定
A 相同时间内产生氧气的体积
B 产生相同体积的氧气所需时间
C 相同时间内产生氧气的质量
(3)得出“过氧化氢溶液的浓度越大分解速率越快”结论所依据的实验是
(4)通过实验①、②、④可得出的结论是
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验是进行科学探究的重要方式,也是学习化学的一个重要途径。
Ⅰ.探究燃烧条件

(1)如图甲,根据两支蜡烛的燃烧情况,说明可燃物燃烧的条件是_______ 。
(2)如图乙,装置中木屑燃烧,煤粉没有燃烧,说明可燃物燃烧的条件是_______ 。
Ⅱ.探究影响燃烧剧烈程度的因素
(3)实验甲中的反应现象为_______ 。
(4)比较实验甲和实验乙,产生不同现象的原因是_______ 。
(5)实验丙的产物与甲相同,写出发生反应的化学方程式_______ 。
(6)上述实验中,能说明“反应物与氧气接触的面积不同,现象不同”的是_______ (填编号)。
Ⅰ.探究燃烧条件

(1)如图甲,根据两支蜡烛的燃烧情况,说明可燃物燃烧的条件是
(2)如图乙,装置中木屑燃烧,煤粉没有燃烧,说明可燃物燃烧的条件是
Ⅱ.探究影响燃烧剧烈程度的因素
| 实验编号 | 可燃物 | 集气瓶中气体 | 反应现象 |
| 甲 | 细铁丝 | 氧气 | |
| 乙 | 细铁丝 | 空气 | 不燃烧 |
| 丙 | 铁粉 | 空气 | 剧烈燃烧、迸发出大量火星 |
(4)比较实验甲和实验乙,产生不同现象的原因是
(5)实验丙的产物与甲相同,写出发生反应的化学方程式
(6)上述实验中,能说明“反应物与氧气接触的面积不同,现象不同”的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】小红利用下图所示装置研究可燃物的燃烧条件。
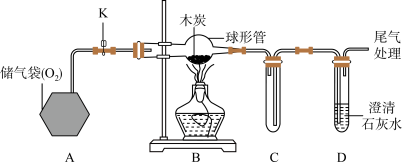
(1)实验时要先检查装置气密性,填装药品,并设法将整个装置充满氮气。若要求实验过程中不得拆、装仪器,请设计后续的实验步骤,并按要求填表。
通过该实验可得到的结论是__________ 。
(2)装置C在步骤②中的作用是__________ 。

(1)实验时要先检查装置气密性,填装药品,并设法将整个装置充满氮气。若要求实验过程中不得拆、装仪器,请设计后续的实验步骤,并按要求填表。
| 步骤 | 操作 | 现象 |
| 一 | 点燃酒精灯加热 | 无现象 |
| 二 | 盖灭酒精灯,待仪器恢复到常温 | / |
| 三 | 无现象 | |
| 四 | 点燃酒精灯加热,继续通氧气 |
(2)装置C在步骤②中的作用是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
【分析数据、得出结论】
(1)由实验__________ 与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是________ 。
(3)若Fe2O3是该反应的催化剂,请写出这个反应的符号表达式_________________________ 。
(4)如表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据。
①据如表可知二氧化锰与氯酸钾的质量比为¬¬_______________ 时,反应速率最快;
②通过分析可知,在化学反应中催化剂的用量__________ 越多越好。(填“是”或“不是”)
③二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的__________ ,所以反应速率受到影响。
【提出猜想】除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度 |
| ① | KClO3 | 580℃ |
| ② | KClO3、MnO2(质量比1:1) | 350℃ |
| ③ | KClO3、CuO(质量比l:1) | 370℃ |
| ④ | KClO3、Fe2O3(质量比1:1) | 390℃ |
【分析数据、得出结论】
(1)由实验
(2)实验所用的三种金属氧化物,催化效果最好的是
(3)若Fe2O3是该反应的催化剂,请写出这个反应的符号表达式
(4)如表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据。
| 二氧化锰与氯酸钾的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 |
| 生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 |
①据如表可知二氧化锰与氯酸钾的质量比为¬¬
②通过分析可知,在化学反应中催化剂的用量
③二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的
您最近一年使用:0次



