化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
[提出问题1] 该氢氧化钠溶液是否变质了呢?
[实验探究1]
[提出问题2] 该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想1:氢氧化钠溶液部分变质。 猜想2:氢氧化钠溶液全部变质。
[查阅资料] ⑴ 氯化钙溶液呈中性。
⑵ 氯化钙溶液能与碳酸钠溶液反应(方程式):________________________ 。
[实验探究2]
[实验结论] 该氢氧化钠溶液_______ (填“部分”或“全部”)变质。
[反思与评价] ⑴氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:_________ 。
⑵在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案________ (填“可行”或“不可行”)。
[理解与应用] 氢氧化钠溶液容易变质,必须密封保存。
[提出问题1] 该氢氧化钠溶液是否变质了呢?
[实验探究1]
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡。 | 氢氧化钠溶液一定变质了。 |
[提出问题2] 该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想1:氢氧化钠溶液部分变质。 猜想2:氢氧化钠溶液全部变质。
[查阅资料] ⑴ 氯化钙溶液呈中性。
⑵ 氯化钙溶液能与碳酸钠溶液反应(方程式):
[实验探究2]
| 实验步骤 | 实验现象 | 实验结论 |
| ⑴取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 | 有 | 说明原溶液中一定有碳酸钠。 |
| ⑵取步骤⑴试管中的少量上层清液,滴加酚酞溶液。 | 说明原溶液中一定有 |
[实验结论] 该氢氧化钠溶液
[反思与评价] ⑴氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:
⑵在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案
[理解与应用] 氢氧化钠溶液容易变质,必须密封保存。
更新时间:2018-05-31 11:35:36
|
相似题推荐
科学探究题
|
较难
(0.4)
解题方法
【推荐1】小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。小刚叫来小军和小红,共同探究这种白色粉末的成分。
【提出问题】白色粉末的成分是什么?
【进行猜想】他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;②可能是Na2CO3;③可能是NaOH与Na2CO3 的混合物。
【设计实验】
(1)为了验证猜想,小军做了下面的实验:
【反思改进】
(2)小红认为小军实验2不能得出猜想③正确,请说明理由__________________
(3)小刚认为小红说的对,为了验证猜想③,设计以下实验:
请你写出实验Ⅰ中反应的化学方程式____________ 。
【反思应用】氢氧化钠易潮解,且容易与空气中CO2发生反应,所以氢氧化钠固体应该_________ 保存。
【提出问题】白色粉末的成分是什么?
【进行猜想】他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;②可能是Na2CO3;③可能是NaOH与Na2CO3 的混合物。
【设计实验】
(1)为了验证猜想,小军做了下面的实验:
| 序号 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量白色粉末,滴加足量稀盐酸 | 气体生成 | 猜想 |
| 2 | 取少量白色粉末溶于水,向所得溶液中滴加无色酚酞溶液 | 猜想③正确 |
【反思改进】
(2)小红认为小军实验2不能得出猜想③正确,请说明理由
(3)小刚认为小红说的对,为了验证猜想③,设计以下实验:
| 序号 | 实验操作 | 实验现象 | 结论 |
| Ⅰ | 取少量白色粉末溶于水,向所得溶液中滴加过量 | 产生白色沉淀 | 猜想③正确 |
| Ⅱ | 取实验Ⅰ的上清液,向溶液中滴加FeCl3溶液 | |
请你写出实验Ⅰ中反应的化学方程式
【反思应用】氢氧化钠易潮解,且容易与空气中CO2发生反应,所以氢氧化钠固体应该
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某化学课外活动小组在实验室配制石灰水时,因发现烧杯底部有固体未溶解,对熟石灰样品的主要成分进行了探究。请你参与讨论并完成实验报告。
【提出问题】针对该熟石灰样品的成分,同学们展开了讨论,小明认为溶解后剩余固体为变质后的难溶性物质。小华同学不同意他的判断,你认为小华同学的理由是_________ 。
【进行猜想】猜想一:熟石灰样品成分是Ca(OH)2;
猜想二:熟石灰样品成分是CaCO3;
猜想三:你认为熟石灰样品成分还可能是_________ 。
【实验与结论】请你通过实验验证你的猜想:
【拓展与应用】实验小组想测定样品中Ca(OH)2的质量分数:
同学们称取上述0.5g样品,加足量水搅拌使之充分溶解后过滤,得滤液和滤渣,向滤液中逐滴滴加1%的稀盐酸,并且不断搅拌。
(1)甲组同学实验数据记录见下表。(提示:氯化钙溶液呈中性)
则样品中Ca(OH)2的质量分数是________ 。
(2)乙组同学由计算机描绘出了整个实验过程中溶液pH的变化图象如图。则图中c点溶液中含有的溶质有_____ (填化学式),乙组同学要计算出样品中氢氧化钙的质量分数,除了要用到已有数据外,你认为还需要的数据是_________ 。

(3)丙组同学经过讨论,认为只要准确的称量测定实验过程中_______ 的质量,不用化学方程式计算也能得到样品中Ca(OH)2的质量分数。
【提出问题】针对该熟石灰样品的成分,同学们展开了讨论,小明认为溶解后剩余固体为变质后的难溶性物质。小华同学不同意他的判断,你认为小华同学的理由是
【进行猜想】猜想一:熟石灰样品成分是Ca(OH)2;
猜想二:熟石灰样品成分是CaCO3;
猜想三:你认为熟石灰样品成分还可能是
【实验与结论】请你通过实验验证你的猜想:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取小烧杯中的物质进行过滤,得到固体和液体。 |  |  |
| ②向①所得液体中加入适量 | 溶液变红 | 猜想三正确 |
| ③向①所得固体中加入适量稀盐酸。 |
【拓展与应用】实验小组想测定样品中Ca(OH)2的质量分数:
同学们称取上述0.5g样品,加足量水搅拌使之充分溶解后过滤,得滤液和滤渣,向滤液中逐滴滴加1%的稀盐酸,并且不断搅拌。
(1)甲组同学实验数据记录见下表。(提示:氯化钙溶液呈中性)
| 加入盐酸溶液的质量/g | 0 | 25 | 36.5 | 50 |
| 溶液的pH | 12 | 11 | 7 | 2 |
则样品中Ca(OH)2的质量分数是
(2)乙组同学由计算机描绘出了整个实验过程中溶液pH的变化图象如图。则图中c点溶液中含有的溶质有

(3)丙组同学经过讨论,认为只要准确的称量测定实验过程中
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】氢氧化钠是一种重要的化工原料,但在空气中很容易变质。
(1)在实验室开放日活动中,某化学兴趣小组探究一瓶氢氧化钠溶液是否变质,进行以下探究:
①氢氧化钠溶液变质的原因是_____ (用化学方程式表示)。
②小建取适量样品于试管中,向其中滴加几滴酚酞溶液,观察到溶液变红色,由此判断这瓶氢氧化钠溶液未变质。你认为小建的结论是否成立?_____ (选填“成立”或“不成立”),理由是_____ 。
③小齐取适量样品于试管中,向其中加入足量的稀盐酸,观察到的现象是_____ ,说明这瓶氢氧化钠溶液已变质。
④为进一步探究该瓶氢氧化钠溶液是部分变质还是全部变质,小思设计了以下实验方案:
(2)实验室用50 g溶质质量分数为18. 25%的稀盐酸与足量碳酸钙反应制取二氧化碳。请计算可制得二氧化碳的质量_____ 。
(1)在实验室开放日活动中,某化学兴趣小组探究一瓶氢氧化钠溶液是否变质,进行以下探究:
①氢氧化钠溶液变质的原因是
②小建取适量样品于试管中,向其中滴加几滴酚酞溶液,观察到溶液变红色,由此判断这瓶氢氧化钠溶液未变质。你认为小建的结论是否成立?
③小齐取适量样品于试管中,向其中加入足量的稀盐酸,观察到的现象是
④为进一步探究该瓶氢氧化钠溶液是部分变质还是全部变质,小思设计了以下实验方案:
| 操作步骤 | 实验现象 | 结论 |
| a.取适量样品溶液于试管中,滴加足量的氯化钡溶液,过滤 | ||
| b.向滤液中滴加适量 | 溶液变红 |
(2)实验室用50 g溶质质量分数为18. 25%的稀盐酸与足量碳酸钙反应制取二氧化碳。请计算可制得二氧化碳的质量
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐1】为探究Ca(OH)2的化学性质,某小组进行了 A、B 两个实验。

将两支试管中的上层废液同时倒入一洁净的烧杯中,发现烧杯中有气泡产生。请分析最终烧杯中成份:
假设1: NaCl、CaCl2、HCl
假设2: NaCl、NaOH、Na2CO3;
假设 3:______________ ;
【讨论】你认为上述假设中__________ 一定不合理;理由是 _________ 。
【实验】某同学通过以下实验方案及现象证明假设 1 成立,请补充完成下表实验。

将两支试管中的上层废液同时倒入一洁净的烧杯中,发现烧杯中有气泡产生。请分析最终烧杯中成份:
假设1: NaCl、CaCl2、HCl
假设2: NaCl、NaOH、Na2CO3;
假设 3:
【讨论】你认为上述假设中
【实验】某同学通过以下实验方案及现象证明假设 1 成立,请补充完成下表实验。
| 实验步骤 | 实验现象 | 实验结论 |
| 取 烧 杯 中 少 量 液 体 于 试 管中,滴入 | 假设 1 正确 |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】某化学兴趣小组进行以下实验:在室温为 15℃时,同学们将 10g 氢氧化钠固体完全溶解于 80g 水中,冷却至室温后匀速的通入二氧化碳气体。同时用传感器测定溶液的 pH 及温度的变化,用数据采集器记录并绘制图像如图 2 和图 3 所示。
【查阅资料】
①碳酸氢钠和碳酸钠的溶解度表(一个标准大气压下)(部分)
②向碳酸钠溶液中通入二氧化碳能化合生成碳酸氢钠。
【进行实验】

(1)图 1 所示实验中,用“分液漏斗”而不用“长颈漏斗”的原因是_____ ;
(2)通过图像分析,小苏打溶液是显_____ (填“酸性”、“中性”或“碱性”)。
(3)为了确定M 处溶液的成分,同学们进行了如下实验:
【反思与评价】
(4)为确定 M 处溶液的成分,(3)中步骤①中加过量试剂的目的是_____ ,步骤①②能否颠倒?_____ (填“能”或“否”)。
【注意:若答对第(5)、(6)小题奖励 4 分,化学试卷总分不超过 60 分。】

【拓展延伸】
(5)实验过程中,同学们发现 18min 后溶液的 pH 不再变化, 则此时烧杯中就可能观察到的现象有_____ 。
(6)图 2 中,BC 段发生反应的化学方程式为_____ 。图 3 中,DE 段温度变化的原因_____ 。
【查阅资料】
①碳酸氢钠和碳酸钠的溶解度表(一个标准大气压下)(部分)
| 温度/℃ | 0 | 15 | 20 | 30 |
| 碳酸氢钠的溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 |
| 碳酸钠的溶解度/g | 7.1 | 13.25 | 21.8 | 39.7 |
【进行实验】

(1)图 1 所示实验中,用“分液漏斗”而不用“长颈漏斗”的原因是
(2)通过图像分析,小苏打溶液是显
(3)为了确定M 处溶液的成分,同学们进行了如下实验:
| 实验步骤 | 加入试剂 | 实验现象 | 初步实验结论 |
| ① | 加入过量的 | 产生白色沉淀 | 含有 |
| ② | 滴入 | 溶液变红 |
(4)为确定 M 处溶液的成分,(3)中步骤①中加过量试剂的目的是
【注意:若答对第(5)、(6)小题奖励 4 分,化学试卷总分不超过 60 分。】

【拓展延伸】
(5)实验过程中,同学们发现 18min 后溶液的 pH 不再变化, 则此时烧杯中就可能观察到的现象有
(6)图 2 中,BC 段发生反应的化学方程式为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
解题方法
【推荐3】某兴趣小组的同学在老师的指导下,对一瓶没有塞橡皮塞的氢氧化钙溶液进行探究,请你一起参与.
【提出问题】该氢氧化钙溶液是否全部变质?
【猜想与假设】
猜想①:氢氧化钙溶液可能全部变质,变成碳酸钙.
猜想②:氢氧化钙溶液可能部分变质,其成分是________ .
【实验探究】
【反思拓展】
(1)氢氧化钙露置于空气中容易变质,原因是___________ (用化学方程式表示).
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是__________ .
【提出问题】该氢氧化钙溶液是否全部变质?
【猜想与假设】
猜想①:氢氧化钙溶液可能全部变质,变成碳酸钙.
猜想②:氢氧化钙溶液可能部分变质,其成分是
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取样于试管中,滴加稀盐酸 | 有 | 原溶液里一定有碳酸钙 |
| (2)另取样于试管中,滴加酚酞试液 | 溶液成红色 | 原溶液一定有 |
【反思拓展】
(1)氢氧化钙露置于空气中容易变质,原因是
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】氢氧化钠是重要的工业原料,也是实验室的常用药品。小明和小芳做了如下探究:
(1)小明查阅资料得知,氢氧化钠溶液露置在空气中容易变质,其变质的化学方程式为______ 。
(2)小明向氢氧化钠溶液中加入稀硫酸,对反应后废液的溶质进行了如下探究:
【提出问题】氢氧化钠溶液和稀硫酸反应后,溶质是什么?
【查阅资料】硫酸钠溶液呈中性
【猜想假设】猜想 I、硫酸钠和氢氧化钠;猜想Ⅱ、硫酸钠和硫酸;猜想Ⅲ、______
【设计实验】
【反思与评价】小芳认为实验操作②得出的结论不成立。为了证明猜想Ⅱ成立,可以向废液中分别加入少量的以下试剂______ 。
A 氧化铜粉末 B 氢氧化钡溶液 C 碳酸氢钠溶液 D 锌粒
(1)小明查阅资料得知,氢氧化钠溶液露置在空气中容易变质,其变质的化学方程式为
(2)小明向氢氧化钠溶液中加入稀硫酸,对反应后废液的溶质进行了如下探究:
【提出问题】氢氧化钠溶液和稀硫酸反应后,溶质是什么?
【查阅资料】硫酸钠溶液呈中性
【猜想假设】猜想 I、硫酸钠和氢氧化钠;猜想Ⅱ、硫酸钠和硫酸;猜想Ⅲ、
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量废液于试管中,滴入几滴酚酞溶液 | 溶液无明显变化 | 猜想 Ⅰ 不成立 |
| ②另取少量废液于试管中,滴入几滴氯化钡溶液 | 猜想Ⅱ成立 |
【反思与评价】小芳认为实验操作②得出的结论不成立。为了证明猜想Ⅱ成立,可以向废液中分别加入少量的以下试剂
A 氧化铜粉末 B 氢氧化钡溶液 C 碳酸氢钠溶液 D 锌粒
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】实验课上学习小组的同学用碳酸钠溶液鉴别失去标签的稀硫酸、氢氧化钠溶液和氯化钡溶液。请你参与其中探究并填空:
(一)鉴别三种溶液
【进行实验】
(二)探究废液的成分
上述实验结束后,该组同学将A、B、C三支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行过滤,得到滤液①,几位同学对滤液①的成分又进行了探究。

【提出问题】滤液中除水外还含有哪些物质?
【猜想】小明同学从微粒角度分析,认为滤液中含有 Na+、Ba2+、H+、CO32-、Cl-、OH-、SO42-七种离子。你认为最多可能含有_______________ 离子(填离子符号)。
【讨论】你认为小明同学的猜想合理吗?请说明理由。_____________ 。
【进行实验】
为确定滤液①的成分,同学们进一步做了如下实验探究:
【实验结论】同学们通过分析推理,得出结论:滤液①中共含有______ 种溶质。
【实验反思】a.向滤液①中加入足量 的氯化钡溶液的目的是_______________ ;
b.从微粒角度思考滤液成分时,首先在分析可能存在的离子基础上,再考虑离子能否共存,即离子间是否能结合为_______________ 。
(一)鉴别三种溶液
【进行实验】
| 实验操作 | 实验现象 | 实验结论 | |
| (1) | 分别用A、B、C三支试管 取三种溶液各少量,然后再 各加入一定量的碳酸钠溶液 | A中出现白色沉淀 B中 C中 | A中的原溶液是氯化钡溶液 B中的原溶液是稀硫酸 C中的原溶液是氢氧化钠溶液 |
(二)探究废液的成分
上述实验结束后,该组同学将A、B、C三支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行过滤,得到滤液①,几位同学对滤液①的成分又进行了探究。

【提出问题】滤液中除水外还含有哪些物质?
【猜想】小明同学从微粒角度分析,认为滤液中含有 Na+、Ba2+、H+、CO32-、Cl-、OH-、SO42-七种离子。你认为最多可能含有
【讨论】你认为小明同学的猜想合理吗?请说明理由。
【进行实验】
为确定滤液①的成分,同学们进一步做了如下实验探究:
| 实验操作 | 实验现象 | 实验分析 | |
| (2) | 取少量滤液①于试管中,向其中加入足量的氯化钡溶液;过滤,得沉淀和滤液②,向沉淀中加入足量稀硝酸。 | 产生白色沉淀 白色沉淀部分消失 | 根据实验现象可知,滤液①中含有 |
| (3) | 取少量滤液②于试管中, | 根据实验现象可知,滤液②中含有氢氧化钠 |
【实验结论】同学们通过分析推理,得出结论:滤液①中共含有
【实验反思】a.向滤液①中加入
b.从微粒角度思考滤液成分时,首先在分析可能存在的离子基础上,再考虑离子能否共存,即离子间是否能结合为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】工业废料石膏(CaSO4·2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、 电石(化学名称为碳化钙)等,某化学兴趣小组展开了如下系列研究。
一、高纯 CaO 的制备
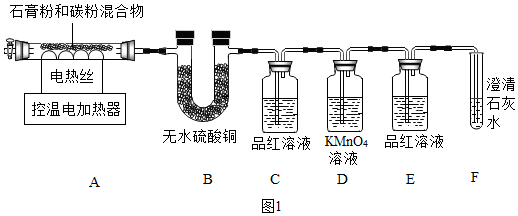
【资料一】 I.石膏(CaSO4·2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。 II.SO2 能使品红溶液褪色,也能使澄清石灰水变浑浊。甲同学用如图1 装置制备 CaO,并验证石膏与焦炭高温反应的其他产物。实验过程中发现:B 中无水硫酸铜变蓝,证明有 H2O 生成;C 中产生品红溶液褪色现象证 明有 SO2 生成;装置_________ 中无明显变化和装置 F 中______ 现象证明有 CO2 生成。
二、硫酸钾和电石的制备
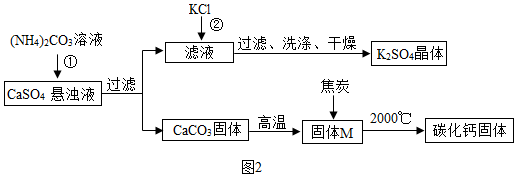
(1)证明固体 M 中不含 CaCO3 的方法是_____________ (写出实验的方法、现象)
(2)反应②的化学方程式为(NH4)2SO4+2KCl=K2SO4↓+2NH4Cl。
三、假设上述流程中制得的碳化钙(化学式为 CaCx)固体中只含杂质 CaO。乙小组同学为 测定 CaCx 中 x 的值进行如下实验。
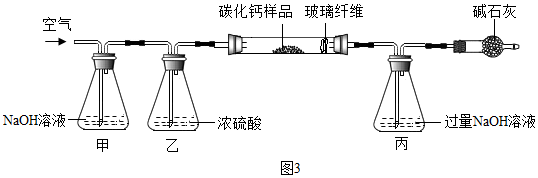
【资料三】CaCx 在空气中灼烧生成 CaO 和 CO2。Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 步骤一:称取 3.76g 样品于图 3 所示石英管中(测定装置图如图 3,夹持及加热装置省略), 反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气。测得丙溶 液的质量比反应前增重了 4.4g。(玻璃纤维可防止固体粉末进入导管) 步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、 干燥等操作得到碳酸钙固体 6 克。试回答下列问题:
(1)装置甲的作用是_______ 。反应完全后继续缓缓通入空气的目的是_____________ 。
(2)根据步骤一、二计算该样品中钙、碳、氧的质量比为_____ 。计算确定 CaCx的化学式_____ 。
(3)若碳酸钙未能完全干燥,则会导致 CaCx中的x的值______________ (填“偏大”、“偏小”、 “无影响”)。
一、高纯 CaO 的制备
【资料一】 I.石膏(CaSO4·2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。 II.SO2 能使品红溶液褪色,也能使澄清石灰水变浑浊。甲同学用如图1 装置制备 CaO,并验证石膏与焦炭高温反应的其他产物。实验过程中发现:B 中无水硫酸铜变蓝,证明有 H2O 生成;C 中产生品红溶液褪色现象证 明有 SO2 生成;装置

二、硫酸钾和电石的制备

(1)证明固体 M 中不含 CaCO3 的方法是
(2)反应②的化学方程式为(NH4)2SO4+2KCl=K2SO4↓+2NH4Cl。
三、假设上述流程中制得的碳化钙(化学式为 CaCx)固体中只含杂质 CaO。乙小组同学为 测定 CaCx 中 x 的值进行如下实验。

【资料三】CaCx 在空气中灼烧生成 CaO 和 CO2。Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 步骤一:称取 3.76g 样品于图 3 所示石英管中(测定装置图如图 3,夹持及加热装置省略), 反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气。测得丙溶 液的质量比反应前增重了 4.4g。(玻璃纤维可防止固体粉末进入导管) 步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、 干燥等操作得到碳酸钙固体 6 克。试回答下列问题:
(1)装置甲的作用是
(2)根据步骤一、二计算该样品中钙、碳、氧的质量比为
(3)若碳酸钙未能完全干燥,则会导致 CaCx中的x的值
您最近一年使用:0次



