今年“3·15”晚会对日常生活中的一些谣言进行了破解。
(1)专家批驳了“可燃面条是问题食品”的谣言。面条由面粉制得。面粉不仅能燃烧,而且分散在空气中遇明火还可能发生爆炸。
①根据面粉能燃烧的事实,推知面粉具有__________ ;
②面粉厂应采取的安全措施是_____________________________________ (写一条即可)。
(2)科研人员模拟人体内部环境,使用西红柿和蟹肉进行实验,发现蟹肉中微量的有机砷(C3H11AsO2)没有转化为有毒的砒霜(As2O3),证实“食物相克:西红柿和螃蟹一起吃会产生砒霜”是谣言。
①在西红柿和蟹肉中,富含蛋白质的是__________ ;
②若有机砷转化为砒霜,该转化属于__________ (填“物理变化”或“化学变化”)。
③As2O3中砷元素的质量分数__________ (列计算式即可)。
(1)专家批驳了“可燃面条是问题食品”的谣言。面条由面粉制得。面粉不仅能燃烧,而且分散在空气中遇明火还可能发生爆炸。
①根据面粉能燃烧的事实,推知面粉具有
②面粉厂应采取的安全措施是
(2)科研人员模拟人体内部环境,使用西红柿和蟹肉进行实验,发现蟹肉中微量的有机砷(C3H11AsO2)没有转化为有毒的砒霜(As2O3),证实“食物相克:西红柿和螃蟹一起吃会产生砒霜”是谣言。
①在西红柿和蟹肉中,富含蛋白质的是
②若有机砷转化为砒霜,该转化属于
③As2O3中砷元素的质量分数
2018·福建·中考真题 查看更多[4]
福建省2018年中考化学试题2020年6月辽宁省本溪市中考二模化学试题福建省龙岩市新罗区龙岩市高级中学2021-2022学年九年级下学期月考化学试题(已下线)专题12 计算题-5年(2018-2022)中考1年模拟化学分项汇编(福建专用)
更新时间:2018-06-25 02:21:01
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】为了测定石灰石中碳酸钙的质量分数,课外实验小组的的同学做了以下实验。
(石灰石的主要成分为碳酸钙,其它成分不溶于水,也不与稀盐酸反应)
步骤1:取块状石灰石,将其研磨成粉末;
步骤2:用电子天平称取石灰石粉末20.0g于烧杯中;
步骤3:向烧杯中不断加入稀盐酸,搅拌,直到不再产生气泡;
步骤4:将烧杯中的残留物过滤、洗涤、干燥(同滤纸一起干燥);
步骤5:称得反应后滤渣的质量为5.0g。
(1)“步骤1”中将石灰石研磨成粉末,该过程中发生的是___________ (填“物理”或“化学”)变化。
(2)石灰石中碳酸钙的质量分数为___________ 。
(3)“步骤4”中若不将滤渣干燥,实验测得碳酸钙的质量分数结果将___________ (填“偏大”、“偏小”或“无影响”)。
(4)计算反应中生成CO2的质量。(写出计算过程)
(石灰石的主要成分为碳酸钙,其它成分不溶于水,也不与稀盐酸反应)
步骤1:取块状石灰石,将其研磨成粉末;
步骤2:用电子天平称取石灰石粉末20.0g于烧杯中;
步骤3:向烧杯中不断加入稀盐酸,搅拌,直到不再产生气泡;
步骤4:将烧杯中的残留物过滤、洗涤、干燥(同滤纸一起干燥);
步骤5:称得反应后滤渣的质量为5.0g。
(1)“步骤1”中将石灰石研磨成粉末,该过程中发生的是
(2)石灰石中碳酸钙的质量分数为
(3)“步骤4”中若不将滤渣干燥,实验测得碳酸钙的质量分数结果将
(4)计算反应中生成CO2的质量。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】为了测定石灰石中碳酸钙的质量分数,课外实验小组的的同学做了以下实验。
(石灰石的主要成分为碳酸钙,其它成分不溶于水,也不与稀盐酸反应)
步骤1:取块状石灰石,将其研磨成粉末;
步骤2:用电子天平称取石灰石粉末20.0g 于烧杯中;
步骤3:向烧杯中不断加入稀盐酸,搅拌,直到不再产生气泡;
步骤4:将烧杯中的残留物过滤、洗涤、干燥(同滤纸一起干燥);
步骤5:主要操作如下图。

(1)“步骤1”中将石灰石研磨成粉末,该过程中发生的是_____ ( 填“物理”或“化学”)变化。
(2)石灰石中碳酸钙的质量分数为______ 。
(3)“步骤4”中若不将滤渣干燥,实验测得碳酸钙的质量分数结果将______ (填“偏大”、“偏小”或“无影响”)。
(4)“步骤3”中发生的反应为CaCO3+2HCl=CaCl2+H2O+CO2 。计算反应中生成CO2的质量。(写出计算过程)
。计算反应中生成CO2的质量。(写出计算过程)
(石灰石的主要成分为碳酸钙,其它成分不溶于水,也不与稀盐酸反应)
步骤1:取块状石灰石,将其研磨成粉末;
步骤2:用电子天平称取石灰石粉末20.0g 于烧杯中;
步骤3:向烧杯中不断加入稀盐酸,搅拌,直到不再产生气泡;
步骤4:将烧杯中的残留物过滤、洗涤、干燥(同滤纸一起干燥);
步骤5:主要操作如下图。

(1)“步骤1”中将石灰石研磨成粉末,该过程中发生的是
(2)石灰石中碳酸钙的质量分数为
(3)“步骤4”中若不将滤渣干燥,实验测得碳酸钙的质量分数结果将
(4)“步骤3”中发生的反应为CaCO3+2HCl=CaCl2+H2O+CO2
 。计算反应中生成CO2的质量。(写出计算过程)
。计算反应中生成CO2的质量。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】《梦溪笔谈》是宋代科学巨著。其中记载:“信州铅山县有苦泉,煮之则得胆矾。熬胆矾铁金,久之亦化为铜。”其中涉及的化学反应是: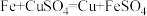 ,回答下列问题
,回答下列问题
(1)胆矾的分子式为CuSO4·5H2O,其元素组成确定,可以认为是纯净物,据此分析:
I、胆矾受热分解生成硫酸铜和水的过程是______ 变化(选填“物理”或“化学”);
Ⅱ、25克胆矾溶于水中形成的1000克溶液中溶质CuSO4的质量分数为______ 。
(2)现有熬胆矾铁釜50 kg,经检测其中含Cu 8 kg。试将求铁釜最初质量的计算过程补充完整。
解:设反应生成的铁的质量为x,
找出对应关系
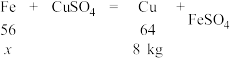
列出比例式______
求解x=______ kg
这件铁釜的最初质量是______ (列式并计算)
答:(略)。
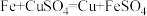 ,回答下列问题
,回答下列问题(1)胆矾的分子式为CuSO4·5H2O,其元素组成确定,可以认为是纯净物,据此分析:
I、胆矾受热分解生成硫酸铜和水的过程是
Ⅱ、25克胆矾溶于水中形成的1000克溶液中溶质CuSO4的质量分数为
(2)现有熬胆矾铁釜50 kg,经检测其中含Cu 8 kg。试将求铁釜最初质量的计算过程补充完整。
解:设反应生成的铁的质量为x,
找出对应关系
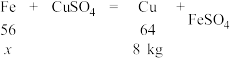
列出比例式
求解x=
这件铁釜的最初质量是
答:(略)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】波尔多液是一种运用广泛的农药,由熟石灰和硫酸铜配制而成。某工厂用以下反应:2Cu+O2+2H2SO4=2CuSO4+2H2O 来生产硫酸铜,若要制得 40kg 硫酸铜。试计算:
(1)硫酸铜中铜元素质量分数是_____ 。
(2)若恰好消耗稀硫酸的质量是 200kg,则该稀硫酸溶质的质量分数是多少_____ ?
(1)硫酸铜中铜元素质量分数是
(2)若恰好消耗稀硫酸的质量是 200kg,则该稀硫酸溶质的质量分数是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】欧盟报告称草甘膦不构成致癌风险,业界再“掐架”,该结果并不具有强制力,将不影响草甘膦的使用,已知草甘膦的化学式为C3H8NO5P。通过计算回答:
(1)草甘膦____(填“属于”或“不属于”)氧化物。一个草甘膦分子中含有的原子个数为____。
(2)草甘膦中碳元素与氧元素的质量比为_______。
(3)草甘膦中磷元素的质量分数为_______。(精确到0.1%)
(4)33.8g草甘膦中含有多少克磷元素?(要求写出计算步骤,精确到小数点后一位)
(1)草甘膦____(填“属于”或“不属于”)氧化物。一个草甘膦分子中含有的原子个数为____。
(2)草甘膦中碳元素与氧元素的质量比为_______。
(3)草甘膦中磷元素的质量分数为_______。(精确到0.1%)
(4)33.8g草甘膦中含有多少克磷元素?(要求写出计算步骤,精确到小数点后一位)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】农业生产中常使用如下化肥:尿素【CO(NH2)2】和碳酸氢铵(NH4HCO3)。
(1)碳酸氢铵中氢元素和氧元素的质量比为_____________ 。
(2)现有一尿素样品,测得其中氮元素的质量分数为43.5%,则该尿素样品是__________ (填 “纯净物”或“混合物”)。
(3)碳酸氢铵能分解产生氨气(NH3)、二氧化碳和水。反应前后元素的种类和质量都不变,一定质量的碳酸氢铵固体放置一段时间后减少7.9g,则产生氨气的质量为____ g。
(1)碳酸氢铵中氢元素和氧元素的质量比为
(2)现有一尿素样品,测得其中氮元素的质量分数为43.5%,则该尿素样品是
(3)碳酸氢铵能分解产生氨气(NH3)、二氧化碳和水。反应前后元素的种类和质量都不变,一定质量的碳酸氢铵固体放置一段时间后减少7.9g,则产生氨气的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】年初爆发的新冠肺炎,让很多人措手不及,后来专家说75%酒精能有效的预防病毒,但是消灭不了病毒,医学上酒精消毒是让细菌的胞膜脱水死亡,消灭的是细菌,而病毒是没有胞膜的,蛋白质变性需要理化干预,比如说高温可以把鸡蛋煮熟就是最简单的变性
(1)请写出酒精的化学式
(2)既然酒精消灭不了病毒,那聪明的你有什么办法消灭病毒吗,并写出他说物理变化还是化学变化
(3)某人有500g质量分数为99%的酒精,现在需要把它配成质量分数为75%的酒精,需要加多少水。
(1)请写出酒精的化学式
(2)既然酒精消灭不了病毒,那聪明的你有什么办法消灭病毒吗,并写出他说物理变化还是化学变化
(3)某人有500g质量分数为99%的酒精,现在需要把它配成质量分数为75%的酒精,需要加多少水。
您最近一年使用:0次
【推荐2】安吉白茶富含人体所需18种氨基酸,其中茶氨酸(C7H14N2O3)能增强血液免疫细胞干扰素分泌量、保护神经细胞、提高人体的抵抗力、记忆力、降低血压、减肥等功效。
(1)氨基酸主要用于合成人体必需的营养物质______ 。
(2)从上述信息可以看出,茶氨酸主要对人体的血液循环系统和______ 系统产生影响。
(3)348克茶氨酸与多少克尿素CO(NH2)2)中的氮元素质量相等?
(1)氨基酸主要用于合成人体必需的营养物质
(2)从上述信息可以看出,茶氨酸主要对人体的血液循环系统和
(3)348克茶氨酸与多少克尿素CO(NH2)2)中的氮元素质量相等?
您最近一年使用:0次




