t1℃时,将等质量的硝酸钾和氯化钾分别放入盛有100g水的烧杯中,充分溶解后的现象如图Ⅰ所示,升温到t2℃后的现象如图Ⅱ所示。结合硝酸钾和氯化钾的溶解度曲线回答问题。

(1)甲烧杯中溶解的物质是___________ 。
(2)t1℃时,甲、乙烧杯中溶液的溶质质量分数关系是甲______ (填“>”“=”或“<”)乙。
(3)t2℃时,乙烧杯中的溶液是___________ (填“饱和溶液”“不饱和溶液”或“不能确定”)。
(4)若使t1℃时乙烧杯中未溶的固体继续溶解,除升温外还可以采用的方法是__________ 。

(1)甲烧杯中溶解的物质是
(2)t1℃时,甲、乙烧杯中溶液的溶质质量分数关系是甲
(3)t2℃时,乙烧杯中的溶液是
(4)若使t1℃时乙烧杯中未溶的固体继续溶解,除升温外还可以采用的方法是
更新时间:2018-07-09 11:26:48
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
真题
名校
【推荐1】向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示。

(1)烧杯中的溶液一定属于饱和溶液的是________ (填序号);
(2)图二能表示NaNO3溶解度曲线的是________ (填“甲”或“乙”);
(3)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的_____ (填序号)。
A.甲、乙都是饱和溶液
B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙
D.溶质质量分数:甲>乙

(1)烧杯中的溶液一定属于饱和溶液的是
(2)图二能表示NaNO3溶解度曲线的是
(3)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的
A.甲、乙都是饱和溶液
B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙
D.溶质质量分数:甲>乙
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】硝酸钾溶解度曲线如图所示

①10℃时,硝酸钾的溶解度是____________ g/100g水。
②某温度时,6.4g硝酸钾放入10g水中恰好形成饱和溶液,则该温度硝酸钾的溶解度是________ g/100g水。
③如下图所示进行实验,分别采用不同方法(每种方法只改变一个量),得到三个恰好饱和的溶液A1、A2、A3,且溶液质量依次减小。

I.请定量说明“方法一”是_____________ ;
II.请在溶解度曲线图中标出表示溶液A2的点,并标注“A2”_____________ ;
Ⅲ.溶液A1、A2、A3中溶质质量分数的大小关系是_______________ 。

①10℃时,硝酸钾的溶解度是
②某温度时,6.4g硝酸钾放入10g水中恰好形成饱和溶液,则该温度硝酸钾的溶解度是
③如下图所示进行实验,分别采用不同方法(每种方法只改变一个量),得到三个恰好饱和的溶液A1、A2、A3,且溶液质量依次减小。

I.请定量说明“方法一”是
II.请在溶解度曲线图中标出表示溶液A2的点,并标注“A2”
Ⅲ.溶液A1、A2、A3中溶质质量分数的大小关系是
您最近一年使用:0次
【推荐3】目前工业上用真空法制备食盐,通过减压能使热的海水快速蒸发,同时还能获得淡水。
(1)实验室中用溶液a(3%NaCl溶液1000g)模拟真空法制备食盐的流程(忽略物质的损耗)如下图所示:

①步骤1中分子的______ 发生了变化。
A.间距 B.质量 C.种类 D.个数
②属于饱和溶液的是______ (填溶液的编号)。
③溶液a中溶质的质量为______ g。溶液a经减压蒸发后得到溶液b和NaCl固体xg,溶液b的质量______ (选填“<”、“=”或“>”)溶液c的质量。
④分离溶液c和氯化钠固体的操作是______ 。
(2)海水晒制可得粗盐,粗盐除NaCl外,还含有 、
、 以及泥沙等杂质。现设计一种制备精盐的实验流程,步骤如图。
以及泥沙等杂质。现设计一种制备精盐的实验流程,步骤如图。

①实验流程中加入过量X、Y溶液中的溶质分别是______ 。(填写编号)请简述选择该选项的理由______ 。
②判断Y溶液过量的方法是______ 。
Ⅰ、取少量溶液A滴入硝酸银溶液,出现白色沉淀
Ⅱ、取少量沉淀滴入盐酸,有气泡产生
Ⅲ、取少量溶液A,滴入紫色石蕊,溶液变蓝
Ⅳ、取少量溶液A滴入石灰水,出现白色沉淀
③沉淀中除了泥沙等难溶杂质,还主要有______ 物质。加入Z溶液过量,但对精盐制备没有影响不必除去,这是利用Z溶液的______ 性质。
(1)实验室中用溶液a(3%NaCl溶液1000g)模拟真空法制备食盐的流程(忽略物质的损耗)如下图所示:

| 温度(℃) | 20 | 90 |
| NaCl的溶解度(g/100g水) | 36 | 39 |
A.间距 B.质量 C.种类 D.个数
②属于饱和溶液的是
③溶液a中溶质的质量为
④分离溶液c和氯化钠固体的操作是
(2)海水晒制可得粗盐,粗盐除NaCl外,还含有
 、
、 以及泥沙等杂质。现设计一种制备精盐的实验流程,步骤如图。
以及泥沙等杂质。现设计一种制备精盐的实验流程,步骤如图。
①实验流程中加入过量X、Y溶液中的溶质分别是
| 选项 溶质 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| X | Na2CO3 | Na2CO3 | BaCl2 | Ba(NO3)2 |
| Y | BaCl2 | Ba(NO3)2 | Na2CO3 | Na2CO3 |
Ⅰ、取少量溶液A滴入硝酸银溶液,出现白色沉淀
Ⅱ、取少量沉淀滴入盐酸,有气泡产生
Ⅲ、取少量溶液A,滴入紫色石蕊,溶液变蓝
Ⅳ、取少量溶液A滴入石灰水,出现白色沉淀
③沉淀中除了泥沙等难溶杂质,还主要有
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】已知A、B两种固体物质的溶解度曲线如图所示,请根据图回答下列问题:

(1)t1℃时,A物质的溶解度_____ B物质的溶解度(填“>”“<”或“=”).
(2)t2℃时,B物质的饱和溶液中溶质与溶剂的质量比为______ .
(3)将A物质的某种溶液从t3℃降至t1℃,溶液____ (填“一定会”“可能会”或“一定不会”)有晶体析出

(1)t1℃时,A物质的溶解度
(2)t2℃时,B物质的饱和溶液中溶质与溶剂的质量比为
(3)将A物质的某种溶液从t3℃降至t1℃,溶液
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】天青石(主要含有 SrSO4和少量 CaCO3 杂质)是获取锶元素的各种化合物的主要原料。请回答下列问题:
(1)硫化锶(SrS)可用作发光涂料的原料,SrSO4和碳的混合粉末在隔绝空气下高温焙烧可生成硫化锶和一种还原性气体,该反应的化学方程式________ ;
(2)以天青石生产 Sr(OH)2·8H2O 的工艺如下:

已知:1.锶(Sr)是人体必需的微量元素,其单质和化合物的化学性质与钙相似
2.Sr(OH)2、Ca(OH)2在水中的溶解度如下表:
①“反应 1”要控制温度在 30℃以下,这是因为_________ ;操作 1的名称是_________ ,其中玻璃棒的作用是________ 。
②滤渣 2是CaCO3和SrCO3 的混合物,滤液 3中含有的溶质为(NH4)2SO4和_______ ;写 出反应 1生成 SrCO3的化学方程式_________ ;
③“煅烧”滤渣 2得到的固体 4的成分是________ ;
④固体4“加热水浸”是为了获得较纯净的Sr(OH)2溶液,此时应缓慢加热使沉淀颗粒长大,滤渣 6的主要成分是______ (填化学式);“趁热过滤”的目的是______ ;
⑤“操作 2”主要有:_____ 、过滤、洗涤、干燥。
(1)硫化锶(SrS)可用作发光涂料的原料,SrSO4和碳的混合粉末在隔绝空气下高温焙烧可生成硫化锶和一种还原性气体,该反应的化学方程式
(2)以天青石生产 Sr(OH)2·8H2O 的工艺如下:

已知:1.锶(Sr)是人体必需的微量元素,其单质和化合物的化学性质与钙相似
2.Sr(OH)2、Ca(OH)2在水中的溶解度如下表:
| 温度/(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度(g) | Sr(OH)2 | 0.91 | 1.77 | 3.95 | 8.42 | 20.2 | 91.2 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
②滤渣 2是CaCO3和SrCO3 的混合物,滤液 3中含有的溶质为(NH4)2SO4和
③“煅烧”滤渣 2得到的固体 4的成分是
④固体4“加热水浸”是为了获得较纯净的Sr(OH)2溶液,此时应缓慢加热使沉淀颗粒长大,滤渣 6的主要成分是
⑤“操作 2”主要有:
您最近一年使用:0次
【推荐3】可从组成、性质和溶液等不同角度研究水。
(1)在水电解器中加入稀Na2SO4溶液(Na2SO4不参与反应),至充满管A和管B。通直流电一段时间后现象如图所示。

①检验A中的气体的方法是____________ 。
②B中气体验纯后点燃,产生___________ 色火焰。
③硫酸钠在水中解离出Na+和SO ,其作用是
,其作用是___________ 。
(2)将黄豆大小的金属钠放入盛有水的烧杯中,生成H2;在反应后的溶液中滴入酚酞试液,溶液变红。写出该反应的化学方程式___________ 。
(3)下图及表是氯化钠和碳酸钠溶解度曲线及不同温度下的溶解度信息。

①t2℃的溶解度是___________ 。
②t2℃时,将40 g Na2CO3固体充分溶解于50g水中,所得溶液的溶质质量分数为________ (列式即可)。
③若Na2CO3中混有少量的NaCl,提纯Na2CO3应采取的方法是________ (填“降温结晶”或“蒸发结晶”)。
(1)在水电解器中加入稀Na2SO4溶液(Na2SO4不参与反应),至充满管A和管B。通直流电一段时间后现象如图所示。

①检验A中的气体的方法是
②B中气体验纯后点燃,产生
③硫酸钠在水中解离出Na+和SO
 ,其作用是
,其作用是(2)将黄豆大小的金属钠放入盛有水的烧杯中,生成H2;在反应后的溶液中滴入酚酞试液,溶液变红。写出该反应的化学方程式
(3)下图及表是氯化钠和碳酸钠溶解度曲线及不同温度下的溶解度信息。

| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| 氯化钠溶解度/g | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠溶解度/g | 6 | 10 | 18 | 36.5 | 50 |
②t2℃时,将40 g Na2CO3固体充分溶解于50g水中,所得溶液的溶质质量分数为
③若Na2CO3中混有少量的NaCl,提纯Na2CO3应采取的方法是
您最近一年使用:0次
【推荐1】海洋中蕴藏着丰富的化学资源,按目前测定,海水中含有的化学元素有80多种。其中由某些元素组成的盐(均不含结晶水)的溶解度曲线如下图所示。
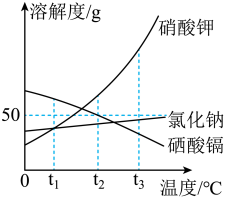
(1)在_________ ℃时,氯化钠和硝酸钾的溶解度相等。
(2)将接近饱和的硒酸镉溶液变为饱和溶液的方法有__________ (任写一种)。
(3)t2℃时,30g硒酸镉固体加到50g水中,充分溶解并恢复至原温度后,所得溶液中溶质的质量分数是____________ (精确到0.1%)。
(4)t1℃时,将三种物质的等质量饱和溶液升温至t3℃(不考虑溶剂蒸发),下列说法正确的是 (填选项)。

(1)在
(2)将接近饱和的硒酸镉溶液变为饱和溶液的方法有
(3)t2℃时,30g硒酸镉固体加到50g水中,充分溶解并恢复至原温度后,所得溶液中溶质的质量分数是
(4)t1℃时,将三种物质的等质量饱和溶液升温至t3℃(不考虑溶剂蒸发),下列说法正确的是 (填选项)。
| A.有晶体析出的是硒酸镉溶液 |
| B.溶质质量分数大小关系是:硝酸钾溶液>氯化钠溶液>硒酸镉溶液 |
| C.溶剂质量大小关系是:硝酸钾溶液=氯化钠溶液>硒酸镉溶液 |
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
名校
【推荐2】将质量均为 30g 的 A、B 两物质分别加入到 50g 水中,充分搅拌后,剩余物质质量与温度的关系如图所示。

(1)固体 B 的溶解度随温度升高而____ (填“增大”或“减小”)。t1℃时,B 的溶解度是 _____ 。
(2)若 t℃时,A、B 两溶液的溶质质量分数相等,该温度 可能是_____ (填序号)。
①0<t<t2 ②t=t2 ③t>t2 ④以上都可能
(3)关于固体 A、B 的说法正确的是_____ (填序号)。
①A 中含有少量 B,可用降温结晶提纯 A
②t1℃时,恒温蒸发水可将浓度为 15%的 B 溶液变为 30%
③t1℃时,等质量的 A、B 饱和溶液中,A 中溶质更多
(4)若 A、B 两物质中有一种是气体,该物质是_____ (填“A”或“B”)。

(1)固体 B 的溶解度随温度升高而
(2)若 t℃时,A、B 两溶液的溶质质量分数相等,该温度 可能是
①0<t<t2 ②t=t2 ③t>t2 ④以上都可能
(3)关于固体 A、B 的说法正确的是
①A 中含有少量 B,可用降温结晶提纯 A
②t1℃时,恒温蒸发水可将浓度为 15%的 B 溶液变为 30%
③t1℃时,等质量的 A、B 饱和溶液中,A 中溶质更多
(4)若 A、B 两物质中有一种是气体,该物质是
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
名校
解题方法
【推荐3】如图1是A、B、C三种物质的溶解度曲线图。请回答:

(1)t1℃时,A.B两种物质溶解度大小关系为A___ (填“>”“<”或“=”)B。
(2)B的饱和溶液中混有少量的物质A,婴除去A得到较纯的B物质,可采用的结晶方法是___ (填“降温结晶”“或“蒸发结晶”)。
(3)将和t2℃时等质量的A、B、C三种物质的饱和溶液,分别降温至t1℃。下列说法正确的是___ (填字母)。
a.析出晶体的质量:A>B b.溶质的质量分数:B>A=C c.溶剂的质量:B>A
(4)如图2所示,在大烧杯中加入一定量的硝酸铵固体后,乙试管内的溶液为_______ 溶液(填“饱和”或“不饱和)。

(1)t1℃时,A.B两种物质溶解度大小关系为A
(2)B的饱和溶液中混有少量的物质A,婴除去A得到较纯的B物质,可采用的结晶方法是
(3)将和t2℃时等质量的A、B、C三种物质的饱和溶液,分别降温至t1℃。下列说法正确的是
a.析出晶体的质量:A>B b.溶质的质量分数:B>A=C c.溶剂的质量:B>A
(4)如图2所示,在大烧杯中加入一定量的硝酸铵固体后,乙试管内的溶液为
您最近一年使用:0次



