下图是A、B、C三种固体物质的溶解度曲线,请回答下列问题。___________________ 。
(2)在t1℃时,将20g A物质加入到50g水中,充分溶解,得到溶液的质量为________ 。
(3)将t3℃时A、B、C三种物质的饱和溶液降温到t2℃,此时三种溶液中溶质的质量分数大小关系是________ 。
(4)若A中混有少量B时,最好采用___________ 的方法提纯A。
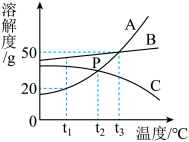
(2)在t1℃时,将20g A物质加入到50g水中,充分溶解,得到溶液的质量为
(3)将t3℃时A、B、C三种物质的饱和溶液降温到t2℃,此时三种溶液中溶质的质量分数大小关系是
(4)若A中混有少量B时,最好采用
2018·甘肃金昌·中考真题 查看更多[13]
2024年江苏省徐州市铜山区中考一模化学试题 2022年湖南省衡阳市第九中学中考化学模拟试题2019年广西百色市靖西市中考一模化学试题湖南省长沙市长郡芙蓉中学2021-2022学年九年级上学期期末模拟化学试题甘肃省张掖市甘州区育才中学2020-2021学年九年级下学期开学考试化学试题山东省济宁市金乡县育才学校2020-2021学年九年级上学期12月月考化学试题2019年山东省济宁市金乡县中考一模化学试题甘肃省武威市民勤县第六中学2019-2020学年九年级下学期开学考试化学试题【校级联考】宁夏银川北塔中学2019届九年级下学期中考第三次模拟化学试题甘肃省民勤县第六中学2019届九年级下学期第一次诊断考试化学试题【市级联考】山东省济宁市2019届九年级上学期期末考试化学试题【校级联考】山东省济宁市鱼台县2019届九年级上学期期末考试化学试题甘肃省金昌市2018年中考化学试题
更新时间:2018-09-21 14:57:24
|
相似题推荐
填空与简答-填空题
|
困难
(0.15)
解题方法
【推荐1】硝酸钾和氯化钾的溶解度曲线如图所示:

(1)t1℃时,硝酸钾的溶解度为________ g;
(2)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是_________ ;
(3)将t3℃时硝酸钾和氯化钾的饱和溶液各100g,降温至t2℃过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是________ 。
A都是饱和溶液 B溶液质量a<b C溶质质量a=b D溶剂质量a<b E溶质的质量分数a=b

(1)t1℃时,硝酸钾的溶解度为
(2)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是
(3)将t3℃时硝酸钾和氯化钾的饱和溶液各100g,降温至t2℃过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是
A都是饱和溶液 B溶液质量a<b C溶质质量a=b D溶剂质量a<b E溶质的质量分数a=b
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐2】t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成下图中的斜线。请回答下列问题:
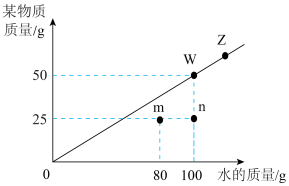
(1)t℃时该物质的溶解度为_____ 。
(2)图中4个点表示的溶液中溶质质量分数的关系是_____ 。
A z=w>m>n
B z>w>m>n
C z>w=m>n
D z>w>m=n
(3)n点表示溶液中溶质的质量分数为_____ 。
(4)该物质的溶解度随温度升高而_____ 。
A 增大 B 减小
C 不变 D 无法确定

(1)t℃时该物质的溶解度为
(2)图中4个点表示的溶液中溶质质量分数的关系是
A z=w>m>n
B z>w>m>n
C z>w=m>n
D z>w>m=n
(3)n点表示溶液中溶质的质量分数为
(4)该物质的溶解度随温度升高而
A 增大 B 减小
C 不变 D 无法确定
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐3】下表是氯化钠和硝酸钾在不同温度下的溶解度。(假设硝酸钾与氯化钠同时溶解在水中各自的溶解度不变,实验过程中水分损失忽略不计)。
①由表可知,20℃时,氯化钠的溶解度是________ 。影响硝酸钾溶解度的因素是_________ 。
②在80℃的100g水中溶解NaCl和KNO3,进行以下实验:

Ⅰ.操作1的名称是_________ 。
Ⅱ.溶液a冷却至b的过程中出现的现象是__________ 。溶液d中所含的溶质是_________ 。
Ⅲ.对整个实验过程分析正确的是_________ 。
A.无法判断a、d溶液中氯化钠溶液的状态 B.固体c是纯净物
C.溶液a中硝酸钾的质量分数为 D.硝酸钾溶液始终处于饱和状态
D.硝酸钾溶液始终处于饱和状态
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度(g/100g水) | KNO3 | 13.3 | 31.6 | 64.0 | 110.0 | 169.0 | 246.0 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
②在80℃的100g水中溶解NaCl和KNO3,进行以下实验:

Ⅰ.操作1的名称是
Ⅱ.溶液a冷却至b的过程中出现的现象是
Ⅲ.对整个实验过程分析正确的是
A.无法判断a、d溶液中氯化钠溶液的状态 B.固体c是纯净物
C.溶液a中硝酸钾的质量分数为
 D.硝酸钾溶液始终处于饱和状态
D.硝酸钾溶液始终处于饱和状态
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
【推荐1】以某矿渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
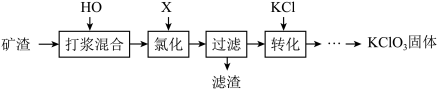
(1)打浆混合的目的是______________________ 。
(2)氯化过程控制矿渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2、CaCl2和H2O,写出该反应的化学方程式__________________ ,此反应 _________ 置换反应(选填“属于”“不属于”); 其中Ca(ClO)2进一步转化为Ca(ClO3)2。
(3)氯化时矿渣稍过量的原因是__________________ 。
(4)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O滤渣的主要成分是____________ 和 ______________ CaCO3、Ca(OH)2填化学式)。
(5)已知:几种物质的溶解度曲线如图所示。
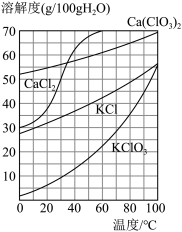
向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若从该溶液中尽可能多地析出KClO3固体的方法是___________ 、冷却结晶。

(1)打浆混合的目的是
(2)氯化过程控制矿渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2、CaCl2和H2O,写出该反应的化学方程式
(3)氯化时矿渣稍过量的原因是
(4)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O滤渣的主要成分是
(5)已知:几种物质的溶解度曲线如图所示。

向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若从该溶液中尽可能多地析出KClO3固体的方法是
您最近一年使用:0次
【推荐2】侯德榜先生发明了侯氏制碱法,主要原理及部分操作为:一定条件下,将NH3、CO2通入饱和氯化钠溶液,发生反应: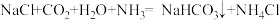 ,过滤,滤液中主要含有NH4Cl、NaCl两种物质,如图为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。回答下列问题:
,过滤,滤液中主要含有NH4Cl、NaCl两种物质,如图为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。回答下列问题:
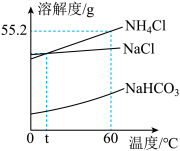
(1)60℃时,氯化铵的溶解度是______ g。
(2)碳酸氢钠晶体首先从溶液中析出的原因是______ 。
(3)从滤液中得到氯化铵晶体的操作:蒸发浓缩、______ 、过滤、洗涤、干燥。
(4)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,下列说法正确的是______ (填标号)。
A.甲和乙都是饱和溶液 B.溶剂的质量:甲<乙
C.溶液的质量:甲>乙 D.溶质的质量分数:甲=乙
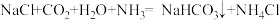 ,过滤,滤液中主要含有NH4Cl、NaCl两种物质,如图为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。回答下列问题:
,过滤,滤液中主要含有NH4Cl、NaCl两种物质,如图为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。回答下列问题:
(1)60℃时,氯化铵的溶解度是
(2)碳酸氢钠晶体首先从溶液中析出的原因是
(3)从滤液中得到氯化铵晶体的操作:蒸发浓缩、
(4)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,下列说法正确的是
A.甲和乙都是饱和溶液 B.溶剂的质量:甲<乙
C.溶液的质量:甲>乙 D.溶质的质量分数:甲=乙
您最近一年使用:0次
【推荐3】2019年1月2日,运城盐湖在低温下湖面上绽放出美丽的“硝花”(如图)。

材料一:“硝花”是晶体结晶在盐板上的一种特有的现象,温度低至0℃或0℃以下时,析出硫酸钠晶体(俗称芒硝),低于-5℃时,硫酸镁晶体也会析出,形成形状多样的“硝花”。
材料二:该盐湖中含有氯离子、钠离子、镁离子、硫酸根离子等,它们会随着温度变化自由组合,结晶出不同的化合物。氯化钠等物质的溶解度曲线如图所示。

材料三:一年四季,盐湖变换着不同的景色,春、秋两季碧波万顷,湖水清澈:夏季气温高达42℃,水位下降,湖底析出氯化钠晶体,生长的藻类使湖水变成了红色;冬季湖面上盐花丛生,洁白如雪。
根据短文回答问题:
(1)硝花是_________ (填“混合物”或“纯净物”);盐湖中含有的阴离子是_________ (写一种,用符号表示)。
(2)上述景色变换中包含的过程有_________ (填序号)。
①蒸发 ②蒸馏 ③结晶 ④升华
(3)入冬,随着温度的变化,该盐湖开始先析出NaCl。NaCl先析出的原因是_________ 。
(4)下列说法正确的是_________ 。
A 运城盐湖中还可能析出氯化镁晶体
B 芒硝是白色晶体
C 硫酸镁的溶解度随着温度升高而增大
D 该盐湖析出氯化钠主要是蒸发结晶,而析出硫酸镁晶体主要是降温结晶

材料一:“硝花”是晶体结晶在盐板上的一种特有的现象,温度低至0℃或0℃以下时,析出硫酸钠晶体(俗称芒硝),低于-5℃时,硫酸镁晶体也会析出,形成形状多样的“硝花”。
材料二:该盐湖中含有氯离子、钠离子、镁离子、硫酸根离子等,它们会随着温度变化自由组合,结晶出不同的化合物。氯化钠等物质的溶解度曲线如图所示。

材料三:一年四季,盐湖变换着不同的景色,春、秋两季碧波万顷,湖水清澈:夏季气温高达42℃,水位下降,湖底析出氯化钠晶体,生长的藻类使湖水变成了红色;冬季湖面上盐花丛生,洁白如雪。
根据短文回答问题:
(1)硝花是
(2)上述景色变换中包含的过程有
①蒸发 ②蒸馏 ③结晶 ④升华
(3)入冬,随着温度的变化,该盐湖开始先析出NaCl。NaCl先析出的原因是
(4)下列说法正确的是
A 运城盐湖中还可能析出氯化镁晶体
B 芒硝是白色晶体
C 硫酸镁的溶解度随着温度升高而增大
D 该盐湖析出氯化钠主要是蒸发结晶,而析出硫酸镁晶体主要是降温结晶
您最近一年使用:0次
【推荐1】溶液与人们的生产、生活密切相关。
(1)A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题。

①t1℃时,溶解度等于20g的物质为___________ (填字母);
②t2℃时,向盛有50gB物质的烧杯中加入100g水,充分溶解后,所得溶液的质量______ 150g(填“>”、“<”或“=”);
③t1℃时,A、B、C三种物质饱和溶液升温到t2℃后,溶液中溶质质量分数由大到小的顺序是_____ 。
④t2℃时,300gA物质的饱和溶液降温到t1℃时,析出晶体的质量是___________ g。
(2)配制50g质量分数为15%的氯化钠溶液:
①溶解过程中玻璃棒的作用是___________ 。
②对配制的溶液进行检测发现溶质质量分数偏小,其原因可能有___________ 。(填字母)
A.称量时,药品与砝码放反了(1g以下使用游码)
B.量取水的体积时,仰视读数
C.装瓶时,有少量溶液洒出
③若用50g质量分数为15%的氧化钠溶液配制溶质质量分数为5%的氯化钠溶液,需要加水的质量是___________ 。
(1)A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题。

①t1℃时,溶解度等于20g的物质为
②t2℃时,向盛有50gB物质的烧杯中加入100g水,充分溶解后,所得溶液的质量
③t1℃时,A、B、C三种物质饱和溶液升温到t2℃后,溶液中溶质质量分数由大到小的顺序是
④t2℃时,300gA物质的饱和溶液降温到t1℃时,析出晶体的质量是
(2)配制50g质量分数为15%的氯化钠溶液:
①溶解过程中玻璃棒的作用是
②对配制的溶液进行检测发现溶质质量分数偏小,其原因可能有
A.称量时,药品与砝码放反了(1g以下使用游码)
B.量取水的体积时,仰视读数
C.装瓶时,有少量溶液洒出
③若用50g质量分数为15%的氧化钠溶液配制溶质质量分数为5%的氯化钠溶液,需要加水的质量是
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
解题方法
【推荐2】不同物质在水中的溶解度不同,t1℃时,将甲,乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一、甲和乙的溶解度曲线如图二、请结合图示回答下列问题:

(1)固体甲对应的溶解度曲线是_____ (填“a”或“b”)。
(2)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是_____ 。
(3)将165gt1℃曲线a对应物质的饱和溶液变为t2℃时的饱和溶液,需蒸发掉水_____ g。(保留一位小数)
(4)将t2℃等质量的甲、乙饱和溶液分别降温到们将t1℃时,所得溶液的有关说法正确的是_____ (填字母)。
a、甲溶液仍为饱和溶液
b、两溶液质量:甲<乙
c、两溶液中溶剂质量:甲=乙
d、两溶液溶质质量分数:甲>乙

(1)固体甲对应的溶解度曲线是
(2)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是
(3)将165gt1℃曲线a对应物质的饱和溶液变为t2℃时的饱和溶液,需蒸发掉水
(4)将t2℃等质量的甲、乙饱和溶液分别降温到们将t1℃时,所得溶液的有关说法正确的是
a、甲溶液仍为饱和溶液
b、两溶液质量:甲<乙
c、两溶液中溶剂质量:甲=乙
d、两溶液溶质质量分数:甲>乙
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
【推荐3】现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
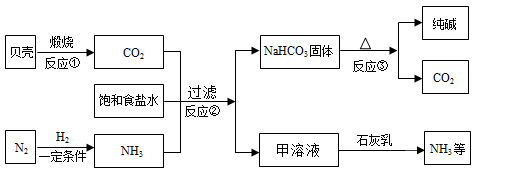
(1)已知20℃,氧化钠溶解度为36g,则20时饱和食盐水溶质质量分数为______________ ;(保留1位小数)
(2)反应①的化学方程式是_______________________ ;
(3)甲溶液中能与石灰乳反应生成氨气的物质是_____________ ,实验室中通常检验氨气的试剂是______________ ;
(4)反应②的化学方程式是_____________________ ;
(5)整个生产过程中可循环利用的物质是_________________ ;
(6)为测定产品纯碱中钠元素质量分数,取样(样品中除纯碱外还含有碳酸氢钠和少量不溶性杂质)设计如下实验过程:

请回答:
Ⅰ.操作①是溶解,操作②为__________________ ;
Ⅱ.原样品中钠元素的质量分数为___________________ ;
Ⅲ.若测定结果偏低,原因可能是__________ (填字母)。
A.溶液D中含有Na2CO3 B.溶液D中含有NaCl
C.操作③中固体没有洗涤干净 D.操作④中加入过量的盐酸

(1)已知20℃,氧化钠溶解度为36g,则20时饱和食盐水溶质质量分数为
(2)反应①的化学方程式是
(3)甲溶液中能与石灰乳反应生成氨气的物质是
(4)反应②的化学方程式是
(5)整个生产过程中可循环利用的物质是
(6)为测定产品纯碱中钠元素质量分数,取样(样品中除纯碱外还含有碳酸氢钠和少量不溶性杂质)设计如下实验过程:

请回答:
Ⅰ.操作①是溶解,操作②为
Ⅱ.原样品中钠元素的质量分数为
Ⅲ.若测定结果偏低,原因可能是
A.溶液D中含有Na2CO3 B.溶液D中含有NaCl
C.操作③中固体没有洗涤干净 D.操作④中加入过量的盐酸
您最近一年使用:0次



