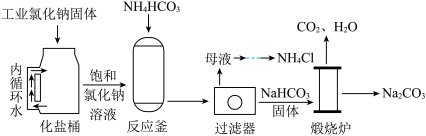
从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,将粗盐溶于水然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发.
(1)正确的操作顺序是_______ (填字母).
(2)加Na2CO3溶液的作用是除去_____ (填化学式)
(1)正确的操作顺序是
(2)加Na2CO3溶液的作用是除去
更新时间:2018-11-09 14:58:19
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
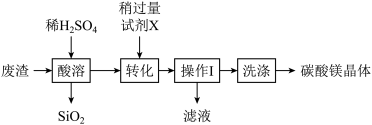
【推荐1】碳酸镁晶体广泛应用于冶金、耐火材料及化工产品等领域。利用某废渣(含MgCO3、MgO和SiO2)制备碳酸镁晶体(MgCO3·3H2O)的工艺流程如图所示,已知SiO2不溶于水。
(1)操作Ⅰ的名称是________________ 。
(2)为加快“酸溶”的速率,可采取的一种措施是________________ 。
(3)试剂X应选用________________(填字母)。
(4)洗涤时检验碳酸镁晶体已洗净的方法:取最后一次洗涤后的滤液,先滴加足量的稀盐酸,再滴加________________ (填化学式)溶液,无明显现象。
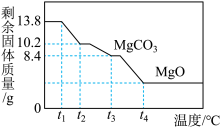
(5)小组同学取13.8g碳酸镁晶体进行加热,测得固体质量与温度之间的关系如图所示。已知碳酸镁晶体受热分解会生成3种氧化物。
①碳酸镁晶体受热分解最终生成水的质量是________________ g。
②计算高温条件下完全反应后生成氧化镁的质量________ (写出计算过程)。
(1)操作Ⅰ的名称是
(2)为加快“酸溶”的速率,可采取的一种措施是
(3)试剂X应选用________________(填字母)。
| A.NaOH溶液 | B.CaCO3悬浊液 | C.Na2CO3溶液 |
(5)小组同学取13.8g碳酸镁晶体进行加热,测得固体质量与温度之间的关系如图所示。已知碳酸镁晶体受热分解会生成3种氧化物。
①碳酸镁晶体受热分解最终生成水的质量是
②计算高温条件下完全反应后生成氧化镁的质量
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
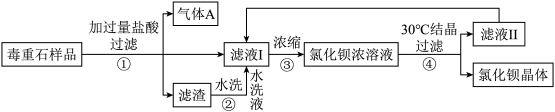
【推荐2】氯化钡是一种可溶性重金属盐,广泛应用于化工领域,其水溶液呈中性。工业上用毒重石(主要成是BaCO3)制备氯化钡晶体。某实验小组模拟工业上制备氯化钡晶体的流程,设计了实验室中制备氯化钡晶体的方案,实验流程如图所示。(该毒重石样品所含杂质难溶于水,不与酸反应)。
(1)步骤①中发生反应的化学方程式为______________ 。
(2)滤液Ⅱ是30℃时氯化钡的____________ 溶液(选填“饱和”或“不饱和”)。
(3)关于上述实验方案的相关内容,下列说法不正确的是____________ (选填字母序号)。
A氯化钡是一种有毒的物质,使用时应注意安全
B该实验流程中得到的副产品二氧化碳是重要的化工原料
C可用重晶石(主要成分是硫酸钡)代替该实验流程中的毒重石,制备氯化钡晶体
D步骤②将滤渣进行水洗,既能提高氯化钡晶体的产率,又能减少Ba2+环境的污染

(1)步骤①中发生反应的化学方程式为
(2)滤液Ⅱ是30℃时氯化钡的
(3)关于上述实验方案的相关内容,下列说法不正确的是
A氯化钡是一种有毒的物质,使用时应注意安全
B该实验流程中得到的副产品二氧化碳是重要的化工原料
C可用重晶石(主要成分是硫酸钡)代替该实验流程中的毒重石,制备氯化钡晶体
D步骤②将滤渣进行水洗,既能提高氯化钡晶体的产率,又能减少Ba2+环境的污染
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】除去NaCl溶液中CaCl2、MgCl2、Na2SO4杂质的操作有:①加入过量的NaOH溶液,②加入过量的BaCl2溶液,③过滤,④加适量的盐酸;⑤加过量的Na2CO3溶液.
(1)以上操作合理的而先后顺序为_____ (数字序号不能重复使用).
(2)请写出BaCl2溶液与Na2CO3溶液反应的化学方程式._____
(3)上述试剂中的Na2CO3不能用K2CO3代替,请说明原因._____
(1)以上操作合理的而先后顺序为
(2)请写出BaCl2溶液与Na2CO3溶液反应的化学方程式.
(3)上述试剂中的Na2CO3不能用K2CO3代替,请说明原因.
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】请回答下列问题:
(1)“粗盐中难溶性杂质的去除”实验步骤:
①溶解称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.2g。
②过滤。
③蒸发,请从溶解度的角度分析,实验中不采用降低溶液温度的方法得到精盐的依据是_____ 。
④计算产率得到精盐3.2g,则精盐的产率为_____ 。(计算结果保留一位小数)
整个实验中至少要进行____ 次称量;从海水中获得的粗盐,经过上述实验得到精盐属于____ (填“混合物”或“纯净物”)。
(2)根据下图所示溶解度曲线。
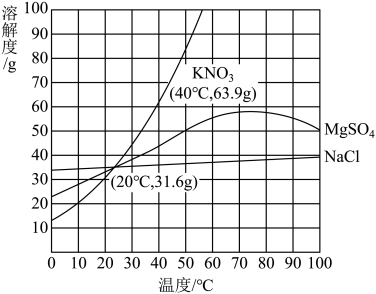
①40℃时,向装有50g水的烧杯中加入25gKNO3固体,充分搅拌后,所得溶液的溶质质量分数为___ (精确到0.1%),将该溶液降温至20℃时,析出KNO3晶体的质量为_____ g。
②若用溶质质量分数为16%的KNO3溶液和蒸馏水,配制200g溶质质量分数为10%的KNO3溶液,则需要取蒸馏水的体积为____ mL。
(1)“粗盐中难溶性杂质的去除”实验步骤:
①溶解称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.2g。
②过滤。
③蒸发,请从溶解度的角度分析,实验中不采用降低溶液温度的方法得到精盐的依据是
④计算产率得到精盐3.2g,则精盐的产率为
整个实验中至少要进行
(2)根据下图所示溶解度曲线。

①40℃时,向装有50g水的烧杯中加入25gKNO3固体,充分搅拌后,所得溶液的溶质质量分数为
②若用溶质质量分数为16%的KNO3溶液和蒸馏水,配制200g溶质质量分数为10%的KNO3溶液,则需要取蒸馏水的体积为
您最近一年使用:0次