学习了酸碱盐的性质后,晨华以AgNO3为代表物质,归纳盐的化学性质,A、B、C、X分别表示能与AgNO3溶液反应的不同类别的物质.

(1)X的化学式可能是__________ .写出一条用途__________ .
(2)当C为铜时,写出反应③的化学方程式___________ .
(3)反应①~④中属于复分解反应的是__________ (填序号).

(1)X的化学式可能是
(2)当C为铜时,写出反应③的化学方程式
(3)反应①~④中属于复分解反应的是
2017·陕西·模拟预测 查看更多[4]
陕西省陕西师范大学附属中学2017届九年级中考五模化学试题(已下线)【万唯原创】2018年陕西省中考化学面对面卷九年级练习册模块一-酸碱盐综合训练(已下线)【万唯原创】2018年陕西省中考化学试题研究卷九年级讲解册模块一-专题5-7(已下线)主题 盐 化肥·基础必练1
更新时间:2018-11-15 15:38:04
|
相似题推荐
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】阅读科技短文,回答下列问题。
联合制碱法又称侯氏制碱法,用于在工业上制取纯碱,由侯德榜于1943年发明,是世界上广泛采用的制纯碱法。具体过程为:低温下,向饱和氨盐水中(氨气、氯化钠都达到饱和的溶液)通入二氧化碳,反应后生成的碳酸氢钠在加热条件下进一步分解为碳酸钠、水和二氧化碳。(碳酸氢钠固体50℃以上开始逐渐分解)其过程可以归纳为以下三步反应: ①NH3+H2O+CO2=NH4HCO3
②NH4HCO3+NaCl=NH4C1+NaHCO3↓
③2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
(1)反应①属于___________ 反应 (填基本反应类型)。
(2)写出纯碱的一条用途___________ 。
(3)在制纯碱过程中得到一种化肥,该化肥属于___________ (填“氮肥”“磷肥”或“钾肥”)。
(4)如图为NH4Cl、NaCl和 NaHCO3的溶解度曲线:
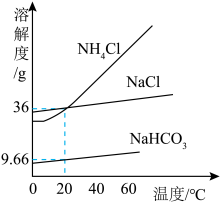
①若反应温度为20℃,结合溶解度曲线,说明反应②中能析出碳酸氢钠晶体的原因:___________ 。
②NaHCO3的溶解度曲线在温度高于60 ℃时“消失”了,试结合短文内容说明原因:___________ 。
联合制碱法又称侯氏制碱法,用于在工业上制取纯碱,由侯德榜于1943年发明,是世界上广泛采用的制纯碱法。具体过程为:低温下,向饱和氨盐水中(氨气、氯化钠都达到饱和的溶液)通入二氧化碳,反应后生成的碳酸氢钠在加热条件下进一步分解为碳酸钠、水和二氧化碳。(碳酸氢钠固体50℃以上开始逐渐分解)其过程可以归纳为以下三步反应: ①NH3+H2O+CO2=NH4HCO3
②NH4HCO3+NaCl=NH4C1+NaHCO3↓
③2NaHCO3
 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑(1)反应①属于
(2)写出纯碱的一条用途
(3)在制纯碱过程中得到一种化肥,该化肥属于
(4)如图为NH4Cl、NaCl和 NaHCO3的溶解度曲线:

①若反应温度为20℃,结合溶解度曲线,说明反应②中能析出碳酸氢钠晶体的原因:
②NaHCO3的溶解度曲线在温度高于60 ℃时“消失”了,试结合短文内容说明原因:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】化学与生活息息相关。
(一)探究物质溶解性的影响因素
小刚同学在实验中获得以下事实:①食盐易溶于水,难溶于植物油;②蔗糖在热水中溶解的质量比在等质量的冷水中溶解的质量大。
(1)上述两个事实表明,固体物质的溶解能力与_____ 因素有关。
(二)感受古法制盐
《四川盐法志》记载,“敞锅熬盐”主要步骤为:
步骤1 将黄卤(所含杂质主要为氯化钡)和黑卤(所含杂质主要为硫酸镁)按比例混合后过滤;
步骤2 滤液放入敞口锅中加热浓缩,析出粗盐;
步骤3 用“花水”冲洗粗盐得精品盐。
回答下列问题:
(2)步骤1中,两种杂质发生反应的化学方程式为____ ,该反应属于基本反应类型中的_____ 反应。
(3)步骤2中,“敞口熬盐”与_____ 的原理相同。
(4)步骤3用“花水”冲洗粗盐,既可除去表面的 和
和 杂质,又不损失
杂质,又不损失 。则“花水”应当是下列物质中的_____(填标号)。
。则“花水”应当是下列物质中的_____(填标号)。
(5)检验步骤3得到的“精品盐”中杂质是否除尽,可采取的方法是:_____ ,证明“精品盐”中的杂质已除尽。
(6)将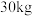 含10%
含10% 的黄卤和
的黄卤和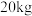 含15%
含15% 的黑卤混合,经“敞锅熬盐”制得的粗盐中
的黑卤混合,经“敞锅熬盐”制得的粗盐中 的质量最多为
的质量最多为_____ kg。
(一)探究物质溶解性的影响因素
小刚同学在实验中获得以下事实:①食盐易溶于水,难溶于植物油;②蔗糖在热水中溶解的质量比在等质量的冷水中溶解的质量大。
(1)上述两个事实表明,固体物质的溶解能力与
(二)感受古法制盐
《四川盐法志》记载,“敞锅熬盐”主要步骤为:
步骤1 将黄卤(所含杂质主要为氯化钡)和黑卤(所含杂质主要为硫酸镁)按比例混合后过滤;
步骤2 滤液放入敞口锅中加热浓缩,析出粗盐;
步骤3 用“花水”冲洗粗盐得精品盐。
回答下列问题:
(2)步骤1中,两种杂质发生反应的化学方程式为
(3)步骤2中,“敞口熬盐”与
(4)步骤3用“花水”冲洗粗盐,既可除去表面的
 和
和 杂质,又不损失
杂质,又不损失 。则“花水”应当是下列物质中的_____(填标号)。
。则“花水”应当是下列物质中的_____(填标号)。| A.蒸馏水 | B.饱和 溶液 溶液 |
C.饱和 溶液 溶液 | D.饱和 溶液 溶液 |
(6)将
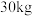 含10%
含10% 的黄卤和
的黄卤和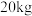 含15%
含15% 的黑卤混合,经“敞锅熬盐”制得的粗盐中
的黑卤混合,经“敞锅熬盐”制得的粗盐中 的质量最多为
的质量最多为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】过氧化钙(CaO2)是用途广泛的优良供氧剂。以电石渣[主要成分为Ca(OH)2,含少量CaCO3]为原料制备CaO2的一种工艺流程如下:

【查阅资料】I.Ca(OH)2+2NH4Cl=CaCl2+2NH3·H2O
Ⅱ.CaCl2+2NH3·H2O+H2O2+6H2O= CaO2·8H2O↓+ 2NH4Cl
Ⅲ.CaO2·8H2O在水中不太稳定,会缓慢分解。
(1)“提取Ca(OH)2”时反应的基本类型是__________ ;Ca(OH)2的俗名为_______ ;
(2)在实验室进行过滤操作时,需要的四种仪器是_________
(3)在其他条件不变的情况下,制备CaO2·8H2O的反应时间(t)对其产率(w)的影响如图所示。平均反应速率最快的时间段为:_______ (填字母)。

a.0~10min b.10~20min
c.20~30min d.30~40min

【查阅资料】I.Ca(OH)2+2NH4Cl=CaCl2+2NH3·H2O
Ⅱ.CaCl2+2NH3·H2O+H2O2+6H2O= CaO2·8H2O↓+ 2NH4Cl
Ⅲ.CaO2·8H2O在水中不太稳定,会缓慢分解。
(1)“提取Ca(OH)2”时反应的基本类型是
(2)在实验室进行过滤操作时,需要的四种仪器是
(3)在其他条件不变的情况下,制备CaO2·8H2O的反应时间(t)对其产率(w)的影响如图所示。平均反应速率最快的时间段为:

a.0~10min b.10~20min
c.20~30min d.30~40min
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】某同学们观察、比较铝箔和铁丝。
(1)金属能加工成“箔”或“丝”,体现了金属的_____ 性。
(2)铝箔光亮如新,体现了其具有抗腐蚀性,原因是_____ ,而一些铁丝表面锈迹斑斑,用盐酸可以将其除去,反应的化学方程式为 _____ 。
(3)下图为Mn(锰)和CuSO4溶液反应的示意图,回答下列问题:

①实际与Mn反应的粒子是_____ 。
②反应中失去电子的粒子是_____ 。
③由反应可知金属的活泼性:Mn_____ Cu(填“>”或“>”)。
(1)金属能加工成“箔”或“丝”,体现了金属的
(2)铝箔光亮如新,体现了其具有抗腐蚀性,原因是
(3)下图为Mn(锰)和CuSO4溶液反应的示意图,回答下列问题:

①实际与Mn反应的粒子是
②反应中失去电子的粒子是
③由反应可知金属的活泼性:Mn
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】新能源汽车是指采用非常规的车用燃料作为动力来源。技术原理先进、具有新技术、新结构的汽车。液氨有望成为新一代绿色能源应用在汽车上。氨气在纯氧中燃烧生成空气中含量最多的气体和一种氧化物,且释放大量热量。请根据要求回答下列问题。
(1)该反应的化学方程式为________ 。
(2)该化学反应前氮元素的化合价为________ 。
(3)该反应进行时的能量转化是由________ 能转化为内能。
(4)目前,多数汽车使用的燃料是汽油或柴油。但是,埋于海底将来可能会替代化石燃料的新能源是________ 。
(1)该反应的化学方程式为
(2)该化学反应前氮元素的化合价为
(3)该反应进行时的能量转化是由
(4)目前,多数汽车使用的燃料是汽油或柴油。但是,埋于海底将来可能会替代化石燃料的新能源是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】按要求填空:
(1)实验室氢气还原氧化铜的化学反应方程式:__________________________________
(2)酒精是一种重要燃料,其燃烧的化学反应方程式:____________________________
(3)实验室铁与稀硫酸化学反应方程式:________________________________________
(4)①写出化学式的名称并标出加点元素的化合价:
KI :名称______ ,化合价______
NaN O3:名称_______ ,化合价____________
②写出下列物质的化学式:
碳60(足球烯):______ 氧化钙:_______
氯化氢:___________ 铝土矿(主要成分)________
(1)实验室氢气还原氧化铜的化学反应方程式:
(2)酒精是一种重要燃料,其燃烧的化学反应方程式:
(3)实验室铁与稀硫酸化学反应方程式:
(4)①写出化学式的名称并标出加点元素的化合价:
K
Na
②写出下列物质的化学式:
碳60(足球烯):
氯化氢:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】“微观一宏观一符号”是化学独特的表示物质及其变化的方法。请根据信息回答下列问题。

(1)硒元素有防癌、抗癌作用。硒元素的部分信息如图1所示。硒元素的相对原子质量为_______ ,原子结构示意图中的x=_______ ,硒离子的化学符号为_________ 。
(2)氘和氚是制造氢弹的原料。氘核和氚核在超高温的条件下会聚合成一个氦核,如图2所示,该变化涉及的元素种类有_______ 种。
(3)已知如图3所示原子对应的元素在元素周期表中位于铝元素的正下方,且与铝元素的化学性质相似,则m的值为________ 。
(4)如图4,是将铜丝插入硝酸银溶液中反应的微观示意图,从微观粒子变化的角度分析该反应的实质是______ ,反应过程中溶液的质量变化是_______ (填“增大”“减小”或“不变”)。

(1)硒元素有防癌、抗癌作用。硒元素的部分信息如图1所示。硒元素的相对原子质量为
(2)氘和氚是制造氢弹的原料。氘核和氚核在超高温的条件下会聚合成一个氦核,如图2所示,该变化涉及的元素种类有
(3)已知如图3所示原子对应的元素在元素周期表中位于铝元素的正下方,且与铝元素的化学性质相似,则m的值为
(4)如图4,是将铜丝插入硝酸银溶液中反应的微观示意图,从微观粒子变化的角度分析该反应的实质是

您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】向硝酸银、硝酸铜和硝酸镁的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中滴加稀盐酸,无明显现象,则滤液中一定含有的金属离子是什么?写出上述过程中一定发生反应的化学方程式。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。某研究性小组对K2SO4和Mn3O4的制备展开了系列研究。
Ⅰ.以硫酸工业的尾气SO2制备K2SO4的工艺流程如下:

(1)反应釜I中发生的反应包括: 2CaCO3 + 2SO2+O2=2_______ +2CO2
(2)反应釜III:向反应II 所得(NH4)2SO4溶液中加入KCl溶液充分反应后,经蒸发浓缩、过滤 、洗涤、干燥等操作即可制得K2SO4产品。为提高K2SO4产品纯度,过滤时应控制反应液的温度范围为______ (填字母序号,如图为几种盐的溶解度曲线)。

A 0℃-10℃ B 20℃-30℃ C 60℃-65℃ D 80℃-90℃
(3)上述工艺流程中循环利用的物质是_______ ;检验产品K2SO4中不含杂质选用的试剂是 _____
A AgNO3溶液 B BaCl2溶液 C Ba(NO3)2溶液 DNaOH溶液
Ⅱ.实验室以SO2气体为原料制备少量高纯Mn3O4的操作步骤如下:
[资料1]亚硫酸(H2SO3)在Mn2+催化作用下被O2氧化为硫酸,硫酸与MnO2在常温下不易发生反应。
[资料2] MnSO4在空气中高温煅烧生成Mn3O4和三氧化硫,当温度超过1000℃时,Mn3O4易被氧化。
【步骤I】制备MnSO4溶液:在三颈烧瓶中(装置见(如图)加入一定量MnO2和水,先通氮气,再通入SO2和N2混合气体,搅拌反应3小时。停止通SO2,继续反应片刻后过滤得MnSO4溶液。

(4)烧杯中石灰乳(有效成分为氢氧化钙)的作用为____________ 。
(5)三颈烧瓶中生成MnSO4的反应化学方程式为______________ 。
(6)步骤I中,先通入氮气的目的是____________ 。为使SO2尽可能转化完全,在不改变固液投料和通入的SO2和N2比例一定的条件下,可采取的合理措施有:及时搅拌反应液、 ____________ (任写1条)。
【步骤II】制备MnSO4•H2O晶体:利用硫酸锰的溶解度在100℃以上随温度升高而急剧降低的原理,采用压力釜升温加压结晶法后过滤、洗涤、低温干燥得纯净的MnSO4•H2O晶体。
【步骤III】制备Mn3O4固体:准确称取101.4mg MnSO4•H2O,将MnSO4•H2O晶体在空气中高温煅烧,下图是用热重分析仪测定煅烧时温度与剩余固体质量变化曲线。
(7)Mn3O4中的Mn元素有+2,+3价,则Mn3O4中+2价和+3价锰的比例为_____
(8)该曲线中A段所表示物质的化学式为____________ 。
(9)试通过计算确定反应至图中C点时所对应的剩余固体成分的化学式____ (请写出计算过程)。

Ⅰ.以硫酸工业的尾气SO2制备K2SO4的工艺流程如下:

(1)反应釜I中发生的反应包括: 2CaCO3 + 2SO2+O2=2
(2)反应釜III:向反应II 所得(NH4)2SO4溶液中加入KCl溶液充分反应后,经蒸发浓缩、过滤 、洗涤、干燥等操作即可制得K2SO4产品。为提高K2SO4产品纯度,过滤时应控制反应液的温度范围为

A 0℃-10℃ B 20℃-30℃ C 60℃-65℃ D 80℃-90℃
(3)上述工艺流程中循环利用的物质是
A AgNO3溶液 B BaCl2溶液 C Ba(NO3)2溶液 DNaOH溶液
Ⅱ.实验室以SO2气体为原料制备少量高纯Mn3O4的操作步骤如下:
[资料1]亚硫酸(H2SO3)在Mn2+催化作用下被O2氧化为硫酸,硫酸与MnO2在常温下不易发生反应。
[资料2] MnSO4在空气中高温煅烧生成Mn3O4和三氧化硫,当温度超过1000℃时,Mn3O4易被氧化。
【步骤I】制备MnSO4溶液:在三颈烧瓶中(装置见(如图)加入一定量MnO2和水,先通氮气,再通入SO2和N2混合气体,搅拌反应3小时。停止通SO2,继续反应片刻后过滤得MnSO4溶液。

(4)烧杯中石灰乳(有效成分为氢氧化钙)的作用为
(5)三颈烧瓶中生成MnSO4的反应化学方程式为
(6)步骤I中,先通入氮气的目的是
【步骤II】制备MnSO4•H2O晶体:利用硫酸锰的溶解度在100℃以上随温度升高而急剧降低的原理,采用压力釜升温加压结晶法后过滤、洗涤、低温干燥得纯净的MnSO4•H2O晶体。
【步骤III】制备Mn3O4固体:准确称取101.4mg MnSO4•H2O,将MnSO4•H2O晶体在空气中高温煅烧,下图是用热重分析仪测定煅烧时温度与剩余固体质量变化曲线。
(7)Mn3O4中的Mn元素有+2,+3价,则Mn3O4中+2价和+3价锰的比例为
(8)该曲线中A段所表示物质的化学式为
(9)试通过计算确定反应至图中C点时所对应的剩余固体成分的化学式

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某兴严小组在实验室用废渣(主要成分为CaCO3,还含有C、CuO、MgO等少量杂质)来制取CaCl2,过程如图所示:

(1)滤渣I的主要成分为_______ (填化学式)。
(2)写出“除铜、镁”时发生反应的化学方程式_______ 。(写一个)
(3)为不产生副产品,可用_______ (填化学式)溶液代替NaOH溶液开展实验。

(1)滤渣I的主要成分为
(2)写出“除铜、镁”时发生反应的化学方程式
(3)为不产生副产品,可用
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某食品脱氧剂为无机铁系脱氧剂(各成分为:2g铁粉、0.5g活性炭、0.5g食盐), 某学习小组对脱氧剂的成分进行后续实验:具体步骤流程如下,请回答:
步骤Ⅰ:

步骤Ⅱ:将乙烘干后进行如下实验,物质之间的转化关系如图(部分产物略去)

(1)操作Ⅰ的名称是_______ ,所用到的玻璃仪器有烧杯、玻璃棒和______ ;
(2)溶液丙中含有的溶质是___________ (写化学式);
(3)固体乙在反应①中体现出的用途是___________ 。
(4)反应②,A 与 C 完全反应后,溶液 D 的阳离子是___________ ;
(5)反应③的基本反应类型是__________ ,写出符合的化学方程式为: __________ 。
步骤Ⅰ:

步骤Ⅱ:将乙烘干后进行如下实验,物质之间的转化关系如图(部分产物略去)

(1)操作Ⅰ的名称是
(2)溶液丙中含有的溶质是
(3)固体乙在反应①中体现出的用途是
(4)反应②,A 与 C 完全反应后,溶液 D 的阳离子是
(5)反应③的基本反应类型是
您最近一年使用:0次




