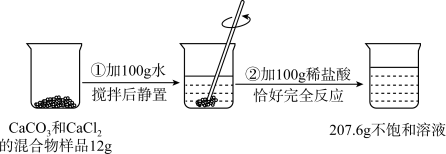
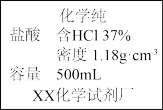请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
(1)实验所用稀盐酸的溶质的质量分数为______。若实验室还需要120g质量分数为7.3%的稀盐酸,现实验室只有36.5%的浓盐酸(密度为1.2g/mL),需要浓盐酸________毫升?配制过程中需加水______毫升?(写出计算过程,下同)
(2)计算原混合物样品中CaCl2的质量________。
(3)本实验最终所得的不饱和溶液的质量分数是________?(精确到0.1%)

(1)实验所用稀盐酸的溶质的质量分数为______。若实验室还需要120g质量分数为7.3%的稀盐酸,现实验室只有36.5%的浓盐酸(密度为1.2g/mL),需要浓盐酸________毫升?配制过程中需加水______毫升?(写出计算过程,下同)
(2)计算原混合物样品中CaCl2的质量________。
(3)本实验最终所得的不饱和溶液的质量分数是________?(精确到0.1%)
更新时间:2019-01-22 17:23:19
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】无土栽培是一种农业高新技术,它可以显著提高农作物的产量和质量。无土栽培中营养液成分易于控制,可随时调节。在光照、温度适宜而没有土壤的地方,如沙漠、海滩、荒岛,只要有一定量的淡水供应,便可进行。现有某品种无土栽培营养液,其中只含有质量分数为16%的NH4NO3;
(1)NH4NO3中氮元素的化合价分别为_______ ;
(2)NH4NO3的相对分子质量为_______ ;
(3)NH4NO3中氮、氢、氧元素的质量比为_______ ;
(4)NH4NO3营养液中氮元素的质量分数为_______ ;
(5)要配制150kg该营养液,需要NH4NO3的质量为_______ 。
(1)NH4NO3中氮元素的化合价分别为
(2)NH4NO3的相对分子质量为
(3)NH4NO3中氮、氢、氧元素的质量比为
(4)NH4NO3营养液中氮元素的质量分数为
(5)要配制150kg该营养液,需要NH4NO3的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质的质量分数。
实验一:37%的浓盐酸(密度为1.19g/mL)、氢氧化钠溶液、蒸馏水、量筒、细口瓶等
实验步骤:
(1)计算:配制74g质量分数为10%的稀盐酸,需要37%的浓盐酸的体积为____ mL(精确到0.1mL,下同);需要蒸馏水的体积为___ mL(水的密度为1.0g/mL)。
(2)量取:用量筒分别量取相应的浓盐酸和蒸馏水。
(3)_____________ 。
(4)装瓶并贴上标签。
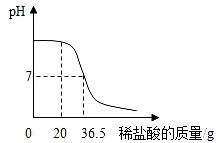
实验二:用上述配制的稀盐酸加入到20g某氢氧化钠溶液中,溶液pH的变化情况如右图所示。试计算该氢氧化钠溶液中溶质的质量分数。____________________________________ (写出计算过程)
实验一:37%的浓盐酸(密度为1.19g/mL)、氢氧化钠溶液、蒸馏水、量筒、细口瓶等
实验步骤:
(1)计算:配制74g质量分数为10%的稀盐酸,需要37%的浓盐酸的体积为

(2)量取:用量筒分别量取相应的浓盐酸和蒸馏水。
(3)
(4)装瓶并贴上标签。
实验二:用上述配制的稀盐酸加入到20g某氢氧化钠溶液中,溶液pH的变化情况如右图所示。试计算该氢氧化钠溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐1】为测定某BaCl2溶液的溶质质量分数,进行如下实验:取104g该溶液于烧杯中,加入1g稀硝酸溶液酸化,无任何现象,然后将30g一定溶质质量分数的硫酸溶液分三次加入,每次充分反应后过滤、称量(实验中物质的质量损失忽略不计),数据如表:
根据以上数据计算:(BaCl2+H2SO4═BaSO4↓+2HCl)
(1)该实验过程中产生沉淀的总质量为 g。
(2)该BaCl2溶液中溶质的质量分数(写出计算过程)。
| 第1次 | 第2次 | 第3次 | |
| 加入硫酸溶液的质量/g | 10 | 10 | 10 |
| 过滤后溶液的质量/g | 105 | 105 | 111.7 |
根据以上数据计算:(BaCl2+H2SO4═BaSO4↓+2HCl)
(1)该实验过程中产生沉淀的总质量为 g。
(2)该BaCl2溶液中溶质的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】硫酸是重要的化工原料,也是实验室常用的化学试剂。某同学将7.1g表面氧化的铝片放入193g稀硫酸中恰好反应,测得生成气体0.6g。已知氧化铝和稀硫酸发生如下反应: ,回答下列问题。
,回答下列问题。
(1)氧化铝中铝元素和氧元素的质量比为_______ 。
(2)求铝片中铝单质的质量_____ ;
(3)求反应后溶液的溶质质量分数_____ 。(写出计算过程)
 ,回答下列问题。
,回答下列问题。(1)氧化铝中铝元素和氧元素的质量比为
(2)求铝片中铝单质的质量
(3)求反应后溶液的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】计算题:小 家乡有一跨河的铁索桥,小
家乡有一跨河的铁索桥,小 欲检测铁索的锈蚀程度,判断铁索桥是否存在安全隐患,他将
欲检测铁索的锈蚀程度,判断铁索桥是否存在安全隐患,他将 已生锈的铁索(注:生锈的铁索中只含氧化铁和铁)放入一定浓度的稀盐酸中充分反应,测得产生气体的质量与稀盐酸的质量关系如图所示。请回答:
已生锈的铁索(注:生锈的铁索中只含氧化铁和铁)放入一定浓度的稀盐酸中充分反应,测得产生气体的质量与稀盐酸的质量关系如图所示。请回答:

(1)该生锈的铁索中铁的质量为______  。
。
(2)求所用稀盐酸溶质的质量分数。(写出计算过程)
 家乡有一跨河的铁索桥,小
家乡有一跨河的铁索桥,小 欲检测铁索的锈蚀程度,判断铁索桥是否存在安全隐患,他将
欲检测铁索的锈蚀程度,判断铁索桥是否存在安全隐患,他将 已生锈的铁索(注:生锈的铁索中只含氧化铁和铁)放入一定浓度的稀盐酸中充分反应,测得产生气体的质量与稀盐酸的质量关系如图所示。请回答:
已生锈的铁索(注:生锈的铁索中只含氧化铁和铁)放入一定浓度的稀盐酸中充分反应,测得产生气体的质量与稀盐酸的质量关系如图所示。请回答:
(1)该生锈的铁索中铁的质量为
 。
。(2)求所用稀盐酸溶质的质量分数。(写出计算过程)
您最近一年使用:0次